为什么浓硫酸具有强吸水性和脱水性?
时间:2022-03-07 11:10 来源:未知 作者:化学自习室 点击: 次 所属专题: 浓硫酸 吸水性 脱水性
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
为什么浓硫酸与水有着如此强烈的结合作用?都说结构决定性质,下面我们就来看看硫酸分子的结构吧!
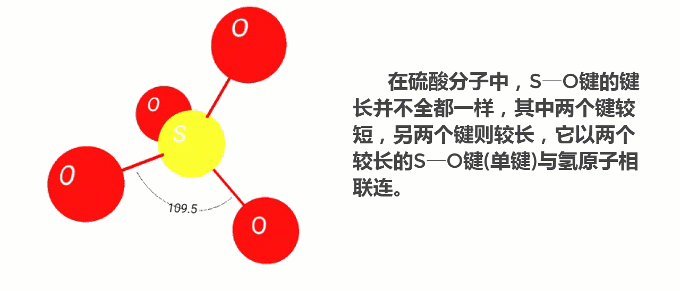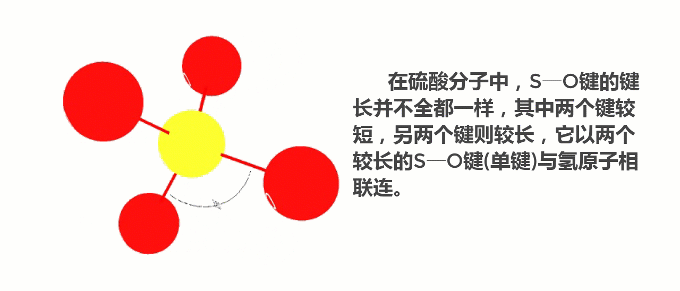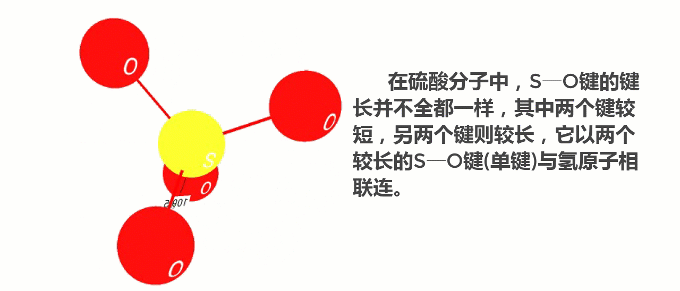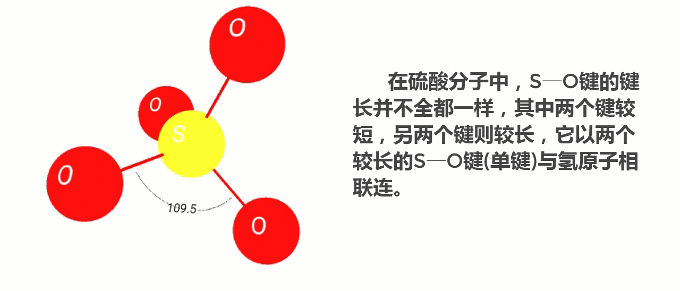
《无机化学丛书》2011年版第5卷中有介绍:在无水硫酸中,每个四面体形的硫酸分子通过氢键与相邻的4个硫酸分子联接而形成层状结构,在浓硫酸中也存在着类似的情况,故它们皆呈油状。也正是由于氢键的存在,硫酸分子间的作用力较强,沸点高达337℃。
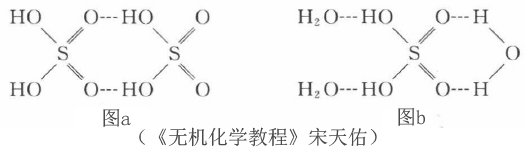
那为什么浓硫酸具有强吸水性和脱水性呢?原来,除了硫酸分子间会形成氢键外(见图A),硫酸分子与水分子间也可以形成较强的氢键(见图B),并且水合时放热较多,因此浓硫酸具有很强的吸水性与脱水性。
另外,吉林大学宋天佑教授等编著的《无机化学》下册中也有如下描述:
硫酸是SO3的水合物,除了硫酸H2SO4(SO3·H2O)和焦硫酸H2S2O7(2SO3·H2O)外,SO3和H2O还生成一系列的其它水合物:
H2SO4·H2O (SO3·2H2O)
H2SO4·2H2O (SO3·3H2O)
H2SO4·4H2O (SO3·5H2O)
这些水合物很稳定,因此浓硫酸有很强的吸水性。当它与水混合时由于形成各种水合物而释放出大量的热,若不小心将水倾入浓H2SO4中,将会因为产生巨大的热量而导致爆炸。因此在稀释硫酸时,只能在搅拌过程中把硫酸缓慢地倾入水中,绝不能把水倾入硫酸中。
由于硫酸的强氧化性和脱水性,它对于动植物组织有很强的腐蚀性,如果在工作中不小心将浓硫酸洒落在皮肤上,应该立即用大量水冲洗(勿用力摩擦!),然后用稀氨水浸润伤处,最后再用水冲洗,这样才不至于造成严重的灼伤。
浓硫酸是工业上和实验室中最常用的干燥剂,用来干燥不与浓硫酸起反应的各种物质,如氯气、氢气和二氧化碳等气体。浓硫酸不但能吸收游离的水,而且还能从一些有机化合物(即碳水化合物,如蔗糖、布、纸等)中,夺取与水分子组成相当的氢和氧,使这些有机物碳化,例如蔗糖或纤维可被浓硫酸脱水:


- 全部评论(0)
