利用空气吹出法从海水中提溴工艺简介
时间:2022-10-26 11:18 来源:未知 作者:化学自习室 点击: 次 所属专题: 海水提溴
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、 “ 海洋元素” — 溴
溴是第一个从海水中发现并分离成功的元素。1825 年, 法国青年化学家巴拉德首次从浓缩海水中发现并提取了溴。单质溴为红棕色液体, 室温下挥发成红棕色蒸气, 有刺激恶臭, 微溶于水, 易溶于乙醇等有机溶剂。溴是强氧化剂, 能强烈灼伤皮肤, 对金属有强烈腐蚀性。溴在岩石圈的分布虽较广泛, 但其丰度很低 ( < 100 ug/ kg) 。溴的天然资源主要是海水和古海洋的沉积物即岩盐矿。地球上约 99% 的溴存在于海水中, 所以溴有 “ 海洋元素”之称。海水中含溴约 65 mg/ L, 属于丰度较大的微量元素。某些岩盐矿的母液和盐湖水中, 亦含有海源溴化物。此外某些海洋生物体含有小量化合态的溴,如海兔毒素、二溴靛蓝等。
溴及溴产品在国民经济中有着重要应用, 它主要用于多种化合物的制备。溴是制取溴的化合物的原料; 在医药上用以生产抗菌素、维生素、激素中间体; 在农药上用以制造杀虫剂、熏蒸剂、植物生长激素; 在其他工业上制造染料、香料、摄影材料、合成纤维、催泪性毒气、灭火剂、二溴乙烷抗震剂。特别是近代, 随着塑料工业的发展和高层建筑的突起, 对溴系阻燃剂的需求大增。此外, 世界上禁止使用氟利昂制冷剂, 用溴化锂作制冷剂的需求量骤增, 因此国内老式生产溴是供不应求, 海水提溴日益紧迫 。
二、溴的生产方法简介
溴的生产方法有空气吹出法、水蒸汽蒸馏法、连续双过程真空提溴法、树脂法、液膜法、半透膜法、溶剂萃取法等。其中, 水蒸汽蒸馏法和空气吹出法的应用最为普遍。产溴大国 ———美国与以色列分别以天然盐湖 ( 含溴量 1 ~ 6 g/ L) 与死海卤 水 ( 提取氯化钾后母液含溴量为 10 ~ 12 g/ L) 为原料提取溴, 由于卤水本身溴含量高, 宜采用水蒸汽蒸馏法和空气吹出法, 工艺完善, 成本较低, 产量高,仅此 2 国的溴产量占全世界的 60% 。而我国溴生产主要集中在环渤海湾、潍坊地区, 生产原料是盐场晒盐或海水淡化后的浓海水和地下苦卤水, 溴含量 ( 约 01 2 ~ 01 3 g/ L) , 与美国和以色 列原料中的溴含量相比低得多, 目前生产工艺全部采用水蒸汽蒸馏法和空气吹出法。水蒸汽蒸馏法约占全国溴生产能力的 10% 。空气吹出法约占全国溴生产能力的 90%。
1、空气吹出法
1815—1826 年, 法国的 巴拉德和德国的凯尔勒维格先后提出空气吹出法, 1907 年德国的库比尔斯基对该方法进行重大改进, 现为最成熟、最普遍采用的提溴工艺, 可从低浓度含溴卤水 ( 2 ~4 g/ L) 或海盐生产过程中的卤水中提溴。其基本原理: 溴离子被氯气氧化为游离溴后, 根据溴的气、液相浓度之间的气液平衡关系被空气从卤水中吹出, 再以吸收剂吸收, 吸收后再通入氯气氧化或加酸酸化使溴游离出来, 最后在水蒸气的气提作用下脱离液相经过冷凝得到溴。国际上广泛采用的吸收剂是纯碱或烧碱溶液, 二氧化硫、铁屑及低温溴盐溶液, 按吸收剂不同可将空气吹出法分为碱液吸收法和酸液吸收法[ 7] 。
我国于 20 世纪 70 年代初利用空气吹出法对地下卤水进行提溴获得成功后, 80 年代后的新建溴厂基本都采用该法。
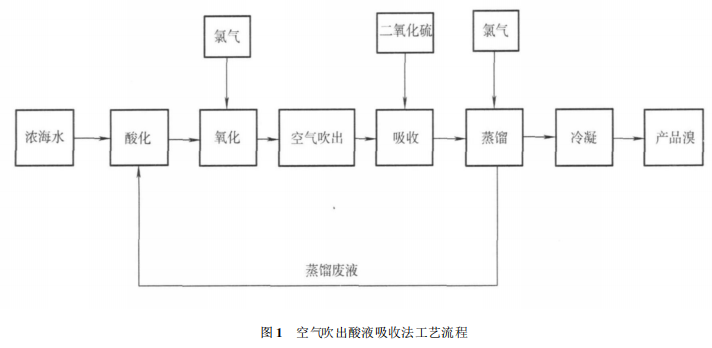
①空气吹出酸液吸收法
第 1 步:酸化, 向生产原料浓海水 ( 其含溴范围:Br- 60 ~ 400 mg/ L) 加入硫酸或盐酸酸化,浓海水的 pH控制在21 5 ~ 41 5。
第2 步:氧化, 向酸化的浓海水通入氯气, 浓海水中的溴离子被氧化:2Br-+ Cl2=2Cl- +Br2 , 生成游离溴。
第 3步:空气吹出, 氧化后的浓海水经管道送到吹出塔顶部, 再用空气鼓风机将游离溴吹出。
第 4步:吸收, 将含大量游离溴的空气导入吸收塔, 通入二氧化硫气体, 将空气中的游离溴转化为雾状的氢溴酸: SO2 + Br2 + 2H2O=2HBr+H2SO4, 得到氢溴酸富集液。
第5 步:蒸馏, 把氢溴酸富集液导入蒸馏塔,从塔底通入氯 气, 把氢溴酸氧化为游离溴:2HBr+ Cl2=2HCl+ Br2 , 溴蒸气从塔顶排出, 经过冷凝、溴水分离, 精制得到高品质的产品溴。
②空气吹出碱液吸收法
1931 年, 美国Dow化学公司采用空气吹出碱液吸收法从海水中提溴的中试成功, 1934 年首先将其工业化, 20 世纪 90 年代初全球用此法生产的溴占90% 。碱法制溴工艺的生产过程类似于酸法制溴, 只是吸收与蒸馏环节不同: 吸收液用碱液,与游离溴发生歧化反应生成溴化物和溴酸盐。
使用氢氧化钠溶液作吸收液发生的基本反应为:
海水氧化:2Br- + Cl2= 2Cl- + Br2
碱液吸收:6NaOH+ 3Br2 =5NaBr + NaBrO3 + 3H2O
蒸馏:5NaBr+ NaBrO3 + 3H2SO4=3Na2SO4 + 3Br2
使用碳酸钠溶液作吸收液发生的基本反应为:
海水氧化:2Br- + Cl2 =2Cl- + Br2
碱液吸收:3Br2 + 3Na2CO3=5NaBr + NaBrO3 + 3CO2↑
蒸馏:5NaBr+ NaBrO3 +3H2SO4=3Na2SO4 + 3Br2
目前, 我国90% 以上溴生产采用空气吹出酸液吸收法。该法设备台数少, 与空气吹出碱液吸收法相比, 吸收液含溴量高 30% ~ 40% , 蒸气消耗量低约 30% 左右, 耗电量低 ( 低 35% ~ 40% ) , 节省化碱、化酸工艺, 氯气和二氧化硫消耗少。在我国, 江苏、四川、浙江、天津多采用碱法吸收工艺, 山东较多采用酸法吸收工艺。空气吹出法对原料含溴量适应性较强, 易于自动化控制, 但缺点在于需要庞大的设备和高能耗。
目前, 我国溴深加工的能力已有明显进步,但在技术上却多是照套图纸异地建设, 而作为关键设备的填料塔及塔内件多是循着其他行业的步子根据别人的结论选用的。 国内亦曾自行设计配套自动控制系统, 未经正常运转就被迫停止。 目前全部是依靠经验, 人工操作阀门控制生产过程,使相当多的溴厂工艺条件波动范围很大, 原料消耗增加, 总收率下降。所以, 亟待进 一步提高工艺水平。

- 全部评论(0)
