电价数、共价数和氧化数
时间:2017-04-18 09:46 来源:未知 作者:关平 点击: 次 所属专题: 化合价 氧化数
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
化合价是元素的重要性质,它是指元素化合时彼此的数量关系,即元素化合时其原子个数是以怎样的比值进行的这一性质。电价和共价是指两类化合价。电价存在于离子化合物中。元素的一个原子形成离子化合物时所得到或失去的电子数,就称为电价数。电价数有正、负之分。
如MgO中镁显+2价,氧显-2价。在共价化合物中元素的化合价叫共价,其值等于这种元素的一个原子跟其他元素的原子化合时所形成的共用电子对数。共价数没有正、负之分。如水中氢为1价,氧为2价。有时共价数不能从分子式直接推出,只能根据分子结构来确定。
氧化数是对原子而言的。它表示化合物分子中各元素原子在形式上或表观上所带的电荷数。1970年,国际纯粹一应用化学联合会对原子的氧化数下过明确的定义:“氧化数是某元素的一个原子的荷电数,这种荷电数由假设每个键中的电子指定给电负性更大的原子而求得。”
例如,过氧化氢分子中氢原子氧化数为+1,氧原子的氧化数为-1。Cl2分子中共用电子对不发生偏移,氯原子有观上不带电,它们的氧化数就定为0,但是Cl2中氯元素的共价数却不为0。一般说来,原子在离子化合物中氧化数跟它(离子)所带的电荷数相同,共价化合物中原子的氧化数则等于两原子间偏移的共用电子对数。
元素的化合价和原子的氧化数的区别可以总结为下表:
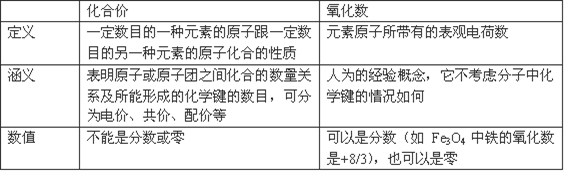
中学课本中所说的元素化合价实际上常指原子的氧化数,或者说化合价和氧化数概念往往混用。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
