凯氏定氮法测定食品中蛋白质及在高考中应用
时间:2017-06-28 10:20 来源:未知 作者:黄晓东 点击: 次 所属专题: 蛋白质 凯氏定氮法
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
工艺技术
蛋白质被认为是构成生物体细胞组织的重要成分。食物中的蛋白质是人体中氮的唯一来源,具有糖类和脂肪不可替代的作用。含氮量是蛋白质区别于其他有机化合物的重要标志。
在检验食品中蛋白质时,通常是先检定出食品中的总氮量,然后乘以蛋白质换算系数,以此得到蛋白质含量。
凯氏定氮法由 Kieldahl 于 1883 年首先提出,至今仍被作为标准检验方法。
凯氏定氮法测定蛋白质分为样品消化、蒸馏、吸收和滴定过程。
原理
向样品中加入浓硫酸和催化剂,充分混匀,然后加热消化分解,样品中碳和氢被氧化成二氧化碳和水,其中的有机氮转化为硫酸铵。碱化蒸馏使氨游离,用硼酸吸收后以硫酸或盐酸标准滴定溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质的含量。
转换因子
转换因子是通过凯氏定氮法测得的氮换算为蛋白质的系数。理想状态下的蛋白质中的氮含量约为16%,所以测量值乘以6.25即为蛋白质量。下表为总结出的转换因子数值。
| 样本 | 转换因子 |
| 乳制品 | 6.38 |
| 面粉 | 5.70 |
| 玉米、高粱 | 6.24 |
| 花生 | 5.46 |
| 大米 | 5.95 |
| 大豆 | 5.71 |
| 肉 | 6.25 |
| 大麦、小米、燕麦、裸麦 | 5.83 |
| 芝麻、向日葵 | 5.30 |
样品消化
浓硫酸具有脱水性和氧化性,可使有机物中的碳、氢被氧化为二氧化碳和水,蛋白质会分解为氨,然后氨与硫酸结合生成硫酸铵。通常加入硫酸钾和硫酸铜作为催化剂来加快蛋白质分解。硫酸钾可以提高溶液的沸点,一般情况下,纯硫酸的沸点在 340 ℃左右,但是在添加硫酸钾后,可提高至 400 ℃以上。提高温度使有机物加快分解。但是不能加入过多的硫酸钾,否则会因为温度过高,使生成的硫酸铵发生热分解成氨而造成损失。硫酸铜除作为催化剂外,还可以指示消化终点的到达,有机物全部消化完全后,溶液呈现清澈的蓝绿色,硫酸铜还可以做蒸馏时碱性反应的指示剂。
蒸馏
消化液中的硫酸铵在碱性环境下会转化成氨。为防止水中微量的氨气受热逸出,影响测定结果,所以水蒸气发生器中的水要保持酸性。硫酸铵是一种强酸弱碱盐,需要足够的碱液使结合态的氨完全反应并释放出来,这个过程中的氢氧化钠一定要过量,过量的氢氧化钠会与硫酸铜生成蓝色的氢氧化铜沉淀,氢氧化铜受热分解成黑色的氧化铜沉淀。检验蒸馏是否完成,可用奈氏试纸法,NH4+或 NH3遇奈氏试剂会反应生成棕红色的碘化汞铵化合物。
吸收
加热蒸馏放出的氨可用硼酸溶液吸收,硼酸有吸收氨的作用,又因其呈微弱酸性,不影响下一步滴定时指示剂的变色反应。温度过高会使硼酸吸收液对氨的吸收作用减弱,从而造成损失,故一般不超过 40 ℃。
NH3+H2BO3=NH3·H3BO3;
滴定
待吸收完全后,用硫酸或者盐酸标准溶液进行酸碱滴定,滴定液的浓度直接影响结果的准确性,必须按照要求进行配制和标定。混合指示剂在中性溶液中呈灰色,滴定终点时液体呈灰色。
NH3·H3BO3+HCl= NH4Cl+H3BO3。
注意事项
①所用的试剂溶液应用无氨蒸馏水配制;
②取样应具有代表性 , 取样前将样品充分混匀;
③样品称量放入凯氏烧瓶时,切勿使样品粘附在瓶颈部,避免样品未消化完全而造成氮损失;
④为了保证使烧瓶壁上的残渣消化完全,在消化过程中要不时地转动凯氏烧瓶;
⑤消化脂肪或糖含量较高的样品时,易产生大量泡沫,为防止泡沫溢出,消化时应先消化加热并不断摇动,或者加入少量辛醇或液体石蜡或硅油消泡剂;
⑥当样品消化液浑浊或未澄清透明时,可先将凯氏烧瓶放冷至室温后,再加入 30% 的过氧化氢,然后继续加热消化;
⑦加碱后,漏斗要进行水封,避免因装置漏气造成氨的逸出影响结果的准确性;
⑧要保证蒸馏装置不能漏气;
⑨在蒸馏时反应室与外界存在的压力差,蒸汽可将氨带出。故蒸馏时,要保证蒸汽均匀、充足,中间不能停止加热,防止发生倒吸;
⑩蒸馏前如果加碱后消化液呈蓝色而没有生成氢氧化铜沉淀,说明加入的碱量不足,需要适量补加碱;
蒸馏时为防止水蒸气发生器内液体爆沸,加入几片碎瓷片或大的玻璃珠,玻璃珠直径最好大于联通的玻璃管直径,以免玻璃珠进入玻璃管内影响蒸汽均匀、充足的输出;冷凝管下端要插入硼酸吸收液液面以下,防止氨逸出,蒸馏完毕后先将冷凝管下端提离液面,再蒸 1 min后清洗管口,再移开吸收瓶,最后关掉热源,否则可能发生倒吸。
结语
凯氏定氮法经典、准确,适用于食品中蛋白质的测定。但是因样品中一般会含有一些非蛋白质的含氮化合物,所以凯氏定氮法测定结果为样品中粗蛋白质含量。然而,此法实际上测的不是蛋白质含量,而是通过测氮含量来推算出样品中蛋白质的含量。
在凯氏定氮法中消化操作的条件是产生误差的主要原因,因此要格外注意。
在实际的生产实验中,每一步应该严格按照标准的规定来进行操作。本文为笔者日常工作实验总结所得,望对实验者有些许帮助。
2017年高考
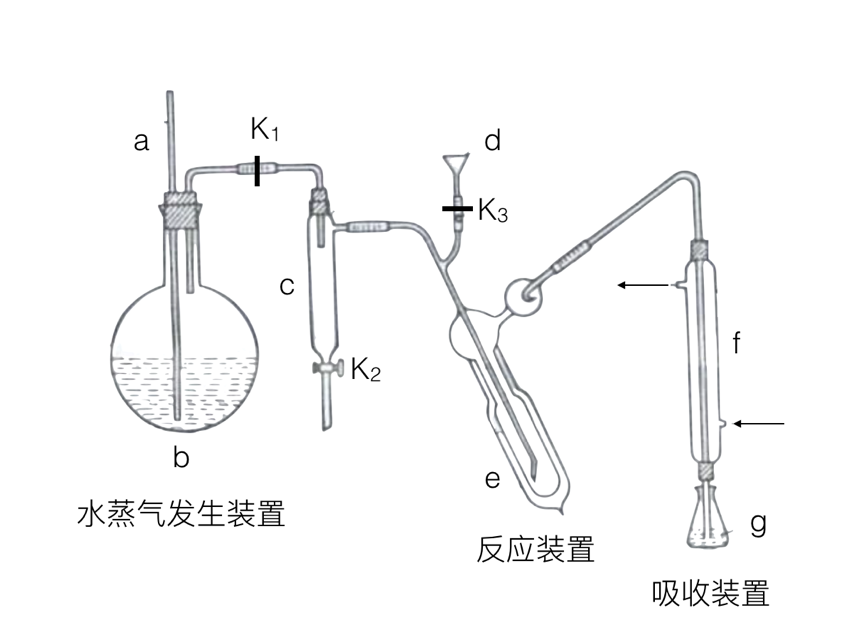
凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。已知:NH3+H2BO3=NH3·H3BO3;NH3·H3BO3+HCl= NH4Cl+H3BO3。

回答下列问题:
(1)a的作用是____________________。
(2)b中放入少量碎瓷片的目的是___________________。f的名称是_______________。
(3)清洗仪器:g中加蒸馏水;打开K1,关闭K2、K3,加热b,蒸气充满管路;停止加热,关闭K1,g中蒸馏水倒吸入c,原因是____________________;打开K2放掉水。重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭K3,d中保留少量水。打开K1,加热b,使水蒸气进入e。
①d中保留少量水的目的是____________________
②e中主要反应的离子方程式为____________________。e采用中空双层玻璃瓶的作用是____________________。
(5)取某甘氨酸(C2H5NO2)样品m克进行测定,滴定g中吸收时消耗浓度为c mol·L-1的盐酸V mL,则样品中氮的质量分数为_______%,样品的纯度≤______ %。
解析:本题考查实验方案设计与评价。蛋白质是含氮的有机化合物。蛋白质与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,并换算成蛋白质含量。题给装置为定氮蒸馏装置,b为蒸汽发生瓶、c为汽水分离管、e为反应管使氨气完全蒸馏出来、g为氨气吸收装置。
(1)a管插入水中起安全瓶作用,若烧瓶内气压过高水会进入a管中维持压强平衡。
(2)b中放入少量碎瓷片的目的是防止暴沸,f的名称是直型冷凝管。
(3)清洗仪器时,停止加热,关闭K1,c中水蒸气冷凝为水后,装置内气体压强小于外界大气压,在外界大气压的作用下,g中蒸馏水由e倒吸进入c中,起到清洗仪器的目的。
(4)d中保留少量水可以防止氨气逸出,也可以用PH试纸试馏出液是否为碱性检验氨是否完全蒸馏出来。e采用中空双层玻璃瓶的作用是减少热量损失,有利于铵根转化为氨气逸出。
(5)由题意可知甘氨酸中n(C2H3NO2)=n(N)= n(HCl)=cV×10-3mol,则样品中氮的质量分数为![]() ,样品的纯度≤
,样品的纯度≤![]() 。
。
答案:
(1)安全管,烧瓶内气压过大,水会进入a管中维持压强平衡
(2)防止暴沸 直型冷凝管
(3)c、e及其所连接的管道内水蒸气冷凝为水后,气压远小于外界大气压,在大气压的作用下,锥形瓶内的蒸馏水被倒吸入c中
(4)①防漏气,便于检验d氨是否完全蒸馏出来
②NH4++OH-![]() NH3↑+H2O,减少热量损失,有利于铵根转化为氨气逸出
NH3↑+H2O,减少热量损失,有利于铵根转化为氨气逸出
(5)![]() ,
,![]()

- 全部评论(0)
