常见晶体的结构类型及分析
时间:2020-06-11 18:05 来源:未知 作者:化学自习室 点击: 次 所属专题: 晶体结构模型
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
晶体 | 晶体结构示意图 | 晶体中微粒分布详解 |
氯化钠晶体 |
| Na+和Cl-交替占据立方体的顶点而向空间延伸。在每个Na+周围最近的等距离(设为a)的Cl-有6个(上、下、左、右、前、后),在每个Cl-周围最近的等距离为Na+亦有6个,这6个离子构成一个正八面体;在每个Na+周围最近的等距离(必为 |
氯化铯晶体 |
| 每8个Cs+、八个Cl-各自构成立方体,在每个立方体的中心有一个异种离子(Cs+或Cl-)。在每个Cs+周围最近的等距离(为 |
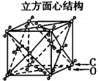
二氧化碳晶体 |
| 每8个CO2构成立方体且在6个面的中心又各占据1个CO2。在每个CO2周围等距离( |
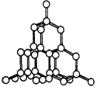
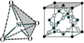
金刚石晶体 |
| 每个C与另4个C以共价键结合,前者位于正四面体中心,后四者位于正四面体顶点。晶体中所有C-C键长相等、键角相等(均为109°28′);晶体中最小碳环由6个C 组成且六者不在同一平面内;晶体中每个C参与了4条C-C键的形成,而在每条键中心的贡献只有一半,故C原子数与C-C键数之比为1:2 |
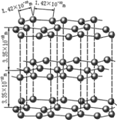
石墨晶体 |
| 层内存在共价键、金属键,层间以范德华力结合,兼具有原子晶体、金属晶体、分子晶体的特征。在层内,每个C与3个C形成C-C键,构成正六边形,键长相等,键角相等(均为120°);在晶体中,每个C参与了3条C-C键的形成,而在每条键中的贡献只有一半,每个正六边形平均只占6×1/3=2个C,C原子个数与C-C键数之比为2:3 |
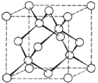
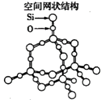
二氧化硅晶体 |
| 每个Si与4个O结合,前者在正四面体的中心,后四者在正四面体的顶点;同时每个0被两个正四面体所共用。正四面体内键角为109°28′,每个正四面体占有一个完整的Si,四个“半O原子”,故晶体中Si原子与O原子个数比为1:(4×1/2)=1:2(可看作是金刚石结构中的每个碳原子之间插入一个氧原子,再将碳原子换成硅原子) |

- 全部评论(0)
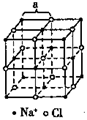
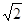 A)的Na+有12个(同层4个、上层4个,下层4个),在每个Cl-周围最近的等距离的Cl-亦有12个
A)的Na+有12个(同层4个、上层4个,下层4个),在每个Cl-周围最近的等距离的Cl-亦有12个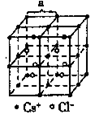
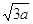 /2)的Cl-有8个,在每个Cs+周围最近的等距离(必为A)的Cs+有6个(上、下、左、右、前、后),在每个Cl-周围最近的等距离的Cl-亦有6个
/2)的Cl-有8个,在每个Cs+周围最近的等距离(必为A)的Cs+有6个(上、下、左、右、前、后),在每个Cl-周围最近的等距离的Cl-亦有6个