氢键最全的知识点及其应用
时间:2023-04-27 10:08 来源:未知 作者:化学自习室 点击: 次 所属专题: 氢键02
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、氢键
1、概念:一种特殊的分子间作用力
2、形成条件:①与电负性大且半径小的原子(F、O、N)相连的 H;②在附近有电负性大, 半径小的原子(F、O、N)
3、表示方法:X—H... Y—。
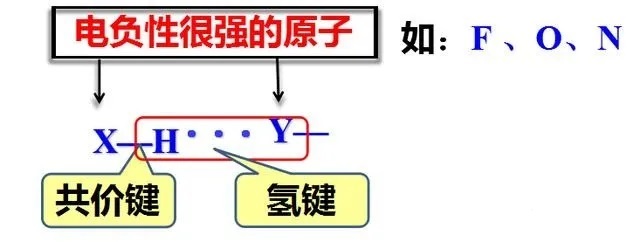
氢键是一种静电作用,是除范德华力外的另一种分子间作用力;氢键的大小介于化学键与范德华力间,不属于化学键,但有键长、键能,氢键具有饱和性、方向性。
二、氢键的存在
1、分子间氢键 。如:C2H5OH、CH3COOH、H2O 、HF、NH3相互之间
2、分子内氢键 。如:苯酚邻位上有-CHO、-COOH、-OH和-NO2时,由氢键组成环的特殊结构
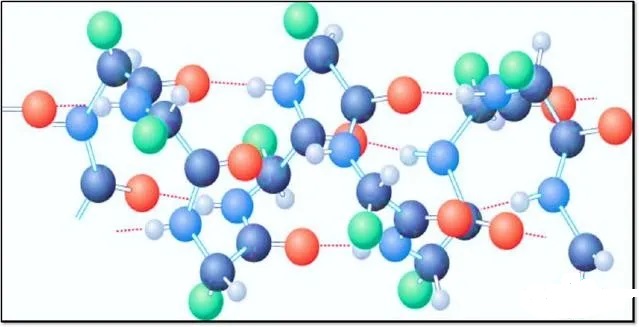
生物大分子中也存在的氢键
三、氢键的强弱
(1)、X—H ... Y—:X和Y的电负性越大,吸引电子能力越强,则氢键越强。如:F 电负性最大,得电子能力最强,因而F-H…F是最强的氢键。
(2)、氢键强弱顺序:F-H…F > O-H…O > O-H…N > N-H…N (注意:C原子吸引电子能力较弱,一般不形成氢键)。
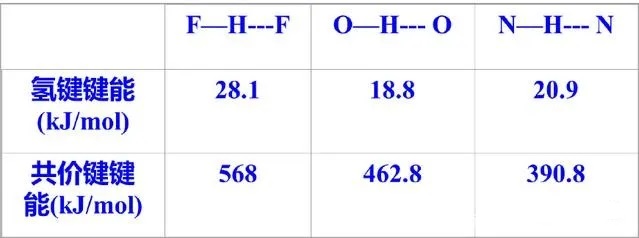
氢键强弱比较
四、对物质熔沸点的影响
分子间能形成氢键的物质,一般都具有较高的熔点和沸点,这是因为固体熔化或液体气化时除了破坏范德华力外,还必须破坏分子间氢键,从而需要消耗更多的能量。在同类化合物中能形成分子间氢键的物质,其熔沸点比不能形成分子间氢键的高。如,第VIA 族元素的氢化物,由H2Te、H2Se 到H2S,随相对分子量的递减,分子间作用力递减,熔沸点依次降低;但H2O 分子间形成了O-H…O 氢键,分子间作用力增强,H2O 的熔沸点陡然升高。
分子内氢键的形成使物质的熔沸点降低。如,邻、间、对硝基苯酚的熔点分别为45℃、96℃、114℃,这是由于间位、对位硝基苯酚中存在分子间氢键,熔化时必须破坏其中的一部分氢键,熔点较高;而邻硝基苯酚中形成分子内氢键,不形成分子间氢键,故熔点较低。
五、对物质溶解性的影响
如果溶质分子与溶剂分子之间形成氢键,则溶质的溶解度会骤增。
如,氨在水中的溶解度大于其他气体,在20℃时,1 体积水吸收700 体积的氨。氨在水中的溶解度特别大,是由于水分子和氨分子通过氢键互相结合形成氨的水合物;乙醇、乙二醇、丙三醇等可与水以任意比混溶,皆源于此。
如果溶质分子形成分子内氢键,则在极性溶剂中的溶解度减小,在非极性溶剂中的溶解度增大。
六、对有机化合物酸性的影响
以羧酸为例,影响羧酸酸性的因素很多,任何能使羧酸负离子比羧酸更加稳定的因素都使羧酸酸性增大;反之,使羧酸酸性减弱。氢键使羧酸根负离子更稳定,使得羧酸的酸性增强。在质子溶剂中,如果羧酸根负离子能被溶剂通过氢键稳定,将同样能观察到其酸性增强的现象。例如乙酸在不同溶剂中的PKa如表1 所示。
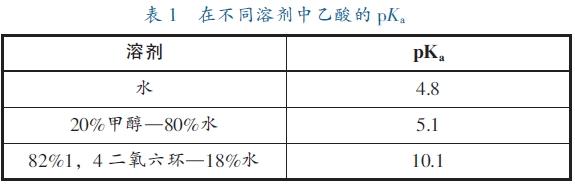
分子内氢键的形成同样会影响羧酸的酸性强弱。最典型的例子是邻羟基苯甲酸的酸性,由于它的羧酸根负离子可与邻位羟基生成氢键,使负离子稳定性大大提高,因而酸性(pKa=2.98) 比对羟基苯甲酸的酸性(pKa=4.57) 强很多。
七、对物质粘度和表面张力的影响
当分子间形成氢键时,分子间作用力增大,流动性减小,粘度增大。一般情况是能形成分子间氢键的物质比不能形成分子间氢键的物质的粘度大。醇和羧酸能形成分子间氢键,而烷烃、酮和酯等则不能,因此醇和羧酸的粘度比分子量相同的烷烃、酮和酯大。甘油、磷酸、浓硫酸等多羟基化合物,由于分子间可形成众多的氢键,这些物质通常为粘稠状液体。
分子内氢键对化合物粘度的影响与分子间氢键不同。存在分子内氢键的化合物相对于存在分子间氢键的化合物,其分子间作用力小,分子流动性变大, 粘度变小。如,邻羟基苯甲醛的粘度比对位异构体小;在硝基苯酚的异构体中,邻位异构体的粘度小。
水的表面张力很大,其根源也在于水分子间的氢键。物质表面能的大小和分子间作用力大小有关,因为表面分子受到液体内部分子的吸引力,向液体内部挤压,能量较高,有使表面自动缩小的趋势,见表2。
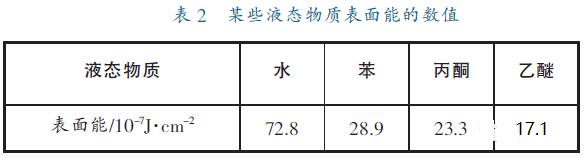
表中所列液态物质中,水的表面能最高,因为水分子之间有强的氢键作用。若加表面活性剂破坏表面层的氢键体系就可降低表面能,这在工业生产中有着重要的意义。
八、影响物质的密度
物质的分子间作用力越大,分子排列越紧密,密度越大。直链烷烃分子随着碳原子数增多,分子间作用力增大,密度变大。
分子间氢键对化合物的密度同样也产生影响。如,醇能形成分子间氢键,低碳醇的密度比分子量相近的烷烃高;随着分子量的增加,烃基部分所占比例增加,阻碍了分子间氢键的形成,高碳醇密度与分子量相近的烷烃的差值逐渐减小。二元醇分子中含有两个羟基,它们形成氢键的能力更强。乙二醇的密度是1.113g·cm-3,比同碳数乙醇密度(0.789g·cm-3)高,比分子量相近的丙醇密度(0.804 g·cm-3) 也高。羧酸能形成强的氢键,羧酸的密度比相应的烷烃和醚高,比相应的醇也高。
液体分子间若形成氢键,有可能发生缔合现象,分子缔合的结果会影响物质的密度。如,·nH2O(H2O)n,常温下液态水中除了简单H2O 分子外,还有(H2O)2,(H2O)3,…,(H2O)n等缔合分子存在。
降低温度有利于水分子的缔合。
九、氢键在生命物质中的作用
生命物质由蛋白质、核酸、糖类、脂类等有机物以及水和无机盐组成,这些物质结合在一起具有生命的特性,氢键在其中起关键的作用。蛋白质是由一定序列的氨基酸缩合形成的多肽链分子,它富含形成氢键结合的能力。在多肽主链中的N-H 作为质子给体,C=O作为质子受体,互相形成C=O…H-N 氢键,决定了蛋白质的二级结构。脱氧核糖核酸(DNA) 分子中,两条多核苷酸链靠碱基(C=O…H-N 和C=N… H-N) 之间形成氢键配对而相连,即腺嘌呤(A)与胸腺嘧啶(T) 配对形成2 个氢键,鸟嘌呤(G) 与胞嘧啶(C) 配对形成3 个氢键,它们盘曲成双螺旋结构的各圈之间也是靠氢键维系而增强其稳定性。一旦氢键被破坏,分子的空间结构发生改变, 生物生理功能就会丧失。

- 全部评论(0)
