气压原理的分析及应用
时间:2020-12-28 14:40 来源:未知 作者:化学自习室 点击: 次 所属专题: 实验与压强
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
气压原理的分析和应用一直是高考中的热点,考查角度比较广泛,但是学生往往缺少理想的模型分析和规范化的语言表达。如2018年全国卷I原理综合题中二氧化氮转化为四氧化二氮的可逆反应,升高温度,压强怎么变化及原因。
气压原理在以往高考(全国卷)中很少单独出题,往往融合在实验综合题及原理综合题中出现,但在2020年全国卷III中单独作为选择题考查了“喷泉实验”原理。
2021高考继续关注以下气压原理考点:(1)分析模型;(2)喷泉实验;(3)气密性检验;(4)防倒吸;(5)压送液体;(6)减压过滤;(7)减压蒸馏;(8)减压蒸发;(9)减压干燥等。多关注教材实验模型。
一、模型搭建:气压的分析
PV=nRT→P=(nRT)/V
影响气体压强的因素:气体分子的物质的量;温度;容器的体积
典例分析:
2018全国卷I T28:
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=﹣44kJ•mol﹣1
2NO2(g) N2O4(g) ΔH2=﹣55.3kJ•mol﹣1
N2O4(g) ΔH2=﹣55.3kJ•mol﹣1
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强P∞(35℃) ______ 63.1KPa(填“大于”“等于”或“小于”),原因是______ 。
1.应用模型:影响气体压强的三个因素(气体分子数;温度;体积)
2.分析题中问题:在恒容条件下,升高温度,气体压强增大;升高温度,2NO2(g) N2O4(g)平衡逆向移动,气体分子数增多,气压增大。
N2O4(g)平衡逆向移动,气体分子数增多,气压增大。
二、检查装置的气密性 (装置气密性检查必须在放入药品之前进行。)
检验原理:密封体系---制造气压差---现实证明气压差稳定存在。
常用方法:微热法或液差法。
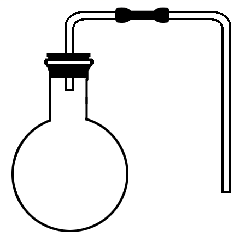
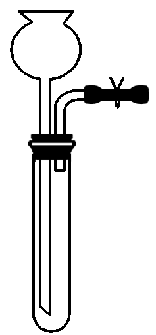
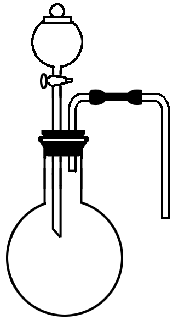
方法一:关闭分液漏斗活塞,将导气管没入水中,用手掌捂住(或用酒精灯微热)圆底烧瓶,若导管口有气泡冒出,松开手掌(或撤去酒精灯),导管中形成一段稳定水柱,说明气密性良好。
方法二:导气管用止水夹封闭,打开分液漏斗活塞,向其中注入水,若水不能顺利滴下,在分液漏斗中形成稳定液面,则说明装置气密性良好。
针对练习:
已知SO2可以用Fe(NO3)3溶液吸收,某学习小组据此按如图装置展开如下相关探究:取一定量的铜片于三颈烧瓶中,通入一段时间N2后再加入足量的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀。
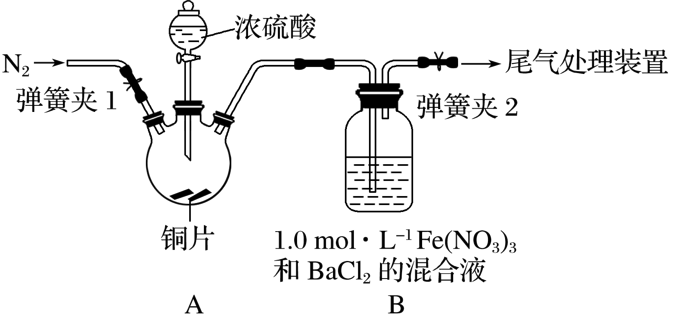
回答下列问题:
装置A中用于添加浓硫酸的仪器名称为__________;检查图中连通装置A、B气密性的方法是_____________
答案:
方法1:关闭弹簧夹1和分液漏斗的活塞,打开弹簧夹2,用手捂热烧瓶A,若B中导管口有气泡冒出,冷却后,导管中有一段液柱上升,则气密性良好,否则气密性不好
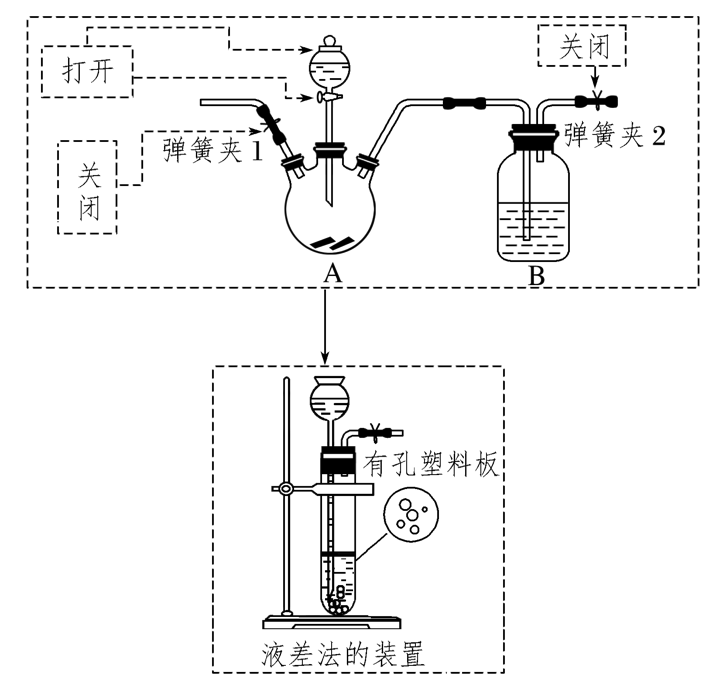
方法2:关闭弹簧夹1和弹簧夹2,打开分液漏斗活塞,向分液漏斗中加水至水不流下,停止加水;观察一段时间,若分液漏斗中的液面不下降,则气密性良好,否则气密性不好
【解题思路】
(1)构建捂热法模型
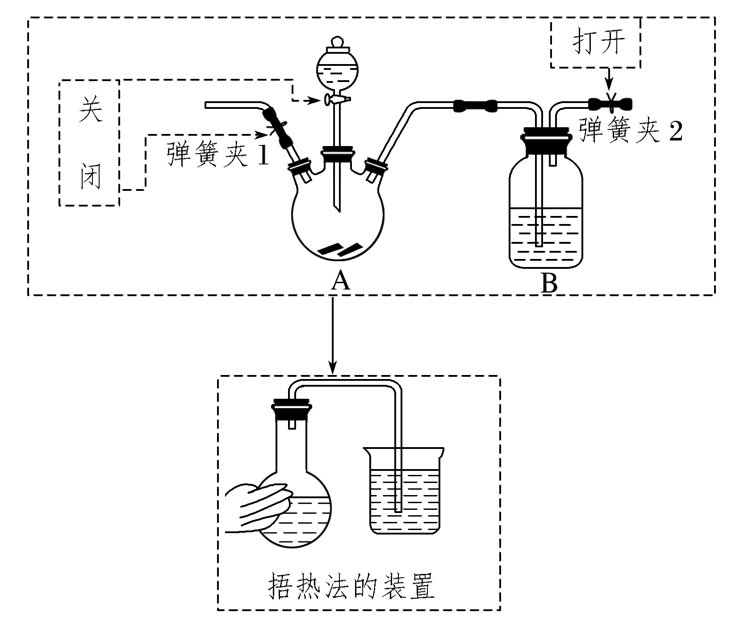
(2)构建液差法模型
三、防倒吸,平衡气压
1.常见的防倒吸装置
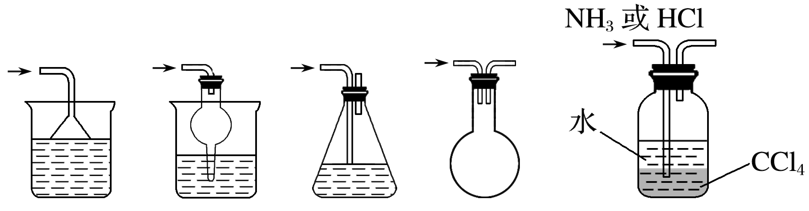
2.常见平衡气压的措施
图中橡皮管A、支管B、玻璃管C都有平衡气压的作用。
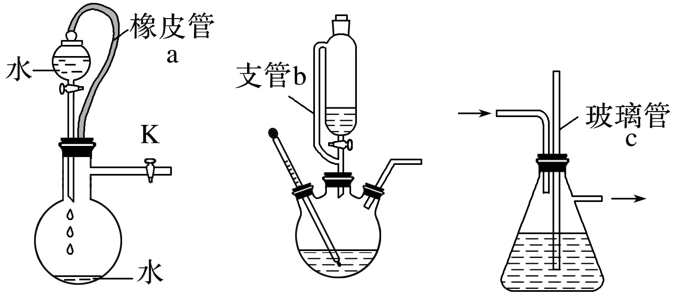
针对练习:
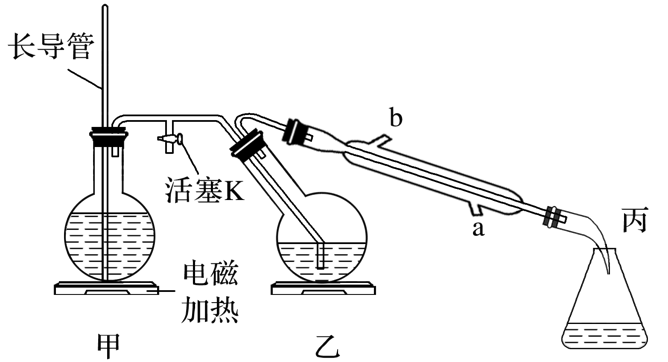
1.工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥发性成分。某兴趣小组用该装置提取柠檬烯的实验操作步骤如下:
(1)将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30 mL 水。
(2)打开活塞K,加热水蒸气发生器甲至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。长导管的作用__________________。
答案:长导管作安全管,平衡气压,防止由于导管堵塞引起爆炸
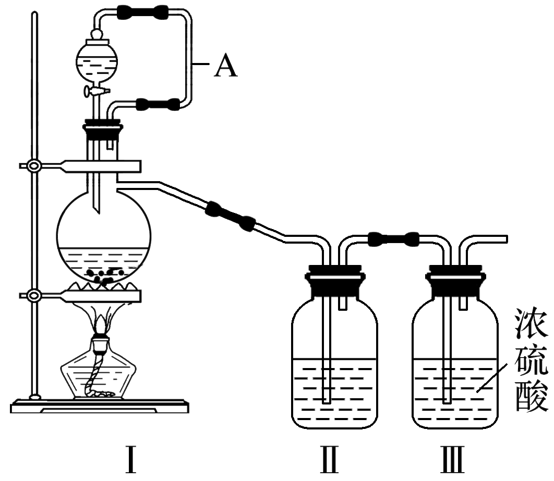
2.某综合实验装置中,A的作用:_______________。
答案:平衡气压,便于液体滴下
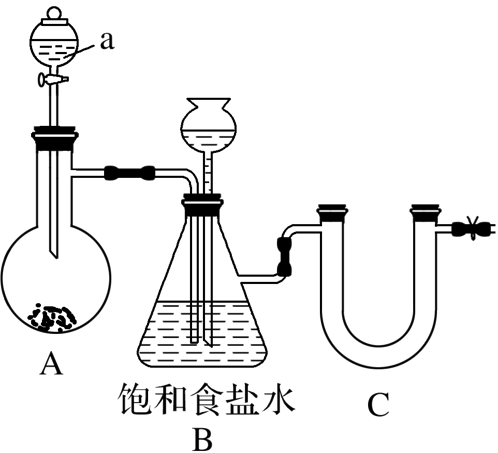
3.下图为制取氯气并探究其性质的实验装置,装置B中的饱和食盐水能够除去Cl2中的HCl,此外还有________作用。
答案:安全瓶
四、压送液体
根据装置的密封性,让反应生成气体或消耗气体,产生压强差,将液体压入或倒流入另一反应容器。
基本模型:氢氧化亚铁的制备
稀H2SO4、铁屑 NaOH溶液
针对练习:
1.凯氏定氮法的实验装置如图,清洗仪器的操作如下:g中加蒸馏水;打开K1,关闭K2、K3,加热b,蒸气充满管路;停止加热,关闭K1,g中蒸馏水倒吸进入c,原因是_______________;打开K2放掉水,重复操作2~3次。
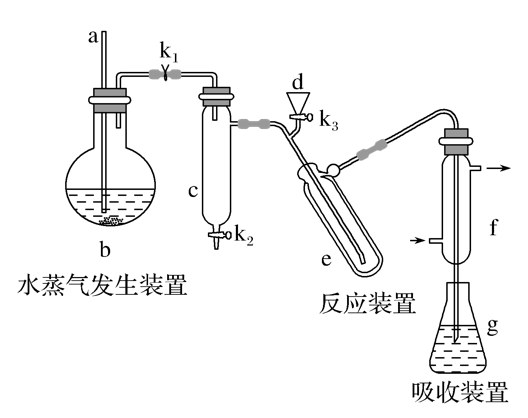
答案:温度降低,装置内气体压强减小,在大气压作用下,g中蒸馏水倒吸入C中
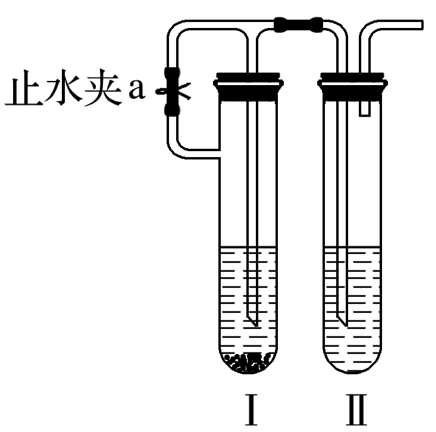
2.(操作顺序)某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁屑、稀硫酸、氢氧化钠溶液。
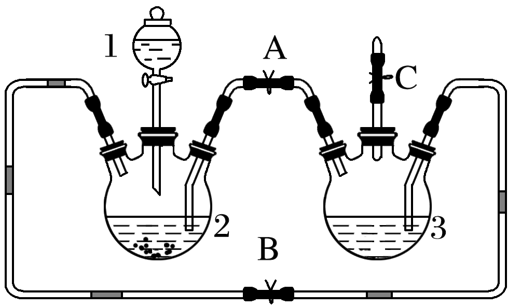
(1)实验开始时稀硫酸应放在__________________中(填写仪器的序号“1”“2”或“3”)。
(2)本实验开始后,首先应排尽装置中的空气,其操作是_______________。
(3)反应一段时间后,可通过控制A、B、C三个开关,将仪器2中的溶液自动转移至仪器3中,操作是______________。
(4)实验时为防止仪器2中铁屑通过导管进入仪器3中,可采取的措施是___________________。
答案:
(1)1
(2)关闭弹簧夹A,打开弹簧夹B和C,旋开分液漏斗的活塞并滴加适量稀硫酸
(3)当仪器中的空气排尽后,关闭弹簧夹B,打开弹簧夹A(或A、C),继续滴加稀硫酸,三颈烧瓶2内的FeSO4溶液进入三颈烧瓶3中
五、喷泉实验
知识点溯源: 氨气“喷泉实验”来自苏教版必修1氨气的性质(第98页“观察与思考”装置图如图1所示)
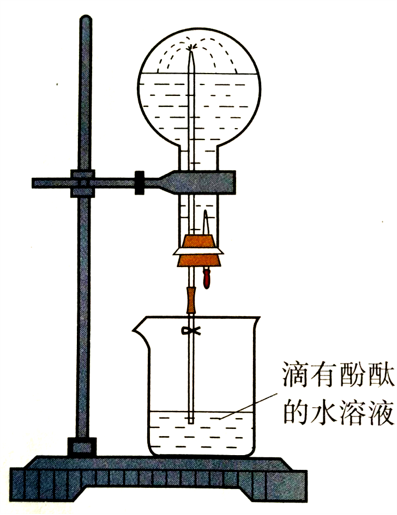
核心观念:形成喷泉的根本原因是气压差。
变式喷泉:
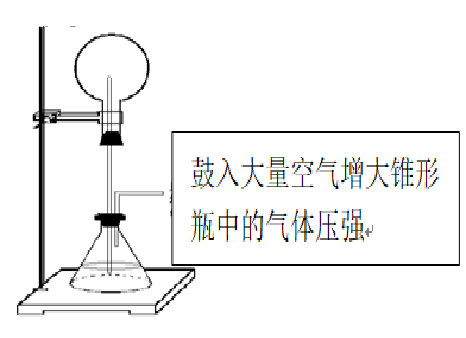
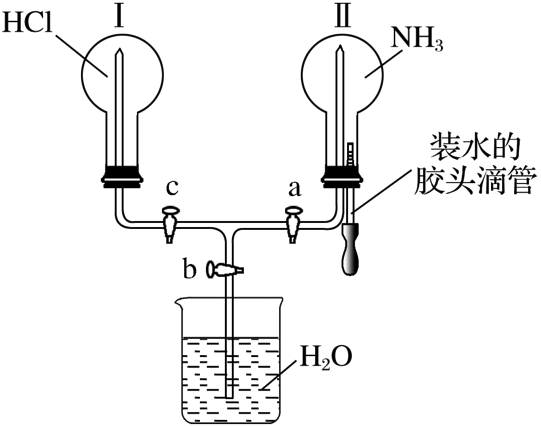
针对练习:
氨气的喷泉实验是中学化学中的重要实验之一。
(1)某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。
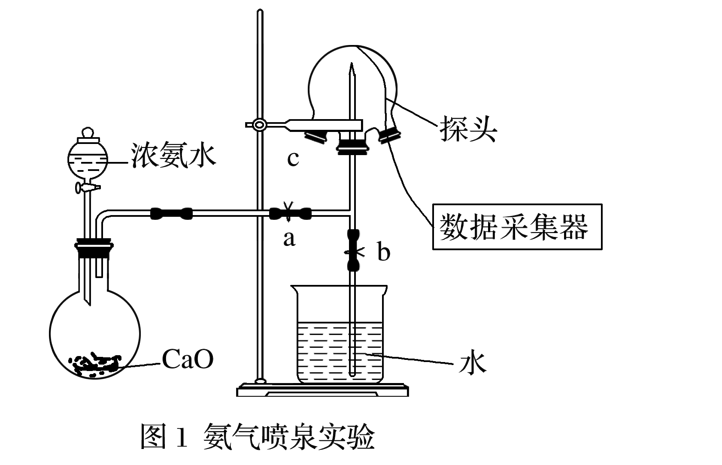
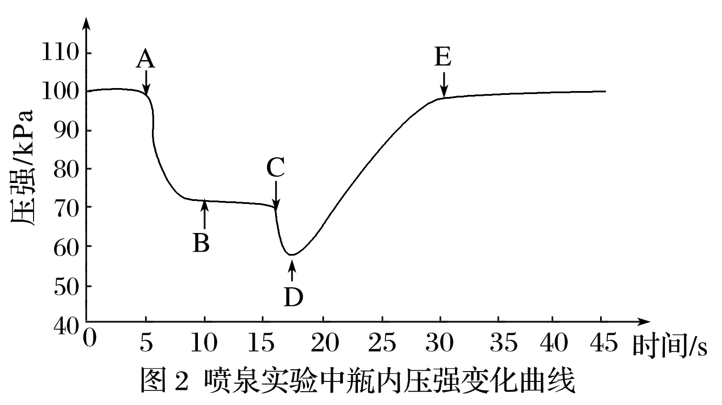
②关闭A,将带有装满水的胶头滴管的橡皮塞塞紧c口,_________,引发喷泉实验,电脑绘制三颈烧瓶内气压变化曲线如图2所示。图2中____点时喷泉最剧烈。
(2)如果只提供图3的装置,请说明引发喷泉的方法_____________
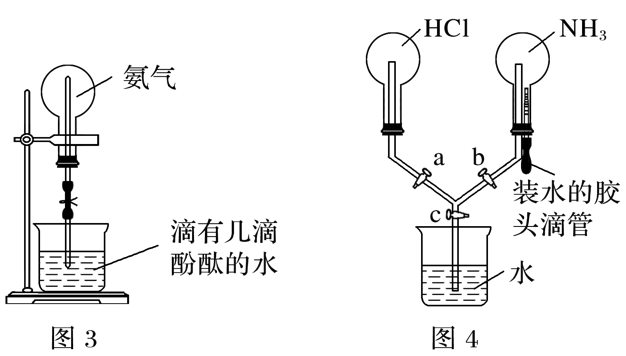
(3)某学生积极思考喷泉原理的应用,设计了如图4所示的装置。
①如果关闭活塞C,打开活塞A、B,再挤压胶头滴管。则可能出现的现象为_______________。
②在①操作的基础上,若要在该装置中产生双喷现象,其操作方法是___________。
答案:
(1)将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明NH3已集满;打开b,挤压胶头滴管使水进入烧瓶;D
(2)打开止水夹,用手或热毛巾将烧瓶捂热,氨气受热膨胀赶走玻璃导管中的空气使氨气与水接触。
(3)HCl气体进入到盛有NH3的集气瓶,产生大量的白烟;打开活塞c
六、减压过滤(抽滤)
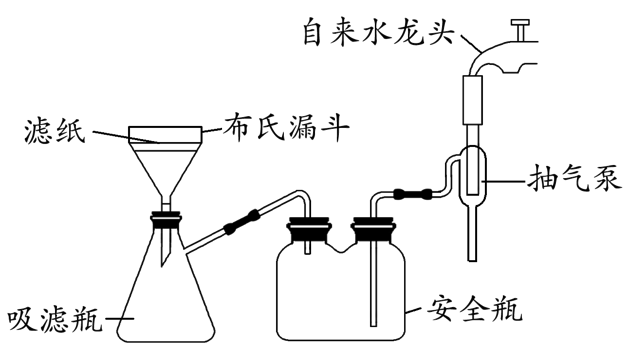
知识点溯源:“减压过滤”来自苏教版选修6《实验化学》硝酸钾晶体的制备,第14页“操作向导”。装置示意图如图所示。
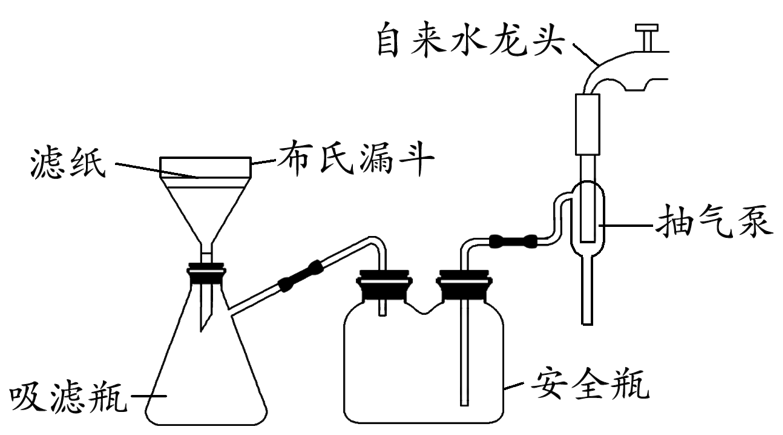
核心观念: 通过制造气压差(产生负压)加快过滤速率,得到更干燥固体。
针对练习:
工业废铁屑表面常有铁锈(成分为Fe2O3),并沾有油污。某校研究性学习小组设计实验方案,按以下①~④步骤用废铁屑制备绿矾(FeSO4·7H2O)晶体。

根据该实验方案,回答下列问题:
(1) 步骤②中烧杯底部留有少量铁屑的理由是___________。
(2) 步骤③过滤装置如下图所示,采用这种装置过滤的主要优点是:______________这种装置工作的主要原理是:________。
(3)在步骤③中,该小组采用如图抽气过滤(减压过滤)装置代替普通漏斗,其目的是______________。
答案:
(1)防止Fe2+被氧化为Fe3+ 2Fe3++Fe==3Fe2+
(2)过滤速度较快;可以得到比较干燥的固体;当自来水龙头打开时,把装置内部的气体随水流带走,导致装置内部的压强降低,使过滤的速度加快
(3)使吸滤瓶内的压强减小,提高过滤的速率;减少滤液与空气的接触,避免Fe2+被氧化
七、减压蒸馏
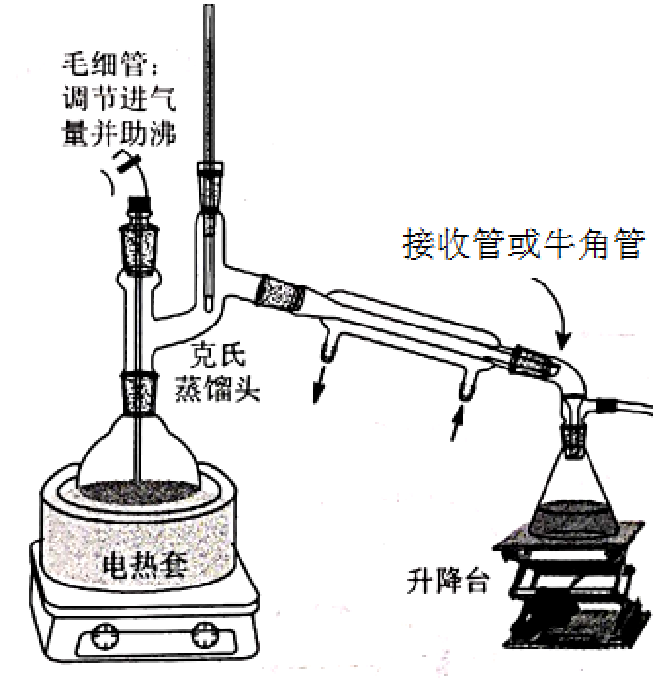
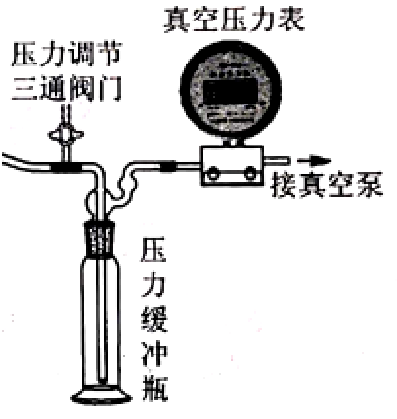
核心观念:通过减压蒸馏可以加快蒸馏速率,防止蒸馏物的分解或氧化。
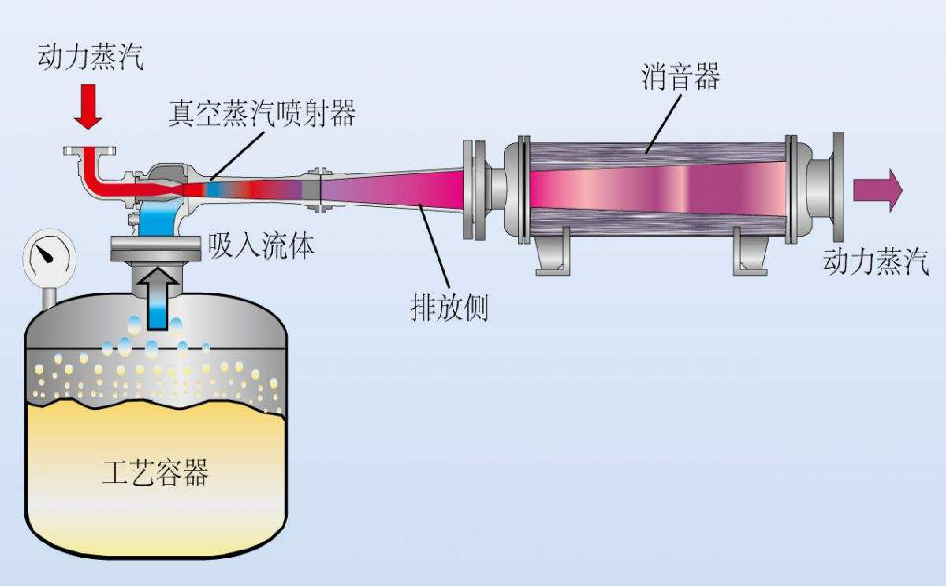
八、减压蒸发也称为减压浓缩或真空蒸发。
操作原理:在密闭的容器内,抽真空使液体处于一个大气压下的环境,从而降低水的沸腾温度,以此进行蒸发浓缩。
核心观念:通过减压蒸发可以加快蒸发速率,防止蒸发物的分解或氧化。
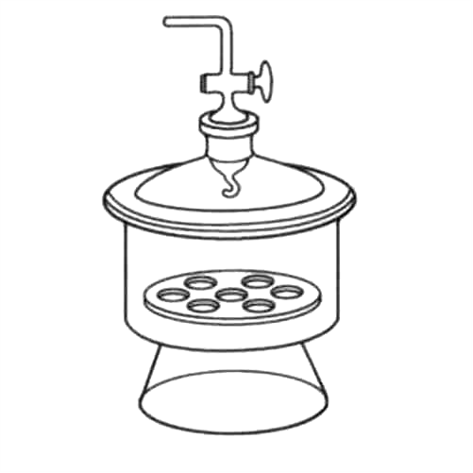
九、减压干燥也叫真空干燥
操作原理:减压干燥的干燥原理是湿物料表面处水分气化的结果,使湿物料内部与表面之间产生水分浓度差,从而使物体干燥。
核心观念:通过减小干燥器中的压强加快干燥速率,防止固体被氧化。

- 全部评论(0)
