中学化学实验常见气体干燥剂的选择和使用
时间:2010-07-13 11:31 来源:未知 作者:石峰 点击: 次 所属专题: 干燥剂 常见气体 气体干燥
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
气体的干燥是气体净化中重要的步骤,掌握中学常见的气体干燥剂、干燥装置、干燥剂选择原则,十分重要,为了便于同学复习和应用,现总结如下。
一、 干燥装置的基本类型和气体流动方向:
|
盛装干燥剂状态 |
液体干燥剂 |
固体干燥剂 |
|
装置示意图 |
洗气瓶 |
球形干燥管 |
|
气体流动方向 |
长管进气,短管出气 |
U形干燥管,进气和出气没有区别; 球形干燥管应该大口进气,小口出气(在干燥管的进出气口都要塞一团棉花,防止干燥剂流动) |
注意:
1、固体干燥剂颗粒大小要适当,颗粒太大气体和干燥剂接触面小,不利于干燥效果不好;颗粒太小,气体不易通过,容易堵塞,一般以黄豆粒大小为宜。
2、液体干燥剂用量要适当,并控制好通入气体的速度,为了防止发生倒吸,在洗气瓶与反应容器之间应连接安全瓶。
二、气体的分类
1、根据酸碱性,
酸性气体:CO2、SO2、NO2、HCl、Cl2、H2S、HBr、HI等
碱性气体:只有NH3
中性气体:H2、O2、CH4、CO、CH2=CH2、C2H2、N2等
2、根据常温氧化还原性强弱,
强还原性气体:H2S、HBr、HI、SO2等
一般性气体:H2、O2、CH4等
三、气体干燥剂的类型及选择
1、常用气体干燥剂按酸碱性可分为三类:
①酸性干燥剂,如浓硫酸、五氧化二磷、硅胶。酸性干燥剂能够干燥酸性或中性的气体,如CO2、SO2、NO2、HCl、H2、Cl2 、O2、CH4等气体。
②碱性干燥剂,如生石灰、碱石灰、固体NaOH。碱性干燥剂可以用来干燥碱性或中性的气体,如NH3、H2、O2、CH4等气体。
③中性干燥剂,如无水氯化钙、无水硫酸铜等,可以干燥中性、酸性、碱性气体,如O2、H2、CH4等。
2、根据干燥剂的氧化性分两类
①强氧化性干燥剂:浓硫酸
②一般干燥剂:五氧化二磷、硅胶、生石灰、碱石灰、固体NaOH、CaCl2、CuSO4等
3、干燥剂选择的基本原则:根据干燥剂和气体的性质选择,其基本原则是干燥剂只吸收气体中的水分,不吸收被干燥的气体,具体表现在:
(1)在选用干燥剂时,显碱性的气体不能选用酸性干燥剂,如不能用碱石灰、CaO和NaOH干燥CO2、SO2、HCl、H2S、Cl2 、NO2等;
(2)显酸性的气体不能选用碱性干燥剂,如不能用P2O5、浓 H2SO4干燥 NH3;
(3)还原性的气体不能选用有强氧化性的干燥剂,如不能用浓 H2SO4干燥 H2S、HBr、HI等;虽然H2、SO2、CO、CH4也有还原性,但是浓硫酸在常温下不能氧化它们,可以用浓硫酸干燥。
(4)能与气体反应的物质不能选作干燥剂,如不能用无水氯化钙干燥NH3(因生成 CaCl2·8NH3)。浓硫酸可以和烯、炔、NO2发生反应,浓硫酸不能干燥烯烃、炔烃和NO2。
四、气体净化中干燥装置的位置顺序
气体的干燥是气体净化的环节之一,在干燥装置和其它净化或反应装置连接时注意:一般情况下,若采用溶液作除杂试剂,则是先除杂后干燥;若采用加热除去杂质,则是先干燥后加热。为了防止大气中的水气侵入,有特殊干燥要求的开口反应装置可加干燥管,进行空气的干燥。

- 全部评论(0)

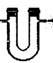 U形干燥管
U形干燥管 