硫酸的工业制法
时间:2023-01-06 11:29 来源:未知 作者:化学自习室 点击: 次 所属专题: 硫酸工业
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
工业制取硫酸分为三个阶段:
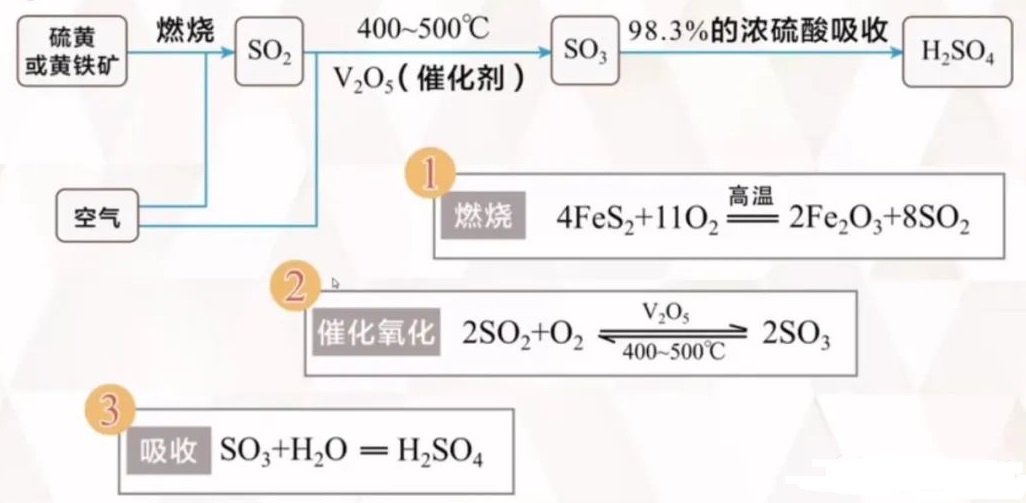
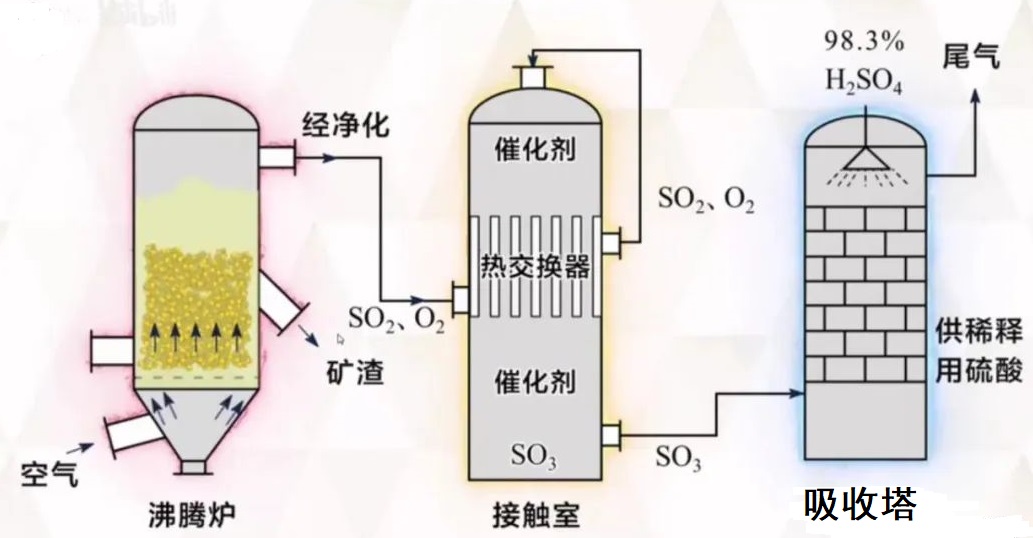
第一阶段:含硫矿物燃烧产生SO2
原料与设备:硫磺或黄铁矿(FeS2);沸腾炉
反应特点:设备提供高温条件引发反应,矿粉中的硫元素与空气中的氧气反应产生SO2,由于该反应放热,反应一旦被引发,不需要再额外提供热量维持反应的进行;
将含硫矿物充分粉碎,预热后从上口投入沸腾炉,热空气以一定流速从设备底部通入,将矿粉吹起翻腾,使空气与矿粉充分接触,以提高反应速率以及原料转化率。
第二阶段:SO2催化氧化产生SO3
原料与设备:第一阶段产生的SO2并投入催化剂V2O5;接触室
反应特点:该反应为可逆反应且正向放热,反应较慢且转化率低;
通过热交换将反应放出的热量带出,一方面降低温度使平衡正向移动提高原料的转化率,另一方面这部分热量对通入的原料气体进行预热提高反应速率,因此该设备也不需要额外提供热量
第三阶段:吸收SO3生成硫酸
原料与设备:第二阶段产生的SO3并投入浓硫酸;吸收塔
反应特点:非氧化还原反应,反应放热;
由于SO3与水反应生成硫酸明显放热,若用水吸收会产生酸雾腐蚀设备,浓硫酸沸点高且难挥发,因此使用浓硫酸吸收SO3生成发烟硫酸。SO3气体从下口通入,浓硫酸从上口喷淋,通过对流使SO3气体被充分吸收
该工业流程的思考
工业制硫酸的各阶段反应均为放热反应,反应一旦引发,反应放出的热量可以维持反应持续进行,减少了热量的消耗;
向设备中投入原料时气体从下口通入,另一原料从上口投入,通过对流使反应更快更充分;
生产过程中会产生酸性气体SO2或SO3,需要用碱液吸收尾气以免气体泄漏引起环境污染。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
