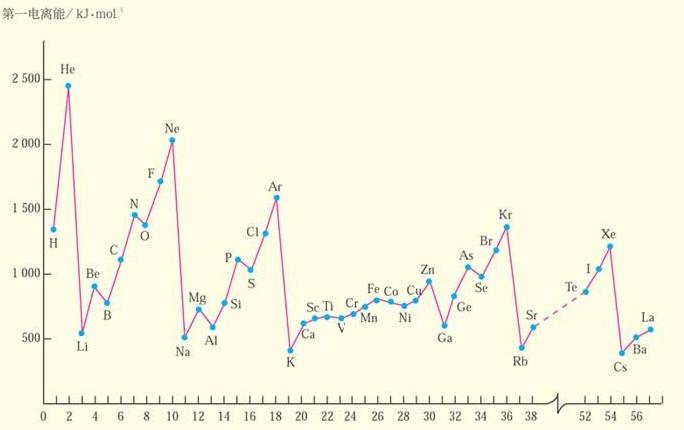
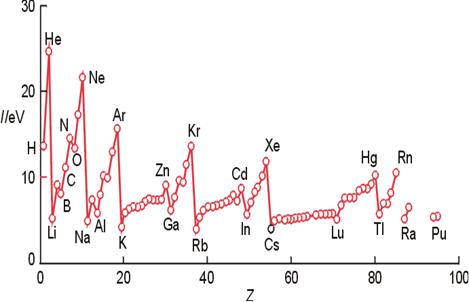
元素第一电离能的变化规律
时间:2013-04-09 08:17 来源:未知 作者:康建峰 点击:次 所属专题: 电离能
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
气态原子要失去电子变为气态阳离子,必须克服核电荷对电子的引力而消耗能量,这种能量称为电离能(I),其单位采用kJ·mol-1。
从基态(能量最低的状态)的中性气态原子失去一个电子形成气态阳离子所需要的能量,称为原子第一电离能(I1);由氧化数为+1的气态阳离子再失去一个电子形成氧化数为+2的气态阳离子所需要的能量,称为原子的第二电离能(I2);其余依次类推。
显然,元素原子的电离能越小,原子就越易失去电子;反之,元素原子的电离能越大,原子越难失去电子。这样,我们就可以根据原子的电离能来衡量原子失去电子的难易程度。一般情况下,只要应用第一电离能数据即可。
元素原子的电离能,可以通过实验测出。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
(3330524811) 评论 元素第一电离能的变化规律:hhhhhhhhhhhhhhc
(343253004) 评论 元素第一电离能的变化规律:hhhhhhhhhhhcc
(343253004) 评论 元素第一电离能的变化规律:hhhhhhhhhhhc
还没有评论,快来抢沙发吧!
