sp3杂化轨道
时间:2013-04-13 18:51 来源:未知 作者:刘洪林 点击: 次 所属专题: 杂化轨道类型
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
同一原子内由一个ns轨道和三个np轨道发生的杂化,称为sp3杂化,杂化后组成的轨道称为sp3杂化轨道。sp3杂化可以而且只能得到四个sp3杂化轨道。
CH4分子的结构经实验测知为正四面体结构,四个C-H键均等同,键角为109°28′,杂化轨道理论认为,激发态C原子(2s12p3)的2s轨道与三个2p轨道可以发生sp3杂化,从而形成四个能量等同的sp3杂化轨道:

其中每一个sp3杂化轨道都含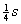 轨道和
轨道和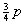 轨道的成分。sp3杂化轨道的形状也和sp杂化轨道类似。成键时,以杂化轨道大的一头与H原子的成键轨道重叠而形成四个σ键。根据理论推算,键角为109°28′,表明CH4分子为正四面体结构。
轨道的成分。sp3杂化轨道的形状也和sp杂化轨道类似。成键时,以杂化轨道大的一头与H原子的成键轨道重叠而形成四个σ键。根据理论推算,键角为109°28′,表明CH4分子为正四面体结构。
除CH4分子外,CCl4、CF4、SiH4、SiCl4等分子也是采取sp3杂化的方式成键的。
CH4分子的结构经实验测知为正四面体结构,四个C-H键均等同,键角为109°28′,杂化轨道理论认为,激发态C原子(2s12p3)的2s轨道与三个2p轨道可以发生sp3杂化,从而形成四个能量等同的sp3杂化轨道:

其中每一个sp3杂化轨道都含
除CH4分子外,CCl4、CF4、SiH4、SiCl4等分子也是采取sp3杂化的方式成键的。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
