常见的有机反应条件归类
时间:2013-11-14 17:04 来源:未知 作者:舒龙昌 点击: 次 所属专题: 有机反应条件
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一.与卤素相关的反应条件
1.“![]() ”为烷烃或烷烃基(如苯环侧链)上氢原子的取代反应,并发生连锁反应,可生成一氯代物或多氯代物。
”为烷烃或烷烃基(如苯环侧链)上氢原子的取代反应,并发生连锁反应,可生成一氯代物或多氯代物。
2.“![]() ”为苯环上氢原子的取代反应。如:
”为苯环上氢原子的取代反应。如:
![]()
3.“![]() 溶液褪色”为碳碳双键或碳碳三键发生加成反应;醛基发生氧化反应。
溶液褪色”为碳碳双键或碳碳三键发生加成反应;醛基发生氧化反应。
4.“![]() 溴水褪色或变浅,且产生白色沉淀”为含酚羟基的物质发生苯环上氢原子的取代反应。取代的位置是酚羟基的两个邻位和一个对位,若这些位置有其它基团占据,则相应位置不能发生取代反应。如右图所示的1 mol白藜芦醇只能与6 mol的Br2发生反应。
溴水褪色或变浅,且产生白色沉淀”为含酚羟基的物质发生苯环上氢原子的取代反应。取代的位置是酚羟基的两个邻位和一个对位,若这些位置有其它基团占据,则相应位置不能发生取代反应。如右图所示的1 mol白藜芦醇只能与6 mol的Br2发生反应。
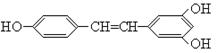
5.“![]() 遇碘水变蓝色”为淀粉溶液遇I2变蓝色。
遇碘水变蓝色”为淀粉溶液遇I2变蓝色。
6.“![]() 溶液变紫色”为含酚羟基的物质遇FeCl3(实为Fe3+)溶液变紫色。
溶液变紫色”为含酚羟基的物质遇FeCl3(实为Fe3+)溶液变紫色。
二.与酸(如H2SO4)相关的反应条件
1.“![]() ”为含醇羟基的物质发生消去反应(分子内脱水),消去的是羟基和β碳原子上的氢原子,生成碳碳双键或碳碳三键和水分子。没有β碳原子或β碳原子上没有氢原子,则不能发生该反应,如CH3OH和(CH3)3CH2OH都不发生消去反应。
”为含醇羟基的物质发生消去反应(分子内脱水),消去的是羟基和β碳原子上的氢原子,生成碳碳双键或碳碳三键和水分子。没有β碳原子或β碳原子上没有氢原子,则不能发生该反应,如CH3OH和(CH3)3CH2OH都不发生消去反应。
若醇不对称,可生成两种或三种烯烃,如3-甲基-3-己醇可生成如下三种烯烃。
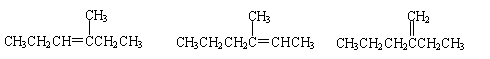
二元醇还可以生成二烯烃或炔烃。
2.“![]() ”为含醇羟基的物质发生分子间脱水(取代反应),生成“—O—”(醚)。
”为含醇羟基的物质发生分子间脱水(取代反应),生成“—O—”(醚)。
3.“![]() ”为苯环上的磺化反应和含醇羟基的物质跟含羧基的物质发生的酯化[可用(CH3CO)2O(乙酸酐)代替浓硫酸]反应以及纤维素(用90%浓硫酸)的水解反应。其中酯化反应的过程一般是羧基中的羟基与醇羟基上的氢原子结合成水,余下部分结合成酯。
”为苯环上的磺化反应和含醇羟基的物质跟含羧基的物质发生的酯化[可用(CH3CO)2O(乙酸酐)代替浓硫酸]反应以及纤维素(用90%浓硫酸)的水解反应。其中酯化反应的过程一般是羧基中的羟基与醇羟基上的氢原子结合成水,余下部分结合成酯。
4.“![]() ”为苯环上的硝化反应。
”为苯环上的硝化反应。
5.“![]() 变黄色”为蛋白质的颜色反应。
变黄色”为蛋白质的颜色反应。
6.“![]() ”为酯(包括油脂)水解生成醇和羧酸;羧酸盐转化为羧酸;酚钠转化为酚;-NH2(含氨基的物质,如氨基酸、蛋白质)+H+→-NH3+;淀粉水解生成麦芽糖、葡萄糖;蔗糖和麦芽糖水解以及蛋白质的水解反应等。
”为酯(包括油脂)水解生成醇和羧酸;羧酸盐转化为羧酸;酚钠转化为酚;-NH2(含氨基的物质,如氨基酸、蛋白质)+H+→-NH3+;淀粉水解生成麦芽糖、葡萄糖;蔗糖和麦芽糖水解以及蛋白质的水解反应等。
7.“![]() 溶液变浑浊”为酚钠溶液中通入CO2气体,生成相应的酚。
溶液变浑浊”为酚钠溶液中通入CO2气体,生成相应的酚。
三.与碱(如NaOH)相关的反应条件
1.“![]() ”为酯(包括油脂)水解生成醇和羧酸盐(此时油脂的反应为皂化反应),若是酚对应的酯,水解后的酚还要跟NaOH反应。
”为酯(包括油脂)水解生成醇和羧酸盐(此时油脂的反应为皂化反应),若是酚对应的酯,水解后的酚还要跟NaOH反应。
2.“![]() ” 为卤代烃水解生成醇(可加热);酚、羧基跟NaOH溶液的中和反应。如除去苯中的苯酚,可向其中加入足量的NaOH溶液,再分液。
” 为卤代烃水解生成醇(可加热);酚、羧基跟NaOH溶液的中和反应。如除去苯中的苯酚,可向其中加入足量的NaOH溶液,再分液。
3.“![]() ”为卤代烃的消去反应,消去卤原子和β碳原子上的氢原子,没有β碳原子或β碳原子上没有氢原子,不能发生该反应。不对称卤代烃可生成两种或三种烯烃,二卤代烃还可能生成二烯烃或炔烃。
”为卤代烃的消去反应,消去卤原子和β碳原子上的氢原子,没有β碳原子或β碳原子上没有氢原子,不能发生该反应。不对称卤代烃可生成两种或三种烯烃,二卤代烃还可能生成二烯烃或炔烃。
4.“![]() 沉淀溶解”为羧酸与Cu(OH)2的中和反应,如苯磺酸、苯甲酸、甲酸、乙酸等。可用新制的碱性Cu(OH)2悬浊液鉴别HCHO、HCOOH和CH3COOH。
沉淀溶解”为羧酸与Cu(OH)2的中和反应,如苯磺酸、苯甲酸、甲酸、乙酸等。可用新制的碱性Cu(OH)2悬浊液鉴别HCHO、HCOOH和CH3COOH。
四.氧化、还原反应条件
1.“![]() 溶液褪色”为碳碳双键、碳碳三键、-CHO、苯环侧链(α碳原子上有氢原子)被氧化。
溶液褪色”为碳碳双键、碳碳三键、-CHO、苯环侧链(α碳原子上有氢原子)被氧化。
2.“![]() ”为含醇羟基的物质发生氧化反应,羟基上的氢原子和α碳原子上的氢原子跟氧化剂提供的氧原子结合生成水,伯醇氧化生成醛,仲醇氧化生成酮,叔醇不能被氧化。
”为含醇羟基的物质发生氧化反应,羟基上的氢原子和α碳原子上的氢原子跟氧化剂提供的氧原子结合生成水,伯醇氧化生成醛,仲醇氧化生成酮,叔醇不能被氧化。
3.“![]() ”表示氧化反应,被氧化的物质有为烯、炔、醇、酚、醛以及苯环侧链(α碳上有氢原子),其中伯醇可直接氧化为羧酸。
”表示氧化反应,被氧化的物质有为烯、炔、醇、酚、醛以及苯环侧链(α碳上有氢原子),其中伯醇可直接氧化为羧酸。
4.“![]() ”为醛基氧化生成羧基或羧酸盐,如醛类物质、甲酸、甲酸盐、甲酸酯以及麦芽糖、葡萄糖等。例:
”为醛基氧化生成羧基或羧酸盐,如醛类物质、甲酸、甲酸盐、甲酸酯以及麦芽糖、葡萄糖等。例:
HCHO+2Ag(NH3)2OH![]() HCOONH4+2Ag↓+3NH3+H2O
HCOONH4+2Ag↓+3NH3+H2O
HCOONH4+2Ag(NH3)2OH![]() NH4OCOONH4(碳酸铵)+2Ag↓+3NH3+H2O
NH4OCOONH4(碳酸铵)+2Ag↓+3NH3+H2O
5.“![]() 火焰明亮并伴有黑烟”为乙烯等含碳量较高的烃的燃烧。
火焰明亮并伴有黑烟”为乙烯等含碳量较高的烃的燃烧。
6.“![]() 火焰明亮并伴有浓烈的黑烟”为乙炔、苯等含碳量高的烃的燃烧。
火焰明亮并伴有浓烈的黑烟”为乙炔、苯等含碳量高的烃的燃烧。
7.“![]() 有烧焦羽毛的气味”为蛋白质如毛、丝等的灼烧。
有烧焦羽毛的气味”为蛋白质如毛、丝等的灼烧。
8.“![]() ”为碳碳双健、碳碳三键、苯环、—CHO、酮(—CO—)等发生加成(还原)反应,但羧基、酯中的羰基一般情况下不发生加成反应。
”为碳碳双健、碳碳三键、苯环、—CHO、酮(—CO—)等发生加成(还原)反应,但羧基、酯中的羰基一般情况下不发生加成反应。
9.“![]() ”为苯环上硝基发生还原反应,生成氨基(—NH2)。
”为苯环上硝基发生还原反应,生成氨基(—NH2)。
五.其它反应条件
1.“![]() 产生气体”,醇羟基、酚羟基、羧基都可以跟钠反应放出H2。
产生气体”,醇羟基、酚羟基、羧基都可以跟钠反应放出H2。
2.“![]() ”,酚羟基跟Na2CO3溶液反应但不放出气体,羧基跟Na2CO3溶液反应可以放出气体(与用量有关)。
”,酚羟基跟Na2CO3溶液反应但不放出气体,羧基跟Na2CO3溶液反应可以放出气体(与用量有关)。
3.“![]() 放出气体”,只有羧基能与NaHCO3溶液反应放出气体。
放出气体”,只有羧基能与NaHCO3溶液反应放出气体。
4.“![]() 有固体物质析出,浮于液面”为皂化反应产物的盐析过程。
有固体物质析出,浮于液面”为皂化反应产物的盐析过程。
5.“![]() 溶液中有固体析出,加水又溶解”为蛋白质溶液的盐析过程。
溶液中有固体析出,加水又溶解”为蛋白质溶液的盐析过程。
6.“![]() 溶液中有固体凝结,加水不可逆”为蛋白质的变性过程。
溶液中有固体凝结,加水不可逆”为蛋白质的变性过程。
7.“![]() ”为C6H12O6(葡萄糖)→2CH3CH2OH+2CO2。
”为C6H12O6(葡萄糖)→2CH3CH2OH+2CO2。
总之,有机物发生什么样的化学反应除由其本身的结构所决定外,还与溶剂(如水、有机溶剂)、反应物的状态(如气态、液态)、溶液的酸碱性、溶液浓度的大小、光、热、压强以及催化剂的不同等直接相关。只要善于归纳整理,灵活运用,就一定能够复习好有机化学。

- 全部评论(0)
