离子交换膜在电化学中的应用
时间:2021-03-26 14:12 来源:未知 作者:张劲辉 点击: 次 所属专题: 离子交换膜
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.离子交换膜的功能
使离子选择性定向迁移(目的是平衡整个溶液的离子浓度或电荷)。
2.离子交换膜在电化学中的作用
(1)防止副反应的发生,避免影响所制取产品的质量;防止引发不安全因素。(如在电解饱和食盐水中,利用阳离子交换膜,防止阳极产生的Cl2进入阴极室与氢氧化钠反应,导致所制产品不纯;防止与阴极产生的H2混合发生爆炸)。
(2)用于物质的制备、分离、提纯等。
3.离子交换膜的类型
根据透过的微粒,离子交换膜可以分为多种,在高考试题中主要出现阳离子交换膜、阴离子交换膜和质子交换膜三种。阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,阴离子交换膜只允许阴离子通过,质子交换膜只允许质子(H+)通过。可见离子交换膜的功能在于选择性地通过某些离子和阻止某些离子来隔离某些物质。
4.离子交换膜类型的判断
根据电解质溶液呈中性的原则,判断膜的类型,判断时首先写出阴、阳两极上的电极反应,依据电极反应式确定该电极附近哪种离子剩余,因该电极附近溶液呈电中性,从而判断出离子移动的方向,进而确定离子交换膜的类型,如电解饱和食盐水时,阴极反应式为2H++2e-=H2↑,则阴极区域破坏水的电离平衡,OH-有剩余,阳极区域的Na+穿过离子交换膜进入阴极室,与OH-结合生成NaOH,故电解食盐水中的离子交换膜是阳离子交换膜。
应用一:隔离某些物质防止发生反应

解析:选B Ⅰ区是阴极室,H+放电生成氢气,同时促进水的电离,生成氢氧化钠,Ⅱ区Na+通过a进入Ⅰ区,故a应该是阳离子交换膜;Ⅲ区和电源的正极相连,为阳极,Cl-放电生成氯气,Ⅱ区Cl-通过b进入Ⅲ区,故b应该是阴离子交换膜;氯气溶于水显酸性,同时次氯酸还具有漂白性,所以滴入甲基橙后溶液先变红后褪色。
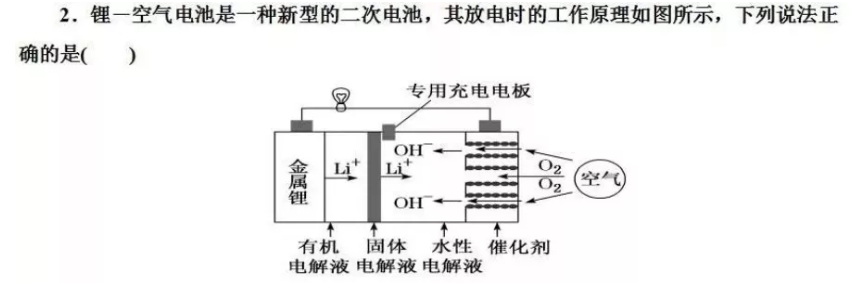
A.正极区产生的LiOH可回收利用
B.电池中的有机电解液可以用稀盐酸代替
C.该电池放电时,正极的反应式为O2+4H++4e-===2H2O
D.该电池充电时,阴极发生氧化反应:Li++e-===Li
解析:选A 金属Li在负极发生氧化反应生成Li+,Li+向正极移动,与正极区生成的OH-结合形成LiOH,从分离出的LiOH中可以回收Li而循环使用,故正极区产生的LiOH可回收利用,A正确;Li能与盐酸反应生成H2,故电池中的有机电解液不能用稀盐酸代替,B错误;该电池放电时,O2在正极得电子发生还原反应生成OH-,电极反应式为O2+2H2O+4e-===4OH-,C错误;该电池充电时,阴极上Li+得电子发生还原反应,电极反应式为Li++e-===Li,D错误。
应用二:物质的制备

解析:选D 由题意知以碘化钾为原料采用电解法制取碘酸钾,就是把-1价碘氧化为+5价碘的过程,所以阳极上的电极反应为
I--6e-+6OH-===IO3-+3H2O,
因此阳极只能用惰性电极而不能用铁作阳极,D正确、A不正确;
阴极上水电离的H+放电生成氢气,电极反应式为2H++2e-===H2↑,理论上每转移2 mol e-,可生成1 mol H2,在标准状况下所占的体积为22.4 L,C不正确;
只有使用阴离子交换膜,才能保证阴极区的碘离子定向移动到阳极区被氧化为碘酸根从而提高原料的转化率,同时阴极区可得到副产品氢氧化钾,所以B不正确。
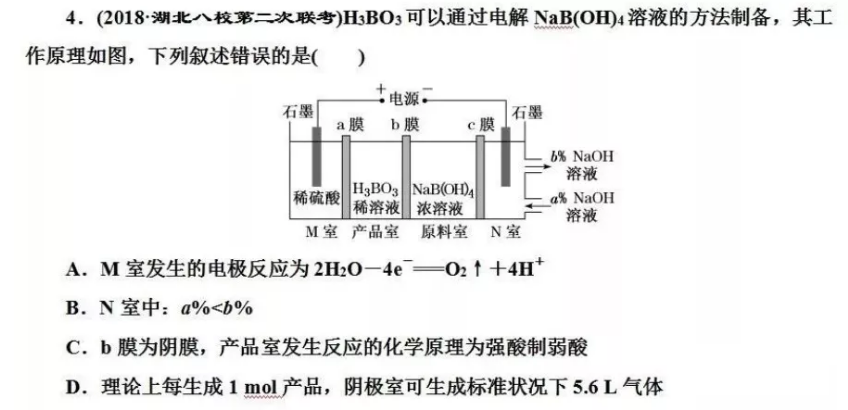
解析:选D M室为阳极室),发生氧化反应,电极反应式为2H2O-4e-===O2↑+4H+,故A正确;N室为阴极室,溶液中水电离的H+得电子发生还原反应生成H2,促进水的电离,溶液中OH-浓度增大,即a%<b%,故B正确;阳极室的H+穿过阳膜扩散至产品室,原料室的B(OH)4-穿过阴膜扩散至产品室,二者反应生成H3BO3,则b膜为阴膜,故C正确;每生成1 mol 产品,转移电子的物质的量为1 mol,阴极室生成0.5 mol 氢气,其标准状况下的体积为11.2 L,故D错误。
应用三:用于物质的分离与提纯

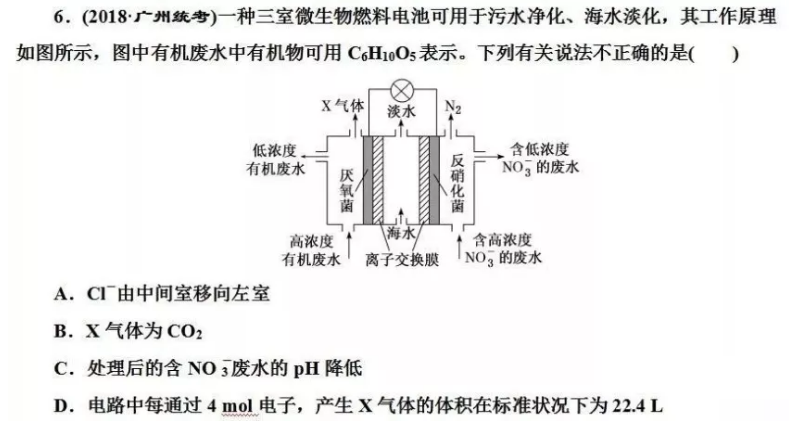
解析:选A 因为阴极是阳离子反应,所以B膜为阳离子交换膜,选项A正确;A极室Cl-在阳极失电子产生氯气,但不产生沉淀,选项B错误;淡化工作完成后,A室Cl-失电子产生氯气,部分溶于水溶液呈酸性,B室H+得电子产生氢气,OH-浓度增大,溶液呈碱性,C室溶液呈中性,pH大小为pHA<pHC<pHB,选项C错误;B极室H+得电子产生氢气,不能使湿润的KI-淀粉试纸变蓝,选项D错误。


- 全部评论(0)
