高考那会儿,盘点师哥师姐们踩过的坑。
时间:2026-05-09 17:16 来源:未知 作者:化学自习室 点击: 次 所属专题: 易错点
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、营养与健康
1、油脂是食物中产生能量最高的营养物质
2、油脂不是高分子化合物,是大分子
3、脚气病是缺乏维生素B1
4、蛋白质的盐析与变性:钾钠铵盐析,铜银铅变性
5、P2O5不可以作食品干燥剂,因为它会产生偏磷酸,偏磷酸有毒。无水硫酸镁可作食品干燥剂
6、用于胃镜的是BaSO4,不是BaCO3
7、苯钾酸和苯甲酸盐都可用于食品防腐(不是增味剂);苯酚可消毒;甲醛有毒(蚁醛)用于杀菌、防腐。三氯乙烷作麻醉剂(2023·全国甲卷)
8、食盐中的碘以碘酸根的形式存在,不是碘单质
9、丝绸、羊毛、蚕丝、锦等、牛胰岛素等的主要成分都是蛋白质
10、纸张、棉絮、棉花等的主要成分都是纤维素(与植物有关的很多都是纤维素)
11、核酸采集棒上的那个棉头是尼龙纤维不是棉花
12、明胶是从动物骨头中提炼出来的胶质,可作食品增稠剂,主要成分是蛋白质
13、铁粉可防止食物变质,但不可防止食物变潮
14、在可乐里加牛奶产生沉淀不是因为钙离子与碳酸根反应,而是牛奶中的胶体遇酸聚沉了。
15、维C具有还原性,可作食品抗氧化剂。(2023·浙江,2023·全国甲卷)
16、纤维素不是营养物质,它可以用来制作酒精,作燃料,不能被人体利用
二、材料
1、传统无机非金属材料:玻璃、水泥、陶瓷
2、AlN、GaN不是合金,是新型非金属材料
3、碳纳米材料、碳纤维的主要成分是碳单质,是新型无机非金属材料,不属于有机高分子材料
4、石墨烯、富勒烯、碳纳米管、C70等均是碳单质
三、资源利用与环境保护
1、绿色化学的核心是从源头治理,不是先污染后治理
2、开发自然资源:减量化,再利用,再循环
3、“双碳”=碳达峰、碳中和
4、促进碳中和最有效的方式之一研发催化剂将二氧化碳转化为甲醇
5、大量燃烧化石材料是造成雾霾的一种因素
6、碳中和生成的二氧化碳小于等于消耗的碳量
7、光化学烟雾的主要成分是氮氧化物和碳氢化合物
8、二氧化硫是空气质量报告指标之一,但H2S不是
9、煤改气、煤改电有利于减少二氧化硫的排放
10、开采可燃冰、燃煤脱硫等措施只对减少酸雨有用,对碳达峰碳中和无效
11、并不是pH<7就是酸雨,pH<5.6才是
12、含磷洗涤剂排入水中,会引起水华
13、水体富营养化的原因:氮肥过度施用
14、芳纶纤维是合成纤维,属于合成高分子材料
15、加聚物不可降解,如:聚乙烯不可降解(加聚反应制得);可用聚乳酸代替(可降解)(缩聚反应制得)
四、物质用途
1、NaOH可以除油污(主要指只能洗去油脂,无法洗去矿石表面所带的矿物油。)
2、肥皂水作蚊虫叮咬处的清洗剂,是化学反应(与蚊子的毒液酸碱中和)
3、适量SO2可给葡萄酒消毒
4、ClO2是安全无毒的第四代消毒剂,可高效杀灭病毒。此外氯气,臭氧也可以用于饮用水消毒
5、含3%过氧化氢的溶液是医院常用的一种消毒剂
6、酒精常用作医用消毒,但不是越浓消毒效果越好
7、浸泡过高锰酸钾的硅土可以作水果的保鲜剂
8、厨房中开水瓶中水垢可用食醋祛除
9、PVC受热分解出含氯的对人体有害的物质,所以不可用于食品塑料
10、含氮量高的硝化物多易燃易爆
11、硝酸铵溶于水吸热,可制成医用速冷袋
12、泡沫灭火器的成分:Al2(SO4)3和NaHCO3,不可用于电器起火
13、石墨做电极利用的是石墨类似金属的性质来导电
14、氨气做制冷剂原理是因为氨气易液化,汽化吸热
15、小苏打NaHCO3、Al(OH)3可治疗胃酸过多,Na2CO3不可以
16、汽车发动机的抗冻剂是乙二醇
五、其他类
1、常见物质俗称:水玻璃:Na2SiO3溶液;大苏打:Na2S2O3;苏打、纯碱:Na2CO3;小苏打:NaHCO3;火碱:NaOH;侯氏制碱法制的“碱”:Na2CO3
2、NH3沸点在-34℃左右,不能用冰水冷凝为液氨
3、NH4NO3易爆,不能制NH3
4、可做原子堆反应剂:Na和K
5、漂白粉是氯化钙和次氯酸钙的混合物
6、84消毒液沾到皮肤需立即用大量水冲洗,并涂抹维生素C
7、胶体能产生丁达尔效应是由于胶体粒子对光线的散射(2023·全国甲卷)
六、结构
1、H的第一电离能大于C
2、结构化学概念辨析
电子空间运动状态——轨道数
电子运动状态——核外电子数
能量种类——能级个数(如1s22s22p6,有3种能量的电子)伸展方向——轨道数
运动范围——电子层数
3、电负性Cl>C>H(可以联想CCl4,CH4)
4、孤电子对排斥力>孤电子与成键电子排斥力>成键电子排斥力
5、O-H键比S-H键电子云重叠程度大,键长更短,键能更大,更稳定
6、过氧化氢分子是“书本结构”,不是平面结构
7、硝基中的氮是sp2杂化
8、壁虎爬墙是范德华力
9、氢键是一种分子间作用力,不是化学键
10、HNO3形成的是分子内氢键
11、冰中1个分子水含2个氢键
12、CH3+是sp2杂化,CH3-是sp3杂化
13、碳碳叁键两端的碳均为sp杂化,直线型,写结构简式时不要写成折线
14、键角:H2O>H2S(分析:中心原子杂化方式相同,电负性O>S)
15、吡啶( )和吡咯(
)和吡咯(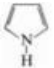 )两个n(原子均为)sp2杂化,均含有大Π键,前者为Π66,后者为Π56
)两个n(原子均为)sp2杂化,均含有大Π键,前者为Π66,后者为Π56
16、配位数不一定等于配体数,如二齿配体、多齿配体、螯合物等,一个配体有多个配位点
17、气态团簇分子的分子式,就是晶胞内的原子数,不能约分。
18、由原子直接构成的共价晶体中没有分子,如SiO2中不含SiO2分子
19、氮化铝是共价晶体
20、共价晶体延展性差,因为共价键具有方向性
21、晶格和晶胞不是同一个概念,晶格可能会出现重复单元
22、结构单元不等于晶胞
23、1cm=107nm=1010pm
24、晶体熔沸点判断方法:
①判断晶体类型:原子晶体>离子晶体>分子晶体(一般)
②原子晶体:半径小、共价键长短,键能大,熔沸点高
离子晶体:阴阳离子电荷越多,离子半径越小,离子键越强,熔沸点越高
分子晶体:氢键→相对分子质量→分子极性(均正相关)
七、有机化学
1、三氯甲烷只有一种结构,不能证明甲烷是正四面体构型,也有可能是正方形
2、乙烯密度与空气密度相似且不溶于水,用排水法收集
3、Ω=1的官能团:碳碳双键、酮羰基、醛基、酯基、硝基等
4、液溴易挥发,也能和硝酸银产生淡黄色沉淀
5、氮在有机物中,若形成三角锥结构类似于(氨气),则该有机物不可能所有原子都共面
6、麦芽糖是还原性糖,可以发生银镜反应
7、有机反应试剂与条件
能与高锰酸钾反应:碳碳双键碳碳三键甲苯苯酚醛基羟基
与溴水反应:碳碳双键(加成)、碳碳三键(加成)、苯酚(取代)、醛基(氧化)
能被氢气加成:碳碳双键碳碳三键苯环酮羰基醛基(强还原剂下羧基也可以)
能与金属钠反应:羟基羧基酚羟基
能与氢氧化钠反应:羧基酚羟基酯基卤代烃
能与碳酸氢钠反应:羧基
能与碳酸钠反应:酚羟基和羧基
8、醛基和液溴、Br2的CCl4溶液均不反应,但可以被溴水氧化
9、醇消去的条件是浓H2SO4、170℃, 卤代烃消去的条件是NaOH/C2H5OH加热。
10、羧基和羟基的缩聚反应,缩聚物同时含羧基和羟基
11、乙二醇和足量酸性高锰酸钾溶液反应会放出二氧化碳,得不到乙二酸
12、一般条件下,羧基、酯基的碳氧双键不加成,酮羰基、醛基的能加成
13、聚乙烯醇不能通过乙烯醇加聚
14、麦芽糖和蔗糖均为二糖,互为同分异构体。纤维素和淀粉,均为多糖,不是同分异构体
15、不是所有的糖类都可以水解,单糖不水解
16、三溴苯酚能溶于苯,不能用浓溴水分离苯和苯酚
17、新制Cu(OH)2(悬浊液)检验下列物质:
乙醇:互溶,无明显现象
乙醛:Δ,生成砖红色沉淀
乙酸:沉淀溶解
乙酸乙酯:分层
丙三醇(甘油):溶解生成绛蓝色溶液(注:多-OH醇的特殊性质)
葡萄糖:先形成绛蓝色沉淀,后Δ,生成砖红色沉淀
18、—CHO的检验:两个必须条件“加热+碱性环境”
A、银镜反应需要“水浴加热”
B、与新制Cu(OH)2悬浊液反应直接在酒精灯上加热即可
C、检验淀粉是否发生水解,因淀粉水解需加入稀硫酸做催化剂,故需先用NaOH溶液将反应液调至碱性,才可加入银氨溶液或新制Cu(OH)2悬浊液进行检验
19、苯酚和浓溴水反应生成的2,4,6-三溴苯酚,难溶于水,但易溶于有机溶剂,所以不生成白色沉淀不代表反应没发生
20、用烧过的铜丝检验羟基时,若只出现Cu丝变红,不能证明有羟基存在,也有可能是羧基溶解了覆盖在Cu丝表面的氧化铜
21、石蜡油分解气含有不饱和烃,但不一定是烯烃
22、石炭酸是苯酚不是羧酸
23、沥青的成分是烃
24、酚醛树脂酸性条件下是线性结构具有热塑性,碱性条件下是网状结构具有热固性
25、裂化汽油中是有双键的,所以不饱和
26、碳的催化重整是将链状烃转化成环状烃,可获得芳香烃
27、高级脂肪酸是电解质;糖类及其水解产物均为非电解质;除可电离出H⁺的有机物酸和酚,大多数有机物为非电解质
28、物理变化:石油分馏 化学变化:煤的干馏、气化、液化,石油的裂化、裂解
八、实验
1、精确度:托盘天平0.1g 量筒0.1mL 滴定管0.01mL
2、量筒没有零刻度线,滴定管零刻度线在上
3、球形冷凝管冷凝面积大,冷凝效果好,用于冷凝回流;直形冷凝管用于蒸馏(注意:球“形”冷凝管别写成“型”了)
4、蒸发结晶时也用得到坩埚钳,用来夹蒸发皿
5、灼烧不能用蒸发皿,应该用坩埚
6、有侧支管的试管叫具支试管,有侧支管的烧瓶叫蒸馏烧瓶,瓶口带有磨口滴管的叫滴瓶(2023·湖北卷)
7、配制一定物质的浓度的溶液,所需容量瓶前加规格
8、启普发生器使用条件:块状固体(不能是粉末)和液体常温下反应,制备气体。
如一轻(H2)二重(CO2)三臭(H2S)
9、冷凝水下进上出(与产物流向相反)(2023·新课标)(2023·湖北卷)
10、抽滤的优点:过滤较快,固体较干燥
11、萃取放气时,分液漏斗下口应倾斜向上
12、收集易升华的物质,导管需要用粗管(牛角管),防止其凝华阻塞
13、测定溶液pH值,pH试纸必须干燥,否则会稀释溶液,导致酸溶液数值偏高,碱溶液数值偏低
14、84消毒液、氯水有漂白性,不能用pH试纸测溶液pH
15、蒸馏时温度计放在支管口,醇的脱水反应温度计插入溶液中(控温)
16、工业制备无水乙醇,工业酒精中加生石灰,蒸馏
17、乙酸和乙醇反应生成乙酸乙酯,因其与乙酸和乙醇互溶,不能用长颈漏斗分离18、冷却结晶:液面出现晶膜时,停止加热蒸发结晶:有大量固体析出时,停止加热
19、CS2洗涤固体硫是因为S易溶于CS2,是物理变化
20、与水相比,乙醇作为萃取剂具有沸点低和易浓缩的优点
21、酯化反应中加入液体的顺序是乙醇→浓硫酸→乙酸,最后加入碎瓷片
22、NH3可用碱石灰干燥,不能用酸性干燥剂(如浓硫酸、P2O5)干燥,也不能用CaCl2干燥(生成CaCl2·8NH3)(2023·广东卷)
23、碱石灰不能干燥CO2,NO2,HCl,SO2、Cl2等
24、浓硫酸不能干燥碱性气体(如NH3),也不能干燥还原性气体(如H2S、HI等)
25、多孔玻璃棒(或球泡)不能防倒吸,可以加大反应物接触面积,使反应充分
26、加入沸石防暴沸的原理:形成分散的气化中心
27、硫酸四氨合铜中加入无水乙醇是为了降低其溶解性,从而使其结晶析出
28、净化实验室制备的Cl2,依次通过盛有饱和NaCl溶液(除HCl)、浓硫酸的洗气瓶(除水蒸气)
29、与MnO2相关:
A、工业流程中体系含有MnO2的时候,想将Fe2+氧化成Fe3+不可用H2O2溶液,因为MnO2会催化H2O2分解
B、工业流程中可用MnO2将Fe2+氧化成Fe3+,不可用H2O2替代MnO2,因为Fe3+会催化H2O2分解(2023·全国乙卷)
30、工业制取KCl时(含有CaCl2、MgSO4等杂质),试剂添加顺序为先加BaCl2溶液,再加K2CO3溶液,顺序不能颠倒(可类比食盐精制)
31、一般实验用的药品不放回原瓶,但Na,K,白磷等除外
32、HF溶液、Na2CO3溶液、Na2SiO3溶液、NaOH溶液均不能用带磨口玻璃塞的玻璃瓶保存;苯、甲苯、乙醚等有机溶剂应用玻璃塞不宜用胶塞
33、保存液溴—磨口玻璃塞、棕色细口瓶、加少量水进行水封,瓶口并用蜡封好
34、CCl4易挥发,见光不分解,且四氯化碳为液体,用细口瓶装
35、KMnO4在加热或光照的条件下会分解,其固体应该保存在棕色广口瓶中
36、见光易分解或变质试剂一般盛于棕色瓶,如HNO3、AgNO3、氯水等置于冷暗处
37、KI、FeSO4等平时保存固体而不保存溶液
38、使用FeSO4或FeCl2溶液时内放少量铁粉或铁钉,防被氧化
39、因吸收CO2或水蒸气而变质的试剂应密封保存(如NaOH、石灰水、漂白粉、水玻璃、Na2O2等),石灰水最好现用现配
40、浓盐酸、氨水、碘及苯、甲苯、乙醚等低沸点有机物均保存在瓶内加塑料盖密封,置于冷暗处。
九、元素化合物
1、SO2、CO2不与CaCl2溶液或BaCl2溶液反应。
2、王水是浓硝酸和浓盐酸的混合物(体积比1:3)
3、硝酸酸酐是N2O5
4、氨气没有碱性,氨水显碱性,所以检验氨气的红色石蕊试纸必须是湿润的
5、鉴别NO2和Br2单质:通过加压的方法,颜色加深的为溴单质,颜色先加深后变浅的为NO2(因为存在平衡2NO2![]() N2O4)
N2O4)
6、碱性氧化物都是金属氧化物,但金属氧化物也有可能是酸性氧化物(如Mn2O7),或者是两性氧化物(如Al2O3)
7、工业炼铝是电解熔融的Al2O3,不能用熔融AlCl3,因其是共价化合物,是分子,熔融状态下不电离
8、直接加热饱和FeCl3溶液无法得到Fe(OH)3胶体(会得到沉淀)
9、含结晶水的晶体风化是化学变化
10、利用反渗透膜从海水中分离出淡水不涉及化学变化
11、工业上常用廉价易得的Ca(OH)2作沉淀剂,如从海水中获得Mg(OH)2
12、汞容易与大部分普通金属形成合金,包括金和银
13、Na2CO3溶解放热,NaHCO3溶解吸热
14、二价铜和少量NH3·H2O生成Cu(OH)2沉淀,NH3·H2O过量则生成[Cu(NH3)4]2+
15、酸性高锰酸钾是用H2SO4酸化的,不可用HCl酸化
16、H3BO3(硼酸)是一元弱酸(原因分析:B(OH)3+H2O [B(OH)4]-+H+)
[B(OH)4]-+H+)
17、制备硫酸时,应使用浓硫酸吸收SO3,而不能用水吸收(接触法制硫酸)
18、有机物碳化体现的是硫酸的脱水性,不是吸水性(2023·广东)(2023·北京)
19、向浓硝酸中插入红热的碳,产生的二氧化氮既可能是浓硝酸与碳反应生成的,也可能是浓硝酸受热分解产生的
补充:此类考点常见于探究类选择题,或“现象、原因、结论”类大表格选择题。在多变量影响实验结果时,一定要记得排除干扰、控制单一变量。
20、铁在氯气中加热产生棕红色(或棕褐色)的烟,铜在氯气中加热生成棕黄色的烟
21、KClO4受热分解,不能蒸发结晶
22、从化合价的角度分析,H2O2中O处于中间,为-1价,所以既有氧化性,也有还原性
23、铝热反应中KClO3的作用为助燃剂
24、金属与HNO3反应不生成H2。浓HNO3一般被还原为NO2,稀HNO3一般被还原为NO。极稀的HNO3与Mg、Al、Fe、Zn等反应时,可被还原成NH4NO3
25、HNO3与金属反应的一般通式:
A、金属+浓HNO3→金属硝酸盐+NO2↑+H2O
B、金属+稀HNO3→金属硝酸盐+NO↑+H2O
参加反应的HNO3=起酸性作用的HNO3+被还原的HNO3
金属与HNO3反应后的溶液中含有NO3-,向其中加酸金属继续被氧化。
26、金属与浓硫酸反应:
A、氢前金属:先生成SO2,随硫酸变稀,后生成H2
B、氢后金属:先加热生成SO2,随硫酸变稀,反应停止
27、不能用稀H2SO4代替稀HCl与CaCO3反应的原因是:会生成微溶的硫酸钙覆盖在碳酸钙表面,将碳酸钙与稀硫酸隔离,阻止反应进一步进行
28、SO42-能与S2-共存,但S2-与SO32-在碱性才共存,酸性条件下发生归中反应,生成S单质
29、与NH4+双水解不共存:SiO32-、[Al(OH)4]-、ClO-
30、[Al(OH)4]-和HCO3-反应是强酸制弱酸:[Al(OH)4]-+HCO3-=Al(OH)3↓+H2O+CO32-
31、Cl2和热的石灰乳反应生成的是ClO3-
32、酸性H2CO3>HClO>HCO3-,所以漂白液漂白原理:NaClO+CO2+H2O=HClO+NaHCO3,产物跟CO2的量无关
33、加入盐酸能产生SO2的溶液,除了可能含有SO32-或HsO3-外,还可能含有S2O32-:S2O32-+2H+=SO2↑+S↓+H2O(2023·广东)
34、检验SO42-之前先用HCl酸化,至无明显现象,再添加BaCl2。不能用HNO3酸化,也不能用Ba(NO3)2溶液(2023·辽宁卷)
35、用KMnO4检验Fe2+是否完全被H2O2氧化为Fe3+之前,一定要将溶液煮沸冷却
36、酸性KMnO4溶液不能用来检验FeCl2中的Fe2+
37、不能用Fe2(SO4)3制备Fe(OH)3胶体,因为硫酸不易挥发
38、钝化不是不反应,而是试剂强氧化性的体现
39、使指示剂先变色后褪色的物质:
A、浓HNO3B、氯水C、Na2O2
40、C和浓H2SO4或者浓HNO3反应均需加热
41、制粗硅生成的气体是一氧化碳: ![]() (2023·辽宁卷)
(2023·辽宁卷)
42、工业上用碳还原二氧化硅制备硅晶体,说明碳的还原性比硅强,但不能说明非金属性强弱
43、不能通过加热氯化铵来制取氨气
44、Na制K原理:Na(l)+KCl(l)=K(g)+NaCl(l),是高沸制低沸
45、KMnO4与草酸反应越来越快的可能原因是反应生成了Mn2+,对反应起催化作用
46、P与N2相比,N2的氧化性更强,但P更活泼(结构的原因)
47、气体除杂:
CO2(SO2/HCl)—饱和NaHCO3溶液(强酸换弱酸)(2023·北京)
CO2(SO2)—酸性高锰酸钾溶液或溴水(SO2的还原性)
SO2(HCl/H2SO4酸雾)—饱和NaHSO3溶液(强酸换弱酸)
十、反应原理
1、Ea越大,反应速率对温度越敏感
2、焓变越大,平衡常数对温度越敏感
3、温度-转化率图像中,最高点不一定是达到平衡,有可能反应时间不够,催化剂越好,越接近平衡
4、使用合适的催化剂可以提升时空转化率(单位时间内的转化率),不可以提升平衡转化率
5、压强变化可能引起物态变化。如水蒸汽液化,于是在温度不变情况下可引起KP改变
6、算分压平衡常数,千万别忘了看看有没有稀有气体(不参与反应的气体)
7、电极材料为活泼金属Li、Na、K等,不能选用水溶液作为导电介质
8、电化学腐蚀和化学腐蚀不一样。例如铁在潮湿的空气中放置,易发生化学腐蚀而生锈这是错的!发生的是电化学腐蚀
9、氯化钠,碳粉,其脱氧原理与钢铁的吸氧腐蚀相同,都是形成原电池
10、电子不能下水,而电流(在某些题目里)可以
11、多元酸分步电离,其第一步电离可能是完全的,后面几步可能是不完全的
12、Kw只有在常温(25℃)下才是10-14
13、CH3COONH4为弱酸弱碱盐,属于强电解质,在溶液中阴阳离子水解程度相差不大,因此溶液pH=7,促进水的电离
14、在分布系数图像中,pH的改变是外加酸碱作用的结果,因此写电荷守恒时千万别忘掉外加的阴、阳离子!
15、H3PO3是二元酸,在分布系数曲线中只有两个交点,不存在PO33-离子,NaHPO3是正盐
十一、其他经验
1、Ⅷ族是副族,但是“过渡金属”,但不标注“B”
2、亚硫酸钙、草酸钙是沉淀
3、苯酚溶于水形成的是乳浊液
4、强氧化剂不一定与强还原剂反应。如:可用浓硫酸干燥SO2
5、乙酸酐( )是两分子乙酸脱去一分子水。注意:不是氧化物
)是两分子乙酸脱去一分子水。注意:不是氧化物
6、絮凝剂有利于生成粒径较大的沉淀,便于分离
7、冰盐水约-18℃
8、颜色反应和焰色反应不一样
9、方程式题中有两个问法大家要注意:沉淀的物质的量最大、沉淀的质量最大

- 全部评论(0)
