等效平衡专题
时间:2016-01-07 20:39 来源: 作者:李文才 点击: 次 所属专题: 等效平衡 专题
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、等效平衡的概念
外界条件相同时,同一可逆反应只要起始浓度相当,无论经过何种途径,都可以达到相同的平衡状态。
概念的理解:
(1)外界条件相同:通常可以是①恒温、恒容(同T同V),②恒温、恒压(同T同P),读题时注意勾画出这些条件。
(2)相同的平衡状态:通常是指平衡混合物各组分的百分含量相同,但各组分的物质的量、浓度可能不同。
(3)平衡状态(终态)只与始态有关,而与途径无关,(如:①无论反应从正反应方向开始,还是从逆反应方向开始②投料是一次还是分成几次③反应容器经过扩大—缩小或缩小—扩大的过程,)只要起始浓度相当,就达到相同的平衡状态。
二、等效平衡的判断及处理
1、步骤
(1) 进行等效转化: 一边倒法,即按照反应方程式的计量数之比转化到同一边的量,与题干所给起始投料情况比较。
(2) 判断起始浓度是否相当。
2、三种类型:
I类:恒温恒容下对于反应前后气体体积发生变化的反应来说(即△n≠0的体系):等效转化后,对应各物质起始投料的物质的量与原平衡起始态相同。
II类:恒温恒容下对于反应前后气体体积没有变化的反应来说(即△n=0的体系):等效转化后,只要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。
III类:恒温恒压下对于气体体系等效转化后,要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。
解题的关键,在读题时分清类别,用相应的方法求解。
例题:
1、 在t℃时,向2L密闭容器中放入1molA和1molB,发生下列反应:A(g)+B(g) C(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是 ( )
C(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是 ( )
A、2molA和1molB
B、2molD和A、B、C各1mol
C、1molC和2molD
D、1molC和1molD
2、在等温等容条件下,有下列气体反应:2A(气)+2B(气) C(气)+3D(气)。现分别从两条途径建立平衡 Ⅰ:A、B的起始浓度均为2mol/L。 Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L。
C(气)+3D(气)。现分别从两条途径建立平衡 Ⅰ:A、B的起始浓度均为2mol/L。 Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L。
下列叙述正确的是:( )
A、Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成相同
B、Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成不同
C、达到平衡时Ⅰ途径的VA等于Ⅱ途径的VA
D、达到平衡后,第Ⅰ途径混合气密度为第Ⅱ途径混合气密度的1/2
3、在一个1L的密闭容器中,加入2molA和1molB ,发生下述反应:2A(g)+B(g)  3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。
3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。
(1)维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L的 ( )
A、3mol C+1mol D
B、1mol A+0.5mol B+1.5mol C+0.5mol D
C、1mol A+0.5mol B+1.5mol C
D、4mol A+2mol B
(2)维持容器的压强和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L(或C的体积分数仍是a%)的是 ( )
A、3mol C+1mol D
B、1mol A+0.5mol B+1.5mol C+0.5mol D
C、1mol A+0.5mol B+1.5mol C
D、4mol A+2mol B
练习:
1、在1L密闭容器中通入2mol氨气,在一定温度下,发生下列反应:2NH3 N2+3H2,达到平衡时,容器内N2的百分含量为a%,若维持容器的体积和温度都不变,分别通入下列几组物质,达到平衡时,容器内N2的含量仍为a%的是 ( )
N2+3H2,达到平衡时,容器内N2的百分含量为a%,若维持容器的体积和温度都不变,分别通入下列几组物质,达到平衡时,容器内N2的含量仍为a%的是 ( )
A、3molH2和1molN2 B、2molNH3和1molN2 C、2molN2和3molH2 D、0.1molNH3,0.95molN2和2.85molH2
2、 在一定条件下,将3molN2和3molH2充入一个容积固定的密闭容器中,发生反应:N2(g)+3H2(g) 2NH3(g),当反应达到平衡时NH3为n mol。在与上述完全相同的容器中,保持温度不变,若平衡时NH3仍为n mol,则下列组合中不正确的是 ( )
2NH3(g),当反应达到平衡时NH3为n mol。在与上述完全相同的容器中,保持温度不变,若平衡时NH3仍为n mol,则下列组合中不正确的是 ( )
选项 | 起始状态/mol | ||
N2 | H2 | NH3 | |
A | 2 | 0 | 2 |
B | 2.5 | 1.5 | 1 |
C | 8/3 | 2 | 2/3 |
D | 0 | 0 | 2 |
3、在一个容积固定的密闭容器中充入1molHI,建立如下平衡:H2(g)+I2 (g) 2HI(g),测得HI的转化率为a%。其他条件不变,在上述平衡体系中再充入1molHI,待平衡建立时HI的转化率为b%,则a、b的关系为 ( )
2HI(g),测得HI的转化率为a%。其他条件不变,在上述平衡体系中再充入1molHI,待平衡建立时HI的转化率为b%,则a、b的关系为 ( )
A.a>b B.a<b C.a=b D.无法确定
4、一个真空密闭恒容容器中盛有1molPCl5,加热到200℃发生如下反应:PCl5(g)  PCl3 (g)+Cl2 (g),反应达到平衡时,混合气体中PCl5,所占体积分数为M%,。若同一温度的同一容器中,最初投入2 molPCl5,反应达平衡时,混合气体中PCl5,所占体积分数为N%。则M和N的关系是 ( )
PCl3 (g)+Cl2 (g),反应达到平衡时,混合气体中PCl5,所占体积分数为M%,。若同一温度的同一容器中,最初投入2 molPCl5,反应达平衡时,混合气体中PCl5,所占体积分数为N%。则M和N的关系是 ( )
(A) M>N (B) M=N (C) M < N (D)无法确定
5、在一固定容积的密闭容器中充入2molA和1molB,发生反应:2A(气)+B(气)  xC(气),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质,达到平衡后,C的体积分数仍为W%,则x值为 ( )
xC(气),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质,达到平衡后,C的体积分数仍为W%,则x值为 ( )
A、1 B、2 C、3 D、4
6、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:3A(气)+2B(气) xC(气)+yD(气),达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则的值分别为 ( )
xC(气)+yD(气),达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则的值分别为 ( )
A x=3 y=1 B x=4 y=1 C x=5 y =1 D x=10 y=2
7、在一定温度下,把2molSO2和1molO2通入一个一定容积的密闭容器里,发生反应:2SO2+O2  2SO3,当此反应进行到一定程度时,就达到化学平衡状态。若该容器中维持温度不变,令a、b、c分别代表初始时SO2、O2和SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡,反应混合物中三种气体的体积分数仍跟上述平衡时完全相同。填写下列空白:
2SO3,当此反应进行到一定程度时,就达到化学平衡状态。若该容器中维持温度不变,令a、b、c分别代表初始时SO2、O2和SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡,反应混合物中三种气体的体积分数仍跟上述平衡时完全相同。填写下列空白:
(1)若a = 0,b = 0,则c = 。
(2)若a = 0.5mol,则b = ,c= 。
(3)a、b、c取值必须满足的一般条件是(用两个方程式表示,其中一个只含a、c,另一个只含b、c)
8、有两个密闭容器A和B,A容器内有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B的容积相等。在保持4000C的条件下使之发生如下反应: 2 SO2+O2  2SO3。
2SO3。
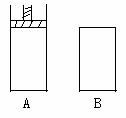
(1)达到平衡时所需要的时间A容器比B容器 ,A容器中SO2的转化率比B容器 。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器化学平衡 移动,B容器化学平衡 移动。
(3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数 ;B容器中SO3的物质的量分数 。(填增大、减小、不变)
答案:例题:1.C 2.AD 3.(1)AB (2)ABD
练习:.1.AD 2.D 3.C 4.C 5.BC 6.CD 7.(1)2mol (2)b=0.25mol,c=1.5mol (3)a+c=2 b+c/2=1(或2b+c=2)
8.(1)短、大 (2)逆向、不 (3)不变、增大

- 全部评论(0)
(739419385) 评论 href="/plus/view.php?aid=5386">等效平衡专题:呃 还是看不懂
(739419385) 评论 href="/plus/view.php?aid=5386">等效平衡专题:呃 还是看不懂
罗罗 评论 href="/plus/view.php?aid=5386">等效平衡专题:这对我很有帮助,Thankyou!!!
