浅谈有机反应方程式书写
时间:2022-03-24 11:05 来源:未知 作者:蒋景耘 点击: 次 所属专题: 有机方程式书写
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
化学方程式是中学化学课程中最重要的化学用语。学好化学方程式可以帮助学生理解化学反应原理,加深对实验现象的理解,更好的掌握物质的化学性质,提高学生应用化学知识解决实际问题的能力。能准确地写出化学方程式,可以客观地反映学生对化学反应原理的理解,对实验现象的认识以及对物质性质的掌握程度。
高考越来越重视学生基础知识,也越来越重视化学方程式的考查。2006年全国普通高考理综化学试题中,学生必须书写到卷面的化学方程式十一个(分值20分,占化学试题总分的18.52%),其中有机化学方程式六个。
有机化学方程式书写是高中生容易出错的一部分知识。为了帮助学生学好化学,准确表达顺利交流化学知识,笔者浅谈有机方程式书写。
一、注意简练科学,有机物写结构简式。
有机反应的实质是有机物内在组成和结构在一定条件下的外在表现。有机物的元素组成比较单一(主要由碳氢氧氮等组成),而一个分子内原子又往往比较多(例如蔗糖 C11H22O11),分子结构复杂,所以有机反应的实质主要是由有机物的分子结构决定的。“结构决定性质”,我们通常从有机物分子结构出发判断能发生什么样的反应。
学过《烃的衍生物》的同学知道分子式为C2H6O的物质可能是乙醇也可能是甲醚,即乙醇与甲醚互为同分异构体。有机物普遍存在同分异构体,有机物分子式无法体现分子结构。又因为多数有机物结构式复杂书写繁琐,所以反应方程式中有机物一般不写分子式也不写结构式而采用结构简式。结构简式既简练又突出官能团,在化学方程式中能简洁准确地体现出反应原理。
例1 写出乙醇和钠反应的化学方程式。
分析:醇和钠反应,本质是“金属钠置换出了羟基中的氢,生成了乙醇钠”(见人教2003版《全日制普通高级中学教科书》(必修加选修)化学第二册151页),乙醇分子内参加反应的是羟基,在书写反应方程式时一定要表示出乙醇中的羟基。所以反应方程式为
2CH3CH2OH+2Na→2CH3CH2OH+H2↑
2C2H5OH+2Na→2C2H5OH+H2↑
在书写有机物结构简式时,注意:
1、碳只能形成四个共价键,不能少写或多写氢。
例新戊烷(CH3)4C ,不能写成(CH2)4C或(CH3)4CH2。
2、一些基团的连接方式要即正确又合乎习惯,不产生歧义。
例醛基―CHO,不能写成CHO―也不能写成―COH(写成此种形式,可能会误认为碳原子和氧原子之间是单键)。
另外常见官能团―C6H5、―OH、―NO、―NH2、―COOH、―COO―等不能写成C6H5―、OH―、NO2―、NH2―、COOH―、―COO等,尤其注意官能团写在物质左侧的。
例2、写出由丙烯制聚丙烯的化学方程式。
nCH2=CH―CH3→ CH2―CH―CH3
CH2―CH―CH3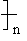
错因:⑴不明白加聚反应仅发生在“C=C”上,不知道新键生成位置。
⑵忽略每个碳原子只能形成四个共价键,既不能多也不能少。改正:
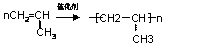
二、在中学阶段未知结构简式的有机物需注明物质名称。
例3、分别写出蔗糖麦芽糖水解的的化学方程式。
分析:蔗糖麦芽糖分子式均为C12H22O11,它们的结构不同在相同条件下发生不同的水解反应水解。但是中学生不知道蔗糖麦哦芽糖的结构式,为准确表示反应,必须注明物质名称。
写出化学方程式为
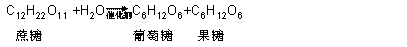
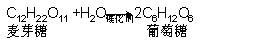
三、注意有机反应的条件
化学反应不是反应物间的简单加和而是相互作用,反应条件不同相互作用强弱就不同。化学反应的实质是旧键断裂新键生成。大多数有机物分子结构相对于无机物复杂,同一分子中存在不同化学键。相同的有机反应物常因反应条件不同,断裂不同化学键(或旧键断裂位置不同)生成不同化学键(或新键生成位置不同)从而生成不同产物。例如乙醇和浓硫酸的混合液加热,当反应温度不同时,乙醇中断裂化学键不同会生成不同的物质——当混合液加热到170℃时,乙醇分子内两个碳原子分别断裂碳氧键碳氢键,即分子内的羟基与相邻碳原子上的一个氢原子,结合成一分子水而脱去,结果是生成不饱和的碳碳双键,生成乙烯;当加热到140℃时,一分子乙醇中的羟基结合另一分子乙醇中羟基上的氢原子,生成一分子水而脱去,其余部分结合成一分子乙醚。另外,在加热的条件下,硫酸分子中的羟基和磺酸基之间的硫氧键断裂,所以乙醇分子中羟基上的氢原子还会结合硫酸分子中的羟基生成一分子水而脱去,生成硫酸氢乙酯。其化学方程式分别为:
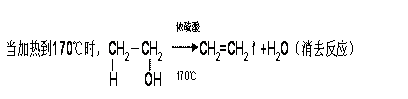
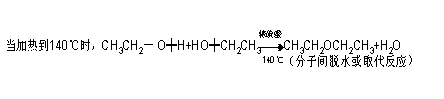
在加热时一般都发生CH3CH2O―H+HO―SO3H →CH3CH2OSO3H+H2O(酯化反应或取代反应)再如乙醇的氧化反应,条件不同产物不同。
![]()
![]()
![]()
因此要充分注意反应条件(温度、压强、催化剂、溶剂的性质、光等)对反应产物的影响。在书写有机反应方程式时要特别注意标明反应条件。
四、注意产物正确
有机反应常见类型有氧化反应、加成反应、消去反应、取代反应酯化反应等。弄清楚这些反应进行的方式和反应发生的部位,对于我们快速而准确地写出有机反应的化学方程式是很重要的。
![]()
分析:醇和酸发生酯化反应是分子间脱去一分子水,其本质是醇羟基中的氢原子和酸分子中的羟基结合成一分子水而脱去,其余部分结合成酯。所以反应方程式为:
![]()
五、不丢小分子
中学教材中,有机反应既写主要有机产物也写无机小分子产物,中学生在书写酯化反应取代反应、消去反应、缩聚反应时常常漏写小分子。
例5、写出苯和液溴反应的化学方程式。
![]()
错因分析:⑴结构简式与化学式互现能力差,或粗心大意忽略原子守恒
⑵根本不清楚反应原理,机械记忆又不准确。
苯和液溴反应属于取代反应,在催化剂的作用下苯环上的一个氢原子和溴分子中的一个溴原子结合成一分子溴化氢而脱去,其余部分结合成溴苯。
![]()
建议:写有机化学方程式时,首先弄清反应原理,其次要细心。
小窍门:为防止漏写小分子,写产物时,可先“小”后“大”,最后配平方程式。
六、注意产物的聚集状态
有不同于反应物聚集状态的产物,要用特定符号表示出。例如,溶液中的反应,生成固体的,在固体产物右边标“↓”符号,生成气体的,在气体产物右边标“↑”符号。
例6、写出下列实验的发挥应化学方程式:
⑴向苯酚溶液中滴入过量浓溴水;
⑵向小苏打溶液中滴入醋酸。
分析:写出的化学方程式要准确表述实验现象。所以,⑴要用符号表示出向苯酚中滴入过量浓溴水立即生成白色沉淀的现象,必须在生成的不溶物右边标出“↓”⑵要用符号表示出向小苏打溶液中滴入醋酸迅速产生气泡的现象,必须在生成的气体右边标出“↑”。化学方程式分别为

七、注意反应物和生成物之间的连接符号
有机反应比较复杂,常常除主反应外还伴有副反应。因此书写有机反应方程式时,反应物与产物之间一般用“→”连接。但是典型的可逆反应用“![]() ”连接,燃烧反应也可用“=”连接。
”连接,燃烧反应也可用“=”连接。
总之,化学方程式是对化学反应的客观表述,具体选用哪些特定符号是以客观事实为基础的。希望同学们学好化学,会读化学方程式,从书面的化学方程式中获得丰富信息:写好化学方程式,准确表达自己掌握知识。

- 全部评论(0)
