������������л�����������ЩӰ�죿
ʱ��:2025-09-02 09:19 ��Դ:δ֪ ����:��ѧ��ϰ�� ���:�� ����ר�⣺ �л��ﻯѧ���� ���
��Ȩ��������������Ϊ����ѧ��ϰ�ҡ�����ζ��δ����ϵ��ԭ���ߣ���ԭ���߿�����������ϵ�����䣺79248376@qq.com����
�������������������ָͬһ�������γɵ��������������Ԫ����Ԫ���ṹ����ˮ��ȩ��ˮ��������ڵ�����ṹ��
���������ͨ�����ı���Ӽ����á����ȶ��ض��ṹ(�����ӡ�����ϩ��ʽ)��������Ӱ���л���������۷е㡢�ܽ�ȡ����ԡ������ȶ��Լ������칹ƽ�⡣������������γ����ֱ�Ӿ�����������۽ṹ�ȶ��Լ�������ʱ��֣��������л����������ʲ���Ĺؼ�����֮һ��

һ��������������ͻ�������۷е�
������������������Ӽ������������»������۷е㽵�͡�
����1������������������������۷е�ĶԱ�
�����۷е���������������������۵��45.3�桢�е�216�棬������ˮ�����ӷ��������������۵�114��C���е�279��C������λ��
�����������У�-OH����λ-NO₂����ԭ���γɷ��������(��Ԫ���������ṹ)���谭���Ӽ�������γɣ���������������-OH��-NO₂����Զ�����γɷ�������������Ӽ��ͨ���������
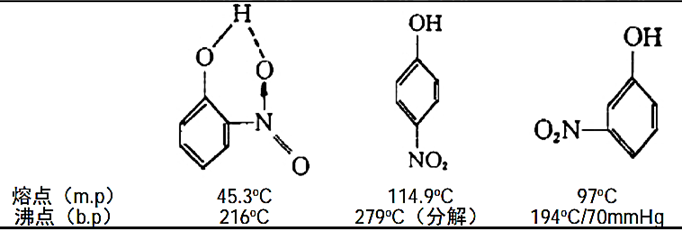
���Ƶأ����ӵ���λ������(�����ǻ�������)Ҳ�������������ӷ��Ը��ڼ�λ����λ�칹�塣
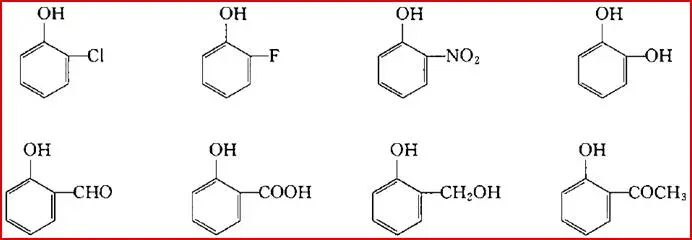
���������ڸı仯������ܽ��
���л�������γɷ���������������ڼ����ܼ��е��ܽ�ȼ�С����֮�ڷǼ����ܼ��е��ܽ�ȱ��
����2�����ǻ�����ȩ����ǻ�����ȩ���۷е���ܽ�ȵĶԱ�

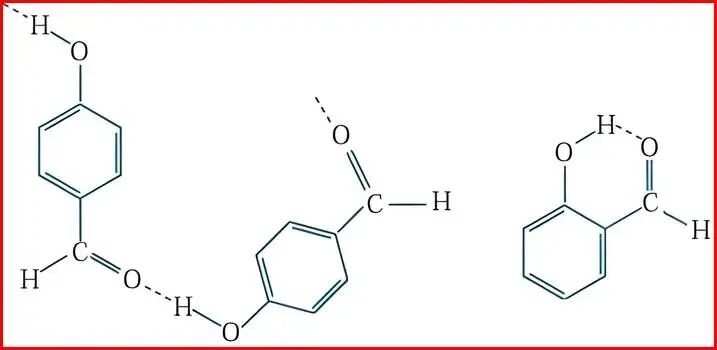
����3������������������������ܽ�ȵĶԱ�
20��Cʱ��������ˮ���ܽ�ȱ�Ϊ0.39:1�����ڱ�����Ϊ1.39:1��
�������������γɷ����������������ˮ�γ����������ˮ�е��ܽ�Ƚϵͣ�����������������ˮ�γɷ��Ӽ�������ܽ�Ƚϸߡ��γɷ�����������л��������ڷǼ����ܼ��е��ܽ����ˮ��Һ��ǡ���෴��
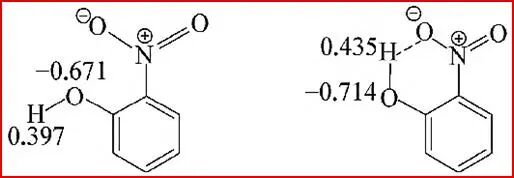
��������������Ի��������Եĵ�������
������������л������Ե�Ӱ��ȿ�����ǿ������Ҳ�����������������Ӱ�������˫����������H⁺�����γɵ��������ܱ�����������ȶ��乲���ʱ����������ǿ����H⁺δ���ʱ����������谭H⁺�ͷ��������Լ�����
����4�����ǻ�������(������ǿ)
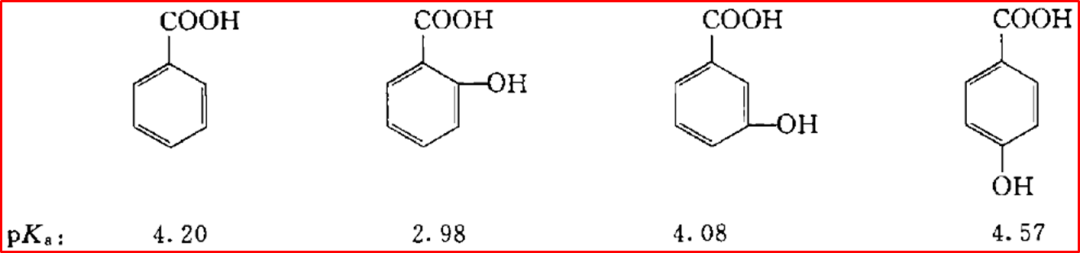
����5������������(���Լ���)
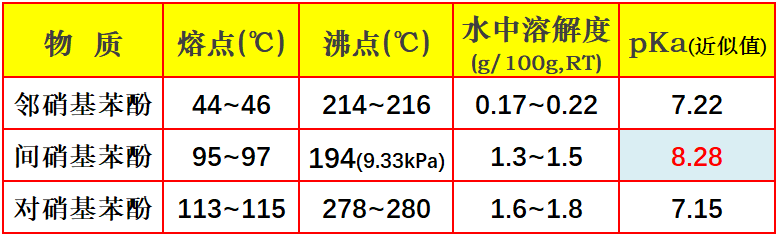
����ע������ChemicalBook�����ݣ��������������ϵ��(pKa)ֵΪ8.28(at 25��)��PHֵ6.6-8.6 (H2O, 20��)���ԡ���ѧ����326���������������������ǿ���Ǽ�������һ���е���������������
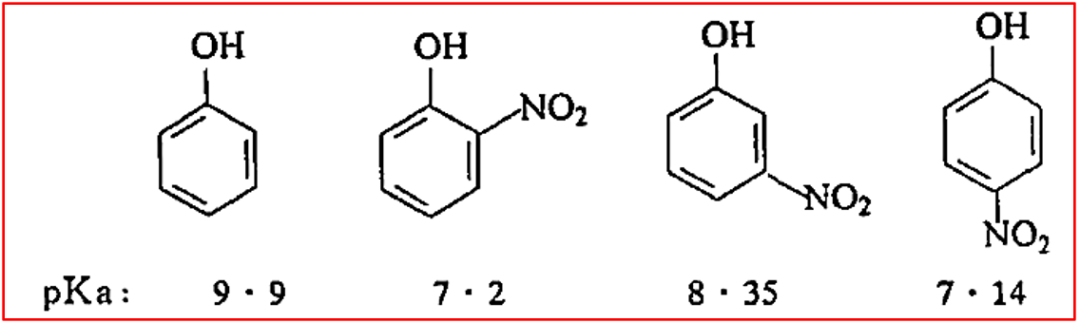
����6��˳��ϩ�����뷴��ϩ����(����˫������)
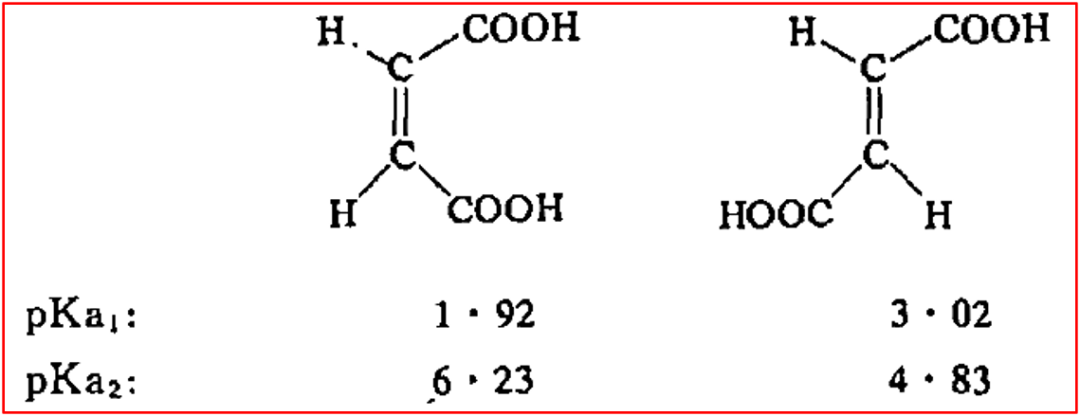
�ġ�����������Է��ӽṹ�ȶ��Ե�Ӱ��
1.�ٽ�ϩ��ʽ�����칹���ȶ�
����7������������������
��������Ǽ��������Ȼ���������˫��Ӱ�죬����ԭ�Ӹ�Ϊ���ã������ܹ��γ�һ��������ϩ��ʽ�칹�壬�γɵ�ϩ��ʽ�칹���ܹ����ǻ��ϵ���ԭ���������е���ԭ���γɷ�����������ȶ������е�ϩ��ʽ�ṹ���ձ�����ŷ������������������������ϩ��ʽ�������γɷ��������(O��H⋯O=C)���ȶ����ܹ��������ڡ�
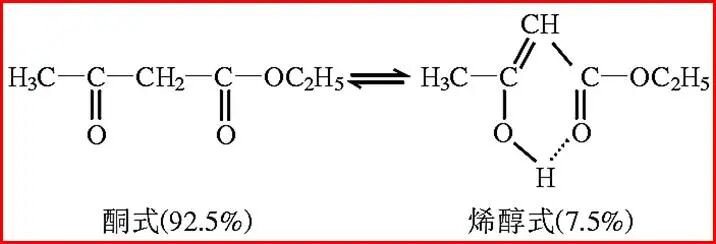
���Ƿ���������Ĵ��ڣ�������ϩ��ʽ���ȶ�����ǿ��ʹ���ڻ����칹ƽ����ռ��һ��������������ռ��Ҫ�ɷ֡�
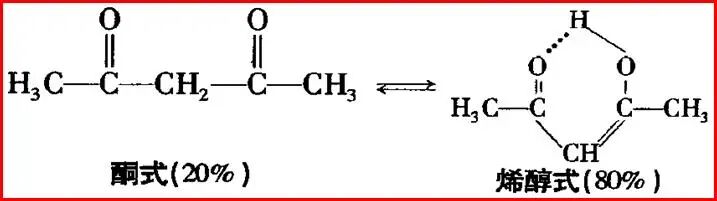
2.����ṹ���ȶ�
����8������ͪ
���л��������У�ͬһ̼ԭ��������2���ǻ���һ�ֲ��ȶ��Ľṹ������ˮ�γ��ʻ�����������ͪ��������ˮ������γɷ��������������һ�����ȶ��ԣ�����ˮ���Խᾧ����ʽ���ڡ�
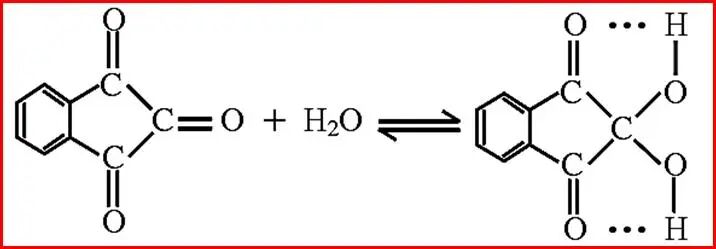
�塢����������Լ��Ե�Ӱ��
����9���ڼ�����
���ڼ����������еļ�C-H��Nԭ���γ�����������͵����������ܶȣ�ʹ��������ڼ�λ�Ͷ�λ�칹�塣
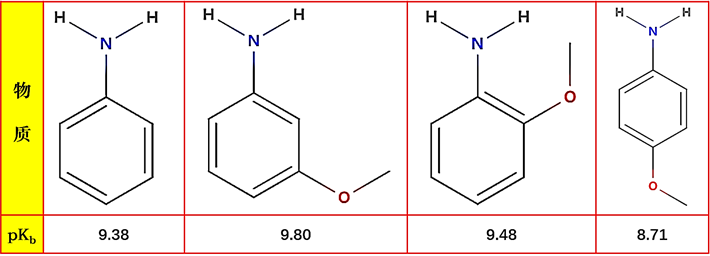
��������������Ժ������Ӱ��
������γ��������״�λ�ú�ǿ�ȶ��м����Ե�Ӱ�죬��������շ�����������ߵIJ���(���Ͳ���)�������������ʹ-OH������Ƶ����Ͳ����ƶ���ͨ����3000�C3200cm⁻¹���ֿ��壬�Ҳ���Ũ��Ӱ�죬��˿�����Ӽ�����Ա����֡�
����10����������������ϩ��ʽ�ṹ�У�-OH���շ������Լ3000cm⁻¹��



- ȫ�����ۣ�0��
