周期表中元素分区
时间:2012-11-29 12:56 来源:未知 作者:陈女婷 点击: 次 所属专题: 元素分区
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
根据元素原子的电子层结构特征,可将周期表中元素分为5个区(见下图):
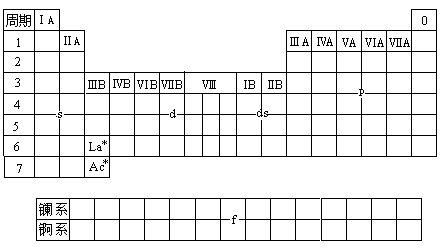
①s区元素 包括ⅠA族碱金属和ⅡA族碱土金属,价电子层结构为ns1和ns2。这些元素的原子最外层只有1或2个电子,很易失去形成+1或+2价离子,都是活泼的金属元素。
②p区元素 包括ⅢA族到零族元素,价电子层结构从ns2np1→ns2np6,只是np电子数不同,都是典型的主族元素。
③d区元素 包括ⅢB族到Ⅷ族元素,价电子层结构为(n-1)d1-9ns1-2,次外层的d电子一般未充满,主要差别在d电子上,因此性质比较相似,都是金属元素,也称为过渡元素。
④ds区元素 包括ⅠB族和ⅡB族、价电子层结构为(n-1)d10ns1-2,次外层d电子是充满的。它们既不完全同于s区元素也不完全同于d区元素。
⑤f区元素 包括镧系和锕系元素,价电子层结构是(n-2)f0-14ns2或(n-2)f0-14(n-1)d1-2ns2,主要差别在倒数第三层f电子数不同,化学性质极其相似,都是金属,也称为内过渡元素。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
