化学元素趣闻--碳族元素
时间:2014-04-24 09:34 来源:未知 作者:周书峰 点击: 次 所属专题: 化学元素概述 碳族
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
有机世界的“主角”——碳C
碳在地球上虽不算太少,但也不算太多,按重量计算,占地壳中各元素总重量的千分之四,按原子总数计算不超过千分之一点五,然而,碳的足迹却遍布全球。
在大自然中,有纯净的碳。比如说,金刚石便是非常纯净的碳——在纯净的氧气中,金刚石居然会燃烧,变成二氧化碳!金刚石是最坚硬的东西,人们用它来裁玻璃,或者装在钻探机的钻头上,成为向地层深处进军的开路先锋。不过,天然的金刚石终究不多,不能满足工业上的需要。现在,我国已试制成功人造金刚石——在高温高压下,用石墨制造金刚石。
用石墨怎么能制造金刚石呢?这是因为石墨也是很纯净的碳。铅笔的笔芯,就是用石墨做的。石墨与金刚石的脾气大不一样,它很软,在纸上一划,便留下一条黑道道,因此常用作铅笔芯。石墨能耐3000℃以上的高温,在工业上用石墨制造坩埚来熔炼钢、铜。石墨还能导电,被用作电极,干电池里那个黑芯子,便是石墨。
金刚石和石墨都是碳,为什么性质截然不同呢?这是因为它们的晶体结构不同。在金刚石中,碳原子排列非常规则,在每一个碳原子周围有四个等距离的碳原子,构成一个正四面体,所以金刚石比重大,坚硬。而是末的晶体结构则是层状,层与层之间距离较大,容易滑动,所以石墨比重比金刚石小,而且软、滑。金刚石与石墨,叫“同素异形体”。既有同一元素构成的两种性质不同的物体。
木炭、煤、骨灰也是碳(含有一些杂质),叫做无定形碳。我国是世界上最早知道用煤作燃料的国家,早在三千多年前,我国便已用“黑石”(即煤)来取暖、烧饭。煤被誉为“工业的粮食”。正当我国人民以更加优异成绩庆祝党的第十次全国代表大会胜利闭幕的时候,我国又新建成一座大型现代化露天煤矿并已投入生产。煤是最重要的工业燃料。经过炼焦后,从煤焦油中还能得到苯、苯酚等五百多种工业原料。烟囱里的烟炱也是纯净的碳。烟炱用来制造墨、墨汁、油墨。在橡胶中加入烟炱,可以使它的机械强度增加十倍。现在90%的烟炱,都是用作橡胶的“增强剂”。
木头、煤、炭等燃烧后,生成了二氧化碳。二氧化碳是无色五味的气体,比空气略重,在空气重的含量为万分之三。一加压力,二氧化碳很易变成无色的液体,温度更低些,则变成白色、雪花般的晶体——干冰。二氧化碳易溶解于水,汽水里便溶有二氧化碳。二氧化碳不助燃,化学灭火剂喷出的气体便是二氧化碳。任、动物、植物在呼吸时不断吐出二氧化碳,据统计,全人类每年呼出的二氧化碳达十亿八千万多吨。而全世界工厂、火车、轮船的烟囱,每年要吐出一百多亿吨二氧化碳。这样下去,世界岂不成了二氧化碳的世界吗?不,不会,原来大自然中有一个奇妙的循环:植物在光合作用时,吸收大量二氧化碳,吐出氧气,这样,二氧化碳才不致于越来越多。
煤不完全燃烧,会生成一氧化碳。一氧化碳是剧毒的气体,“煤气”中毒,这“煤气”便是一氧化碳。一氧化碳在工业上是重要的燃料和原料。一氧化碳燃烧士产生蓝色的火焰,炉膛的煤层上常看见浅蓝色火苗,那便是一氧化碳在燃烧。
山上巨大的石灰岩,也是碳的化合物——碳酸钙。石灰岩可以作建筑材料、铺路、造桥。石灰岩在石灰窑中灼烧后,可变成生石灰(氧化钙),生石灰常用来做建筑粘合剂或粉刷墙壁。生石灰遇水后,变成熟石灰(氢氧化钙),同时放出大量的热。
石油,更是碳的化合物的“仓库”。石油主要是各沸点不同的碳氢化合物的混合物。石油被誉为“工业的血液”,从石油中可提取汽油、煤油、柴油,是工业上最重要的液体燃料,用来开动各种内燃机。用石油作原料,还可制造塑料、合成纤维、合成橡胶等三大合成材料。
天然气常和石油矿“住”在一起。天然气的主要成分是甲烷也是碳氢化合物,用作气体燃料和化工原料。
碳,是生命的基础。一切动、植物体中的有机质,都是碳的化合物——蛋白质、油脂、淀粉、糖以及叶绿素、血红素、激素,都离不了碳。在工业上,碳的化合物也是非常重要的,象塑料、化学纤维、橡胶、香料、染料、制药等有机化学工业,绝大部分都是生产碳的化合物。

宇宙中发现的碳的同素异形体--石墨烯与富勒烯
无机世界的“主角”——硅
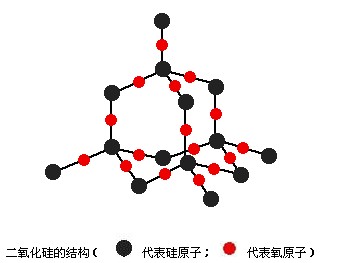
如果说碳是有机世界的“主角”,那么无机世界的“主角”该是算硅了。硅是地壳中第二个含量最多的元素,占地壳总重量的26%,仅次于氧;而在地壳中,绝大部分硅是以二氧化硅SiO2的形势存在的,据统计,二氧化硅占地壳总重量的87%,这也就是说,硅和氧这两种最多的元素所形成的无机化合物,几乎“垄断”了地壳。重要的岩石,如长石类、辉石类、角闪石类和云母类,都含有二氧化硅(或以其它形势存在的硅的化合物)。砂子中也含有大量的二氧化硅。最纯净的二氧化硅要算是石英了。具有六面角柱形,头上带有六面角锥的透明无色的石英结晶,便是水晶。水晶硬而透明,特别是能很好的透过紫外线,折光率大,在光学上具有重要用途。水晶眼镜,便是用水晶磨成的。水晶图章,美观而耐用。水晶中如含有一些杂质,则带有颜色,如紫水晶、烟水晶。在大自然中,大的水晶不多,最大的有一米多高。
所有的植物都含有硅,特别是马尾草和竹子中含硅最多。动物中含硅较少。在海绵、鸟的羽毛、动物的毛发中含有硅。人体中含硅量约为万分之一。
人们早在远古时代便和硅的化合物打交道。但是,纯净的硅直到1811年才第一次被制得。到1823年,硅才被确定为化学元素。粉末状的纯硅,是棕褐色的,在空气中可燃烧变成二氧化硅。如果把粉末状硅溶解在熔化了的金属(如锌、镁、银)中,慢慢冷却,可制得以完整的八面体析出的结晶硅。结晶硅具有钢灰色的金属光泽,熔点为1414℃,具有显著的导电性。纯净的结晶硅(含硅量达99.9999%以上),是现在最重要的半导体材料之一,与锗Ge齐名。
硅和碱作用,能析出大量的氢气。制备1立方米的氢气只需0.63公斤硅,如果改用金属的话,却需2.9公斤的锌或2.7公斤的铁。在工业上,用焦炭在电路中还原二氧化硅SiO2(石英)来制取纯硅。
纯硅的用途并不太广,最重要的硅的化合物是二氧化硅,它是重要的工业原料。玻璃工业每年消耗几百万吨的砂子,因为玻璃是用砂子(主要成分二氧化硅SiO2)、苏打(碳酸钠Na2CO3)和石灰石(主要成分碳酸钙CaCO3)作原料熔炼成得。用纯二氧化硅——石英制成的石英玻璃,能耐高温,即使剧烈灼烧后立即浸到水里也不会破裂。由于石英玻璃能很好的透过紫外线,所以常用来制造光学仪器。纯净的玻璃是无色的。加入不同的化学元素,可使玻璃产生不同的颜色:电焊工人所戴的蓝色护目镜片,是加了氧化铈或氧化钕。加入氧化铁Fe2O3,玻璃呈黄色。若加入氧化亚铁FeO,则变成红色。若加入极细的金粉Au、铜粉Cu或硒粉Se,玻璃呈红色。若加入极细的银粉Ag,则呈黄色。
粘土的主要成分是水化硅酸铝。粘土大量被用来和石灰石一起煅烧,制成水泥。粘土也被用来烧制砖、瓦等建筑材料。纯净的粘土——高岭土,是制造瓷器、陶器最重要的原料。玻璃、水泥、陶瓷、建筑材料等工业,均以硅为“主角”,被合称为“硅酸盐工业”。
硅和碳的化合物——碳化硅,俗称金刚砂,是无色的晶体,含有杂质时为钢灰色,它非常坚硬,硬度和金刚石相近。在工业上,常用金刚砂制造砂轮和磨石。它还很耐高温,用来做耐火的炉壁。
硅和氯的化合物——四氯化硅SiCl4,是无色的液体,很易挥发,在57℃就沸腾。在军事上用来作烟雾剂,因为它一遇水,便水解生成硅酸和氯化氢SiCl4+3H2O→H2SiO3+4HCl,产生极浓的白烟。特别是海战时,水蒸气多,烟雾更浓。四氯化硅的成本比白磷P4低廉的多。
硅虽然是无机世界的“主角”,但是近年来,它在有机世界中也成为引人注目的角色——人们制成了一系列有机硅化合物。有机硅有个特性——憎水。一些药品瓶的内壁,如青霉素瓶,便常涂着一层有机硅。这样,在使用后瓶壁上就不会留有药液。巍立在首都广场上的人民英雄纪念碑,表面也涂着一层有机硅,这样可以防尘防潮,保护那精美的浮雕。有机硅塑料具有很好的绝缘性能,如果用它作为电动机的绝缘材料,可以使电动机的体积和重量都减少一半,而使用寿命却可以延长八倍多,并且在高温、潮湿的情况下都能使用。有机硅橡胶,在冰天雪地之中(甚至低到-90℃),或在烈曰酷晒之下(甚至高达350℃),都不龟裂、不老化、保持弹性,用它来制造汽车轮胎非常合适。
马口铁的“外衣”——锡
锡是大名鼎鼎的“五金”——金、银、铜、铁、锡之一。早在远古时代,人们便发现并使用锡了。在我国的一些古墓中,便常发掘到一些锡壶、锡烛台之类锡器。据考证,我国周朝时,锡器的使用已十分普遍了。在埃及的古墓中,也发现有锡制的曰常用品。
在自然界中,锡很少成游离状态存在,因此就很少有纯净的金属锡。最重要的锡矿是锡石,化学成分为二氧化锡。炼锡此炼铜、炼铁、炼铝都容易,只要把锡石与木炭放在一起烧,木炭便会把锡从锡石中还原出来。很显然,古代的人们如果在有锡矿的地方烧篝火烤野物时,地上的锡石便会被木炭还原,银光闪闪的、熔化了的锡液便流了出来。正因为这样,锡很早就被人们发现了。
我国有丰富的锡矿,特别是云南崮旧,是世界闻名的“锡都”。此外,广西、广东、江西等省也都产锡。1800年,全世界锡的年产量仅四千吨,1900年为八万五千吨,1940年为二十五万吨,现在已超过六十万吨。
锡是银白色的软金属,比重为7.3,熔点低,只有232,你把它放进煤球炉中,它便会熔成水银般的液体。锡很柔软,用小刀能切开它。锡的化学性质很稳定,在常温下不易被氧气氧化,所以它经常保持银闪闪的光泽。锡无毒,人们常把它镀在铜锅内壁,以防铜温水生成有毒的铜绿。牙膏壳也常用锡做(牙膏壳是两层锡中央着一层铅做成的。近年来,我国已逐渐用铝代替锡制造牙膏壳)。焊锡,也含有锡,一般含锡61%,有的是铅锡各半,也有的是由90%铅、6%锡和4%锑组成。
锡在常温下富有展性。特别是在100℃时,它的展性非常好,可以展成极薄的锡箔。平常,人们便用锡箔包装香烟、糖果,以防受潮(近年来,我国已逐渐用铝箔代替锡箔。铝箔与锡箔很易分辨——锡箔比铝箔光亮得多)。不过,锡的延性却很差,一拉就断,不能拉成细丝。
其实,锡也只有在常温下富有展性,如果温度下降到13.2℃以下,它竟会逐渐变成煤灰般松散的粉末。特别是在-33℃或有红盐(SnCl4·2NH4Cl)的酒精溶液存在时,这种变化的速度大大加快。一把好端端的锡壶,会“自动”变成一堆粉末。这种锡的“疾病”还会传染给其他“健康”的锡器,被称为“锡疫”。造成锡疫的原因,是由于锡的晶格发生了变化:在常温下,锡是正方晶系的晶体结构,叫做白锡。当你把一根锡条弯曲时,常可以听到一阵嚓嚓声,这便是因为正方晶系的白锡晶体间在弯曲时相互摩擦,发出了声音。在13.2℃以下,白锡转变成一种无定形的灰锡。于是,成块的锡便变成了一团粉末。
锡不仅怕冷,而且怕热。在161℃以上,白锡又转变成具有斜方晶系的晶体结构的斜方锡。斜方锡很脆,一敲就碎,展性很差,叫做“脆锡”。白锡、灰锡、脆锡,是锡的三种同素异性体。
由于锡怕冷,因此,在冬天要特别注意别使锡器受冻。有许多铁器常用锡焊接的,也不能受冻。1912年,国外的一支南极探险队去南极探险,所用的汽油桶都是用锡焊的,在南极的冰天雪地之中,焊锡变成粉末股的灰锡,汽油就都漏光了。
锡的化学性质稳定,不易被锈蚀。人们常把锡镀在铁皮外边,用来防止铁皮的锈蚀。这种穿了锡“衣服”的铁皮,就是大家熟知的“马口铁”。1吨锡可以覆盖七千多平方米的铁皮,因此,马口铁很普遍、也很便宜。马口铁最大的‘主顾”是罐头工业。如果注意保护,马口铁可使用十多年而保持不锈。但是,一旦不小心碰破了锡“衣服”,铁皮便很快被锈蚀,没多久,整张马口铁便布满红棕色的铁锈斑。所以,在使用马口铁时,应注意切勿使锡层破损,也不要因它受潮、受热。“马口铁”这名字,是由于它是从西藏阿里部马口地方输入(英国经印度从马口输入)而得名的。
锡,也被大量用来制造锡铜合金——青铜。
锡与硫的化合物——硫化锡,它的颜色与金子相似,常用作金色颜料。
锡与氧的化合物——二氧化锡。锡于常温下,在空气中不受氧化,强热之,则变为二氧化锡。二氧化锡是不溶于水的白色粉末,可用于制造搪瓷、白釉与乳白玻璃。1970年以来,人们把它用于防止空气污染——汽车废气中常含有有毒的一氧化碳气体,但在二氧化锡的催化下,在300℃时,可大部转化为二氧化碳。
锡和氯可形成两种化合物:1.二氯化锡(又称氯化亚锡),具有很强的还原能力,工业上常利用氯化亚锡使别种金属还原,是化学上常用的还原剂之一;在染料工业上,也可用做媒染剂。2.四氯化锡:在二氯化锡溶液里通入足量的氯气,便可得到四氯化锡,四氯化锡是沸点为114的无色液体。——遇水蒸气就水解,冒出强烈的白烟,形成白色的浓雾,军事上用它装在炮弹里,制成烟雾弹。四氯化锡能与氯化铵化合,生成一种复盐(SnCl4·2NH4Cl),是重要的媒染剂。


(矿物锡石主要成分二氧化锡是提取金属锡的主要原料)
蓄电池的“主角”—铅
铅的“资格”够老的了,人们早在几千年前便已认识铅了。我国在殷代末年纣王时便已会炼铅。古代的罗马人喜欢用铅作水管,而古代的荷兰人则爱用它作屋顶。
铅是银白色的金属(与锡比较,铅略带一点浅蓝色),十分柔软,用指甲便能在它的表面划出痕迹。用铅在纸上一划,会留下一条黑道道。在古代人们曾用铅作笔。“铅笔”这名字,便是从这儿来的。铅很重,一立方米的铅重达11.3吨,古代欧洲的炼金家们便用旋转迟缓的土星来表示它,写作“h”。铅球那么沉,便是用铅做的。子弹的弹头也常灌有铅,因为如果太轻,在前进时受风力影响会改变方向。铅的熔点也很低,为327℃,放在煤球炉里,也会熔化成铅水。
铅很容易生锈——氧化。铅经常是呈灰色的,就是由于它在空气中,很易被空气中的氧气氧化成灰黑色的氧化铅,使它的银白色的光泽渐渐变得暗淡无光。不过,这层氧化铅形成一层致密的薄膜,防止内部的铅进一步被氧化。也正因为这样,再加上铅的化学性质又比较稳定,因此铅不易被腐蚀。在化工厂里,常用铅来制造管道和反应罐。著名的制造硫酸的铅室法,便是因为在铅制的反应器中进行化学反应而得名的。
金属铅的重要用途是制造蓄电池。据不完全统计,197l年,铅的世界年产量达308.3万吨,其中大部分是用来制造蓄电池。在蓄电池里,一块抉灰黑色的负极都是用金属铅做的。正极上红棕色的粉末,也是铅的化合物—一氧化铅。一个蓄电池,需用几十斤铅。飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源。工厂、码头、车站所用的“电瓶车”,这“电瓶”便是蓄电池。广播站也要用许多蓄电池。
金属铅还有一个奇妙的本领——它能很好地阻挡X射线和放射性射线。在医院里,大夫作X射线透视诊断时,胸前常有一块铅板保护着;在原子能反应堆工作的人员,也常穿着含有铅的大围裙。铅具有较好的导电性,被制成粗大的电缆,输送强大的电流。铅字是人们熟知的,书便是用铅字排版印成的,然而,“铅字”并不完全是铅做的,而使用活字合金浇铸成的。活字合金一般含有5一30%的锡和10一20%的锑,其余则是铅。加了锡,可降低熔点,便于浇铸。加了锑,可使铅字坚硬耐磨,特别是受冷会膨胀,使字迹清晰。
保险丝也是用铅合金做的,在焊锡中也含有铅。
铅的许多化合物,色彩缤纷,常用作颜料,如铬酸铅是黄色颜料,碘化铅是金色颜料(与硫化锡齐名)。至于碳酸铅,早在古代就被用作白色颜料。考古工作者发掘到的古代壁画或泥俑,其中人脸常是黑色的。经过化学分析和考证,证明这黑色的颜料是铅的化合物——硫化铅。其实,古代涂上去的并不是黑色的硫化铅,而是白色的碳酸铅。只不过由于长期受空气中微量硫化氢或墓中尸体腐烂产生的硫化氢的作用,才逐渐变成了黑色的硫化铅。这件事一方面说明碳酸铅作为白色颜料的历史很悠久,另一方面也说明碳酸铅作白色颜料有很大的缺点——变黑。现在,我国已不大用碳酸铅作白色颜料,而是用白色的二氧化钛——俗称“钛白”。铅的最重要的有机化合物是四乙基铅,常用作汽油的防爆剂。
铅和铅的化合物有毒。考古工作者们在发掘古罗马的墓时,曾发现尸骨上常有一些黑斑。经化学分析,确定是硫化铅。骨头里怎么会有硫化铅呢?经考证,原来古罗马人是用铅管做自来水管。水中总溶有少量的氧气,它能与铅作用,生成微溶于水的氢氧化铅。这种自来水被喝进人体后,铅就把骨骼中的钙取代出来,积存于骨骼。久而久之,铅越积越多。人死后,尸体腐烂时产生硫化氢气体,与骨骼中的铅生成黑色的硫化铅。达件事说明铅不仅有毒,而且是积累性的。铅最易积累于人的牙床。这样,中了铅毒的人,牙床边缘便变成灰色。铅中毒使人腹痛,严重的会发展到神经错乱。正因为这样,用铅做茶壶、酒壶,是不适宜的。在炼铅工厂中,要特别注意做好预防铅中毒的工作。
我国是世界上最早会炼铅的国家之一。我国著名的炼丹著作《周易参同契》中,便说: “胡粉投火中,色坏还为铅”。据考证,胡粉即氧化铅。“投火中”后,氧化铅被炭还原成金属铅,于是“色坏”,从黄色“还为铅”。《周易参同契》是我国公元二世纪时魏伯阳的著作,可见我国很早便会炼铅了。不过,在我国古籍中,常把铅与锡并称而又互相混用。《管子》中说:“上有陵石者下有铅锡。”《博物志》中说:“烧铅锡成胡粉。”《太平寰宇记》中引《尔雅》说:“锡之善者曰铅。”都是如此。这是由于铅与锡不仅都是易被木炭还原的金属,几乎同时被人们发现,而且它们的外貌、性质十分类似,容易被混为一谈。
铅占地壳总原子数的十万分之一。在大自然中,最重要的铅矿是方铅矿。我国有丰富的铅矿。

(方铅矿PbS)

- 全部评论(0)
