氧化物的分类归纳
时间:2016-04-21 16:47 来源:未知 作者:谭飞鸣 点击: 次 所属专题: 氧化物
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
氧元素与另外一种元素所组成的二元化合物 叫做氧化物。其通式可表示为XOM。在氧化物 中,由于氧元素化合价和尤元素的种类、化合价 的多样性,导致氧化物无论在种类上,还是在性质 上都是多种多样的。人们在对氧化物进行分类 时,习惯根据氧化物的性质,把它们划分为酸性、 碱性、两性和不成盐氧化物等简单的几种类型,没 有从氧化物的结构、组成、以及价态上进行完整地 考虑。这样,在理论上和实际应用中,都有很多不完善之处。笔者根据近几年查阅的书刊报道和工 作经验,对氧化物从价态、组成、结构和性质上全面考虑进行分类如下:
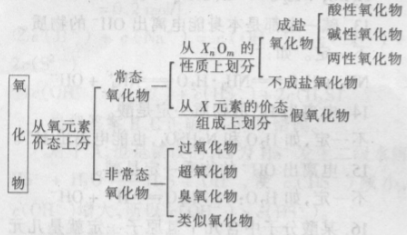
这样分类后能够使人们对氧化物的认识更完 善、更合理。同时,对某些氧化物名称的来源,实 际组成和与现行说法的差别,以及某些类型氧化物在特殊条件下的“名不符实”等,作一简单介绍。
一、酸性氧化物
酸性氧化物的主要特征是能与碱作用生成盐 和水。它包括大多数非金属氧化物和某些金属元 素的高价氧化物。例如SO3、Mn2O7等。
许多酸性氧化物能直接与水作用生成相应的 酸。但也有一些酸性氧化物不能与水直接化合。 例如SiO2、B2O3)等。
二、碱性氧化物
碱性氧化物的主要特征是能与酸作用生成盐和水。它包括大多数的金属氧化物。碱性氧化物 中除了少数金属性较强的钠、钾等的氧化物能与水直接化合生成相应的碱外,大多数碱性氧化物 都是难溶于水的。
某些金属元素,在与氧结合时、可显示多种价态。通常它们的高价氧化物是酸性氧化物,低价氧化物是碱性氧化物,而处于中间价态的氧化物则为两性氧化物。例如,锰的氧化物中,Mn2O7和 MnO,为酸性氧化物,MnO和MnJOJ为碱性氧化 物,而MnO2则是两性氧化物。
三、两性氧化物
两性氧化物是介于酸性氧化物和碱性氧化物 之间的一类氧化物。它兼有酸性氧化物和碱性氧 化物的特征,既可与酸作用生成盐,又可与碱作用 生成盐。例如Al2O3,ZnO等。
四、不成盐氧化物
在氧化物中,有极少数氧化物象NO、N2O、 CO、H2O等。它们在一般条件下既不与水作用, 又不与酸类或碱类物质作用(H2O除外),我们称 之为不成盐氧化物。
这里需要说明的是:有些不成盐氧化物在一 定条件下是可以“成盐”的。如CO,在工业上制备 甲酸,就是利用CO和NaOH在一定条件下反应来 制取的:CO+NaOH=HCOONa 在中学阶段,我们将CO划分到不成盐氧化物类, 是因为中学化学中还没有涉及象上述的用CO制甲酸这方面的知识。同时也提示我们:在教学中, 不能将某些概念或定义讲得太死,要留有一定的 余地,注意出现特殊情况。
五、假氧化物
有些元素和氧的二元化合物,从分子组成上 看是氧化物,但实际并不是氧化物且结构比较复 杂。我们将这类氧化物称做假氧化物。
例如Pb3O4是一种混合价态的化合物。该化 合物是PbO与空气在反射炉中450 ~ 500℃:时作用而得到的,其结构由PbⅣO6八面体(Pb - 0.214 PM)共用对边而成的链组成,这些链由PbⅡ原子 连接起来。
再如Fe3O4,从化学式上看是氧化物,经X射线晶体测定:其组成实际是FeⅢ [FeⅢ FeⅡO4 ]2我 们也将其称为假氧化物。
目前,在中学化学教学中,仍然将Fe3O4称之 为氧化物,并解释说它是由FeO和Fe2O3组成的 具有特殊结构的氧化物,属于纯净物。笔者认为这样做是有一定道理的,它考虑到了中学化学教 学的实际情况和学生的知识水平。如果在中学阶段就告诉学生Fe3O4的实际组成,必将增加学生在认识上的混乱和学习上的负担。
六、过氧化物
这类氧化物,是由于分子中含有过氧基 (-O — O-)或过氧离子(O22-)而得其名。此外具 有极弱酸性的过氧化氢(H2O2)与碱作用,也可生 成过氧化物:
Ba(OH)2 +H2O2=BaO2 + 2H2O 因此,过氧化物也可看作是过氧化氢的盐。
能生成过氧化物的金属,主要是碱金属和碱 土金属。例如Na2O2等。
七、超氧化物
金属性特别活泼的碱金属和碱土金属,在一 定条件下,在过量的氧气中燃烧时,可生成比过氧 化物含氧量更高的氧化物。例如KO2、 NaO2等, 我们称之为超氧化物。另外,超氧化氢(HO2)也 属于超氧化物。
超氧化物中的超氧离子(O2-),是O2分子作 为一个整体获得一个电子后形成的,因此稳定性 很差,是很强的氧化剂。
八、臭氧化物
常见的臭氧化物大都是比较活泼的碱金属的氧化物,例如KO3、CsO3等。它们是通过臭氧(O3) 与碱金属氢氧化物反应制备而得其名的。
例如:4KOH + 4O3 ==4KO3 +O2 +2H2O 臭氧离子(O3- )不稳定,常温下即可缓慢分解。
九、类似氧化物
这类化合物象OF2、O2F2等,从它们的分子组 成上看符合氧化物的定义,但是氧元素在分子中 的化合价分别为+2和+ 1价,是电子的提供者而 不是获得者,因而只能称作氟化物而不称作氧化 物。为了说明符合氧化物定义而又不属于氧化物 的现象,我们称这类化合物为类似氧化物。
上述的分类方法,把大多数的常见氧化物基 本上都划分到了合理的类别。当然,这种分类的 方法也并不是十分完善的。例如:它未能包含所 有的氧化物、也不能体现出是离子型还是共价型 等。这些问题,有待与同行们商榷。

- 全部评论(0)
