例谈电池的能量密度
时间:2016-06-04 15:13 来源:未知 作者:罗翊轩 点击: 次 所属专题: 比能量
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
例 [2013 高考新课标 ]二甲醚直接燃料电池具有启动快,效率高等优点,其能量密度高于甲醇直接燃料电池(5.93kw·h·kg-1) 。若电解质为酸性,二甲醚直接燃料电池的负极反应为 ,一个二甲醚分子经过电化学氧化,可以产生 个电子的电量; 该电池的理论输出电压为1.20V,能量密度E= ( 列式计算,能量密度= 电池输出电能/燃料质量,1kw·h=3.6×106J)
本题考查原电池原理$物质的量在化学实验中的应用,切入点新,是化学学科与物理学科的综合,使理综卷产生了理综味,这也是理综考试卷发展的必经之路。
本题电池的能量密度源于化学4 选修课本电池优劣的判断标准之一: 单位质量或者单位体积的电池所储存的能量多少,能量密度即比能量,或输出功率的多少,功率密度即比功率。
在人教版教师教学参考用书里,几乎没有能量密度的更多介绍,教辅资料上几乎不见能量密度的例题和习题。 因此在新课学习或者高考复习时被师生们忽视甚至忽略。
由题给的直接燃料电池的能量密度的计算式和甲醇直接燃料电池的能量密度(5.93kw·h·kg-1) 知,本题二甲醚直接燃料电池的能量密度的计算只要计算出1kg 二甲醚输出的电能即可。
解析: 若电解质为酸性,燃烧产物不被电解质吸收,二甲醚直接燃料电池的负极发生氧化反应,反应为:CH3OCH3+3H2O-12e-=2CO2+12H+
显然,一个二甲醚分子经过电化学氧化,可以产生12 个电子的电量;1kg 二甲醚的物质的量n=1000/46 mol,可以产生1000/46×12×6.02×1023个电子的电量;一个电子的电量是1.6×10-19C
1kg 二甲醚输出的电能:
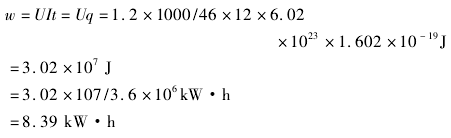
二甲醚直接燃料电池能量密度E=8.39kw·h·kg-1
甲醇直接燃料电池的理论输出电压是多少? 也可以通过列式计算求出来。
若电解质为酸性,甲醇直接燃料电池的负极反应为:CH3OH+H2O-6e-=6CO2+6H+
一个甲醇分子经过电化学氧化,可以产生 6个电子的电量。
1kg 甲醇的物质的量1000/32mol,可以产生的1000/32×12×6.02×1023个电子的电量;一个电子的电量是 1.6×10-19C
1kg 甲醇输出的电能:
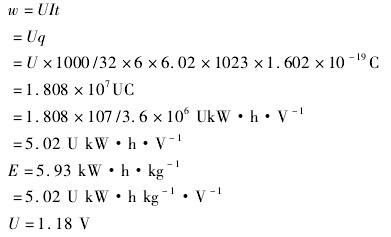
若电解质为碱性,甲醇直接燃料电池的负极反应为:CH3OH+8OH--6e-=CO32-+6H2O
同样可以算出理论输出电压是1.18V。
P=W/T,功率可以由电池输出的电能换算得到,会算比能量,比功率也不难。

- 全部评论(0)
