四氧化三铁为啥属于盐?
时间:2019-04-06 16:58 来源:未知 作者:赵宝 点击: 次 所属专题: 四氧化三铁
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
什么是氧化物?
两种元素组成的化合物,一种是氧,叫做氧化物。当然,总有例外。
氧化物中的氧多数都是-2价,例如H2O,CO2
少数为-1价,例如H2O2过氧化氢,Na2O2过氧化钠
更少数为-1/2价,例如K2O,读作超氧化钾
这一步一步的,氧在氧化物中的化合价逐渐升高,会不会升高到正价呢?那需要一个比氧更能夺电子的元素。整个元素周期表中得电子能力最强(电负性)的是氟(F),故OF2(二氟化氧)中氧为+2价。此时我们不叫它氧化物,而叫氟化物。
对于下文中讲到的四氧化三铁,(包括四氧化铁)结构与普通氧化物不同,故分类为“复杂氧化物”,他们的结构与普通氧化物有很大不同。我个人认为,所谓复杂氧化物,即指:在氧化物中,氧原子的成键方式不止一种。(个人观点)
铁的氧化物有哪些?
列出铁的氧化物,以正视听(释义:保证事实被正确理解)。
化学式 | Fe价 | 化学名称 | 备注 |
FeO | +2 | 氧化亚铁 | 中学不学 |
Fe2O3 | +3 | 氧化铁 | |
Fe3O4 | ★ | 四氧化三铁 | |
FeO2 | +4 | 二氧化铁 | 中学不学 |
FeO3 | +6 | 三氧化铁 | 中学不学 |
FeO4 | +6 | 四氧化铁 | 中学不学 |
上表Fe元素的价态我都标了出来,其中Fe3O4的价态是★,比较复杂,容我慢慢说。对于上表,你会说:二氧化铁,三氧化铁,四氧化铁是什么鬼!氧化亚铁也许还有人见过,后三种绝没见过。但它确实存在,中学不学它,看看就行了,不需重视。
FeO4中的Fe也许有人以为我写错了,其实没错,不是+8,就是+6。
Fe3O4中铁的价态为什么复杂?
我们来算算,氧是-2价,四个氧,-8价,那Fe就是+8价。+8价分给三个Fe原子,每个Fe原子的价态就是+8/3价。“正三分之八价!”化合价代表得失电子的数目,不可能得三分之八个电子。我们管这种“经过化学式,演算推倒出来的化合价”叫做表观化合价。而实际上,这里的情况是什么呢,我们来看看三种氧化物与酸的反应。
反应原理:金属氧化物 + 酸 → 盐 + 水,反应前后金属的价态不变。
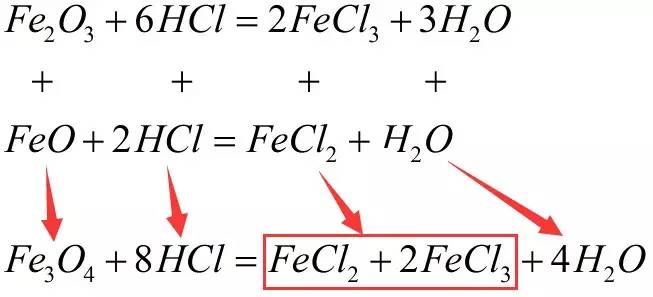
我们会发现,四氧化三铁的反应,可以看做是前反应的加和,所以在结构上我们暂且认为:Fe3O4 = Fe2O3 + FeO(这种认识方法并不严密,但暂且可以这么认为)。一个Fe3O4分子中的三个铁原子,两个显+3价,一个显+3价。
在一个化合物中,一种元素只有一种化合价,这个看似正确的说法,自从我们见到硝酸铵(NH4NO3)后就颠覆了(NH4NO3中第一个n(为)-3价,第二个n(为)+5价)。今天我们又学了四氧化三铁中的三个铁原子,分别显示+2和+3两种价态。
其实,上文说的FeO4也是个说明这个问题的好例子。四氧化铁中Fe为什么是+6不是+8,是因为这四个氧中,有三个氧是-2价,一个氧是0价。化合物中还会有零价的元素?会!!!!
Fe3O4具有怎样的结构?
要回答这个问题,回忆下高中化学必修一,第三章“金属及其化合物”中讲到了氢氧化铝是两性氢氧化物。
氢氧化铝在水中发生两种电离:
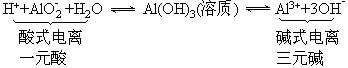
一方面,氢氧化铝可以电离出氢离子和氢氧根离子:
![]()
另一方面,氢氧化铝可以电离出氢离子和铝酸根离子:
![]()
能电离出氢离子和酸根离子,所以氢氧化铝我们也可以看做是酸:铝酸(H3AlO3)。
铝酸易失去一分子水,变为偏铝酸:
![]()
偏铝酸是弱酸,在水溶液中也会部分电离:
![]()
以上是高一课本内容,由以上内容我们来照葫芦画瓢:
氢氧化铁是两性氢氧化物,在水中发生两种电离:电离出铁离子和氢氧根离子,电离出氢离子和铁酸根离子。
铁酸易失去一份子水,变为偏铁酸。
偏铁酸可电离,电离出偏铁酸根离子。
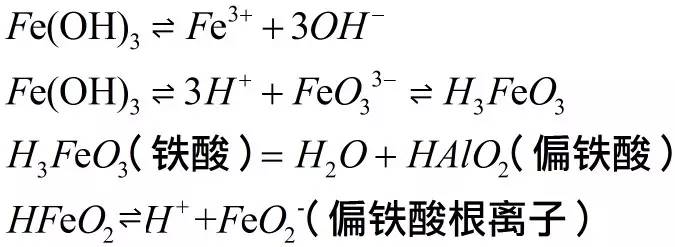
好了。偏铁酸根是个阴离子,它可以和阳离子构成盐。如果这个阳离子是+2价的亚铁离子,那么构成的盐就是:
![]()
由于是亚铁离子和偏铁酸根离子构成的盐,读作:偏铁酸亚铁
数数这个偏铁酸亚铁的组成原子,三个Fe,四个O,刚好:Fe3O4!!!
事实上,四氧化三铁,人家的真实结构是:偏铁酸亚铁。是一种盐!!!

- 全部评论(0)
(1264369313) 评论 href="/plus/view.php?aid=16236">四氧化三铁为啥属于:这个,,,超氧化钾是KO2而不是K2O
@kjzzz(603521979) 评论 href="/plus/view.php?aid=16236">四氧化三铁为啥属于:氢氧化铁是两性氧化物?
@kjzzz(603521979) 评论 href="/plus/view.php?aid=16236">四氧化三铁为啥属于:氢氧化铁是两性氧化物?
 2595191531@qq.com 评论
href="/plus/view.php?aid=16236">四氧化三铁为啥属于:错了,氢氧化铁不是两性。原理从根本上就错了 管理员回复:
2595191531@qq.com 评论
href="/plus/view.php?aid=16236">四氧化三铁为啥属于:错了,氢氧化铁不是两性。原理从根本上就错了 管理员回复:
