高考化学考试必知的评分细则
时间:2020-03-12 16:51 来源:未知 作者:化学自习室 点击: 次 所属专题: 评分细则
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.化学用语的评分细则:
化学Ⅱ卷50%左右的答案要用化学用语表述,若化学用语使用不过关,且没有引起足够的重视,在高考中失分是显而易见的,如以下情况:
(1)化学方程式、离子方程式,不写反应条件扣一半的分,不配平或产物、反应物的化学式有一处写错不得分,“??”和“===”错用不得分,或增加反应条件,或增加“↑”“↓”等扣1分,化学式错误或化学方程式未配平判零分,“↑”“↓”符号该标出之处漏标酌情扣分。
(2)热化学方程式不注明各物质的聚集状态或焓变数值不注明、计算错误、不带单位、该注明“+”“-”号而漏写均判为零分。
(3)将化学式写成名称、将有机物结构简式写成分子式、将离子方程式写成化学方程式均不得分。
(4)回答不具体:如标准答案是除去水蒸气;除去CO2。评分细则规定:除去、吸收、去掉水蒸气或H2O、CO2给满分或除去CO2及酸性气体给满分,仅答酸性气体不给分。
2.化学简答与计算题评分细则:
(1)简答题出现科学性错误,该空不得分:一个答案,经常有考生由于没有足够的把握,写出一对一错,或二对一错,或一对多错的答案,这种情况多少反映考生抱有某种程度的投机心理,把多个可能的答案全部写出,让评卷教师做出选择。阅卷老师一直坚持凡是出现多个答案情况时,只要有一个是错误的,则毫不留情,给予零分处理。
(2)出现错别字且错别字是关键字该空不得分:如:催化剂~摧化剂、崔化剂;加成反应~加层反应;苯~笨;玻璃棒~玻利棒;电解质~电解子;金刚石~金钢石等等。
(3)简答不全面得一半分。
(4)关于实验设计的简答缺少步骤、现象和结论中的一部分,分步得分。
(5)凡是辨别不清的,皆为“0”分。答题时首先不能过于潦草,而且要十分清晰,易于辨认。有两种情况存在,其一是学生在修改答案时,改动不够坚决和清楚,如由a改成B,由b又改成D,中间修改不清楚,难以辨认,其二是不排除考生有投机心理,让评卷老师去猜。另外有些学生开始答卷(题)时,没有把握,用铅笔答题,最后又没有用0.5 MM黑色签字笔圈定,扫描时图像不够清晰,造成失分。
(6)“白纸黑字”原则:凡是试卷上写了的就有,没有写的就没有,答错位置或答题超出试卷,皆为“0”分。
(7)“见空给分”原则。在连续多个答案中,为了便于操作,通常采用“独立操作,互不牵连”的原则,即前面一个答案的正确与否,不影响后面答案的给分,同理,如前者正确,而后者错误,也按步骤照样给分,虽然此法可能让某些人占了便宜,但也不能冤枉一些人,而且便于操作。
(8)化学计算的表达式错误或计算数据错误不给分,缺少单位扣一半分,不注意有效数字酌情减分。
3.化学评分细则示例
[示例] (13分)CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。
(1)其中一种途径是将CO2转化成有机物实现碳循环。
如2CO2(g)+2H2O(l)===C2H4(g)+3O2(g) ΔH=+1 411.0 kJ·mol-1
2CO2(g)+3H2O(l)===C2H5OH(l)+3O2(g) ΔH=+1 366.8 kJ·mol-1。
则由乙烯水化制乙醇反应的热化学方程式为_____________________________。
(2)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。
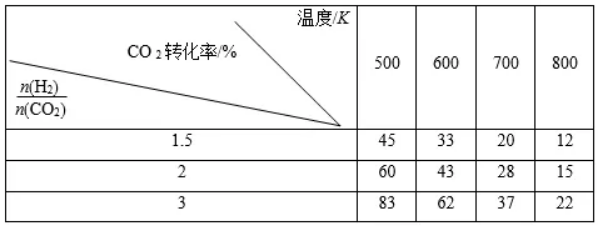
根据上表中数据分析:
①温度一定时,提高氢碳比,CO2的转化率________(填“增大”“减小”或“不变”)。
②该反应的正反应为________(填“吸”或“放”)热反应。
(3)一定条件下,将3mol H2和L mol CO2混合在固定容积为2 L 的密闭容器中,发生如下反应:3H2(g)+CO2(g) CH3OH(g)+H2O(g)。2 min末该反应达到平衡,测得CH3OH的浓度为0.2 mol·L-1。下列判断不正确的是________。
CH3OH(g)+H2O(g)。2 min末该反应达到平衡,测得CH3OH的浓度为0.2 mol·L-1。下列判断不正确的是________。
A.该条件下此反应的化学平衡常数表达式为K=0.91(L/mol)3
B.H2的平均反应速率为0.3 mol·L-1·S-1
C.CO2的转化率为60%
D.若混合气体的密度不再改变时,该反应一定达到平衡状态
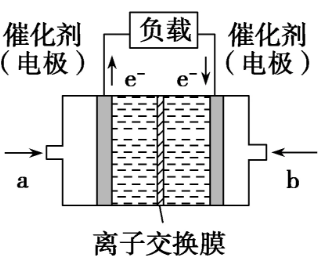
(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是________(填“乙醇”或“氧气”),b处电极上发生的电极反应是_________。
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为_________________________________。
【答案】
(1)C2H4(g)+H2O(l)===C2H5OH(l) ΔH=-44.2 kJ·mol-1(2分)
(2)①增大 ②放(每空各1分)
(3)B,C,D(3分)
(4)乙醇(1分) O2+2H2O+4e-===4OH-(2分)
(5)5·6×10-5mol·L-1(3分)
【评分细则】
(1)漏写状态符号、用错反应热符号、漏写反应热的单位,上述情况有一处出现均不得分。
(2)填错不得分。
(3)每选对一个选项得1分,错选a要从得分中扣1分。
(4)填“C2H5OH”不得分,电极反应式不配平不得分.
写为“O2+2H2O+4e-―→4OH-”也可得2分。
(5)数据错误不得分,漏写单位扣1分。

- 全部评论(0)
