“四大平衡”归纳总结
时间:2021-08-17 11:03 来源:未知 作者:化学自习室 点击: 次 所属专题: 五大平衡
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
高中化学教材中,有一个平衡理论体系,包括溶解平衡、化学平衡、电离平衡、水解平衡、络合平衡等。
化学平衡是这一平衡理论体系的核心。系统掌握反应速率与化学平衡的概念、理论及应用对于深入认识其他平衡,重要的酸、碱、盐的性质和用途,化工生产中适宜条件的选择等,具有承上启下的作用;
对于深入掌握元素化合物的知识,具有理论指导意义。正因为它的重要性,所以,在历年高考中,这一部分向来是考试的热点、难点。
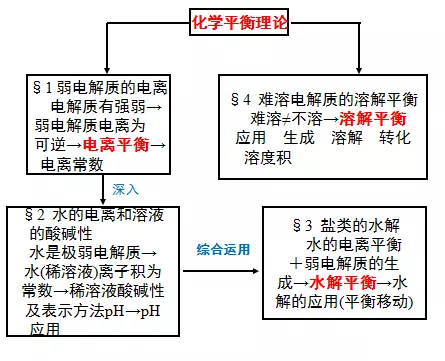
1.高中化学常见四大平衡
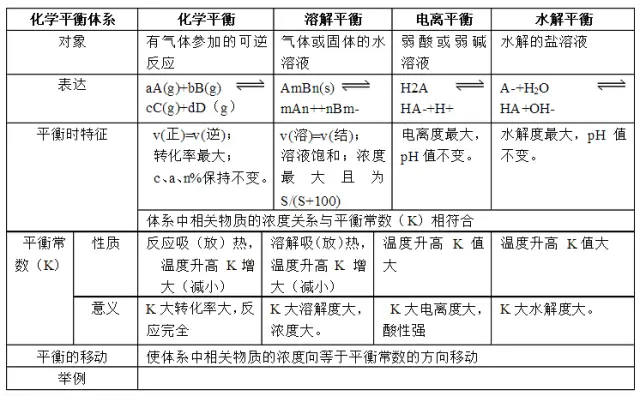
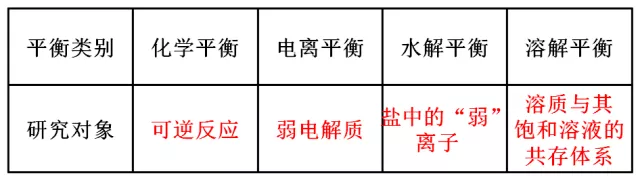
2.常见四大平衡研究对象
模型一、化学平衡
研究对象:可逆反应。如:N2+3H2 2NH3 ;ΔH<0 ,加热不利于氨的生成,增大压强有利于氨的生成。
2NH3 ;ΔH<0 ,加热不利于氨的生成,增大压强有利于氨的生成。
模型二、电离平衡:
研究对象:弱电解质。如:CH3COOH H++CH3COO- ; ΔH>0加热促进电离,稀释电离度增大。
H++CH3COO- ; ΔH>0加热促进电离,稀释电离度增大。
模型三、水解平衡
研究对象:弱酸盐或弱碱盐或弱酸弱碱盐。如:Fe3++3H2O Fe(OH)3+3H+; ΔH>0配制Fe3+溶液应加入少量酸防止Fe3+ 水解。不断加热FeCl3 溶液,蒸干灼烧可得到Fe2O3 固体。
Fe(OH)3+3H+; ΔH>0配制Fe3+溶液应加入少量酸防止Fe3+ 水解。不断加热FeCl3 溶液,蒸干灼烧可得到Fe2O3 固体。
模型四、溶解平衡
研究对象:气体或固体溶于水形成的饱和溶液中形成的平衡体系。
(1)气体的溶解平衡
如:Cl2+H2O H++Cl-+HClO 当加入NaCl、Na2CO3等时平衡会发生移动。当收集Cl2、SO2、CO2、H2S 等气体时往往分别通过饱和的NaCl、NaHSO3、NaHCO3、NaHS等溶液以除去可能有的酸性气体,且抑制气体的溶解。
H++Cl-+HClO 当加入NaCl、Na2CO3等时平衡会发生移动。当收集Cl2、SO2、CO2、H2S 等气体时往往分别通过饱和的NaCl、NaHSO3、NaHCO3、NaHS等溶液以除去可能有的酸性气体,且抑制气体的溶解。
(2)固体的溶解平衡如:
如:NaNO3(s) Na++NO3-;ΔH>0 加热促进溶解;Ca(OH)2(s)
Na++NO3-;ΔH>0 加热促进溶解;Ca(OH)2(s) Ca2++2OH-;ΔH<0加热溶解度降低;MgCO3+H2O=Mg(OH)2+CO2反应的进行是由于MgCO3存在溶解平衡;MgCO3(s)
Ca2++2OH-;ΔH<0加热溶解度降低;MgCO3+H2O=Mg(OH)2+CO2反应的进行是由于MgCO3存在溶解平衡;MgCO3(s) Mg2+(aq)+CO32-(aq);由于CO32- 能水解,加热时CO32-的水解程度增大,促进了MgCO3的溶解,最终MgCO3 转化成Mg(OH)2。
Mg2+(aq)+CO32-(aq);由于CO32- 能水解,加热时CO32-的水解程度增大,促进了MgCO3的溶解,最终MgCO3 转化成Mg(OH)2。
3、知识结构
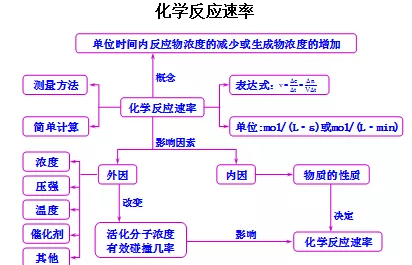
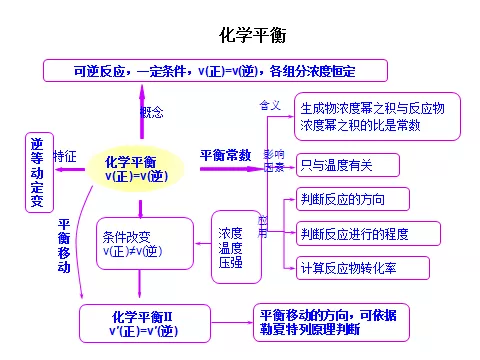
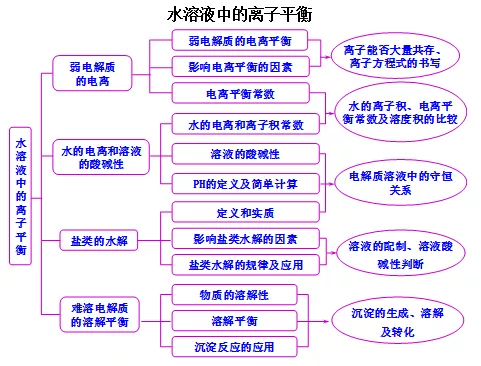
4、归纳总结
四大平衡无论是理论学习还是解题方法,都有许多的共通之处。归纳总结四大平衡的共同点是一种有效的复习方法。

1. 所有的平衡都建立在“可逆反应”的基础上
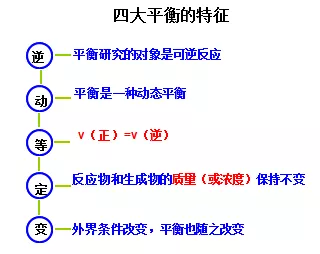
2.平衡特征相同
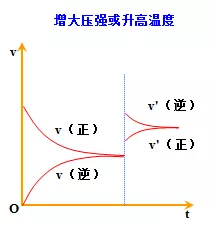
3.都可借助v-t图学习平衡的建立及平衡的移动
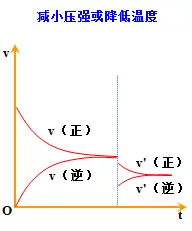
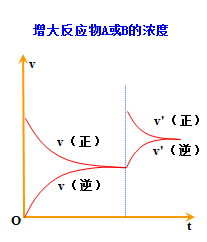
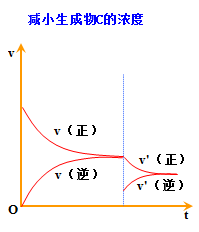
4. 都能用勒夏特列原理解释平衡的移动
勒夏特列原理:如果改变影响平衡的一个条件(如温度、浓度、压强等),平衡就向减弱这个改变的方向移动.
平衡的实质是两个变化方向的速率相等,所以影响平衡的因素首先是影响速率的因素:
(1)温度:升温促进吸热过程进行

(2)浓度:增大某物质浓度,平衡向消耗该物质的方向移动
(3)减压或稀释
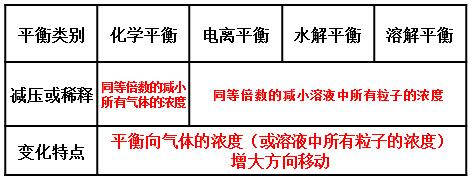
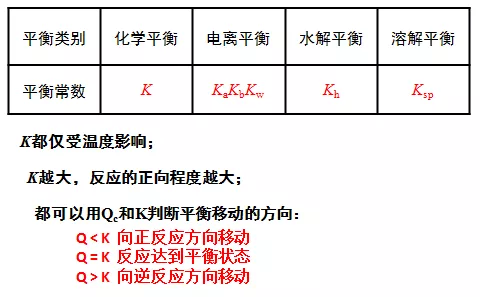
5. 都存在平衡常数K

- 全部评论(0)
