工业制硫酸
时间:2026-03-17 17:42 来源:未知 作者:化学自习室 点击: 次 所属专题: 硫酸工业
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
硫酸是“化工之母”,工业上主要采用接触法生产。该方法的核心在于通过催化剂使SO2反应生成SO3再用水吸收。整个生产流程主要分为三阶段:造气、催化氧化、吸收。
一、三步流程详解
工业制硫酸通常以硫黄(s)或黄铁矿(FeS2)为原料。目前,以硫黄为原料因流程简单、污染小而成为主流趋势 。
第一步:造气(沸腾炉)
目的:制取SO2设备:沸腾炉(或焚烧炉)
硫黄法:直接焚烧硫黄。
S+O2 SO2
SO2
黄铁矿法:高温煅烧黄铁矿。
4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
考点提示:矿石进厂需粉碎(增大接触面积,加快反应速率);矿渣(Fe2O3)可用于炼铁,实现资源综合利用 。
第二步:接触氧化(接触室)
目的:将SO2化氧化为SO3核心步骤)
设备:接触室(内装热交换器和催化剂层)
2SO2+O2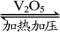 2SO3
2SO3
工艺条件的选择(高频考点):
条件 | 选择原因 | 备注 |
|---|---|---|
温度 | 400-500℃ | 综合考虑反应速率和催化剂活性,并非温度越低越好 。 |
压强 | 常压 | 加压虽能提高转化率,但效果不显著,且会增加设备成本 。 |
催化剂 | 五氧化二钒 | 不能提高平衡转化率 ,只能加快反应速率。 |
拓展知识:热交换器
接触室中安装热交换器,利用反应放出的热量预热进入的冷气体,既节约能源,又控制反应温度 。
第三步:吸收(吸收塔)
目的:将SO3化为H2SO4设备:吸收塔
SO3+H2O=H2SO4
核心考点:工业上不能直接用水吸收SO3
因为直接用水会产生大量酸雾,导致吸收效率极低 。
正确做法:用98.3%的浓硫酸吸收 SO3得到发烟硫酸或再稀释成商品硫酸 。

二、尾气处理与环境保护
工业尾气中含有少量 SO2必须回收利用,防止污染。
常用方法:氨吸收法
SO2+2NH3+H2O=(NH4)2SO3(或NH4HSO3)
生成的亚硫酸铵可用于制取氮肥,实现变废为宝。
三、历史小知识:铅室法
在接触法普及之前,硫酸曾通过铅室法生产。该方法利用氮氧化物作为氧的载体,在铅制反应室中使SO2氧化。但它只能生产稀硫酸(约65%),且杂质多、设备庞大,因此已被淘汰 。

- 全部评论(0)
