乙炔的实验室制法
时间:2017-05-26 11:05 来源:未知 作者:向小平 点击: 次 所属专题: 乙炔
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
反应原理:CaC2+2H2O→C2H2↑+Ca(OH)2
发生装置:使用“固+液→气”的制取装置。
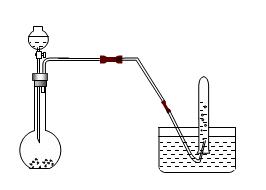
收集方法:排水集气法。
注意:
1、实验中常用饱和食盐水代替水,目的是得到平稳的乙炔气流。
2、制取时,应在导气管口附近塞入少量棉花的目的是,为防止产生的泡沫涌入导管。
3、用电石和水反应制取的乙炔,常闻到有恶臭气味,是因为在电石中含有少量硫化钙、磷化钙等杂质,跟水作用时生成H2S、PH3等气体有特殊的气味所致。
电石是固体,水是液体,且二者很易发生反应生成C2H2气体。很显然C2H2的生成符合固、液,且不加热制气体型的特点,那是不是说就可以用启普发生器或简易的启普发生器来制取乙炔呢?
答案是否定的。实验室中不可用启普发生器或具有启普发生器原理的实验装置作制备乙炔气体的实验装置。主要原因是:
1、反应剧烈,难以控制。
2、当关闭启普发生器导气管上的活塞使液态水和电石固体分离后,电石与水蒸气的反应还在进行,不能达到“关之即停”的目的。
3、反应放出大量的热,启普发生器是厚玻璃仪器,容易因受热不均而炸裂。
4、生成物Ca(OH)2微溶于水,易形成糊状泡沫,堵塞导气管与球形漏斗。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
(2144930686) 评论 href="/plus/view.php?aid=16373">乙炔的实验室制法:有用,真的有用。
(1845621080) 评论 href="/plus/view.php?aid=16373">乙炔的实验室制法:有用,有大用。
还没有评论,快来抢沙发吧!
