制作快速发热的“保温袋”
时间:2022-08-01 17:37 来源:未知 作者:彭琳 点击:次 所属专题: 金属铁 化学暖袋
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
实验目的
利用铁与空气中的氧气发生化学变化,产生热量,制作成快速发热的“保温袋”。
器材与用品
保鲜袋 烧杯(或玻璃杯) 药匙 布袋 还原性铁粉 食盐 水
实验步骤
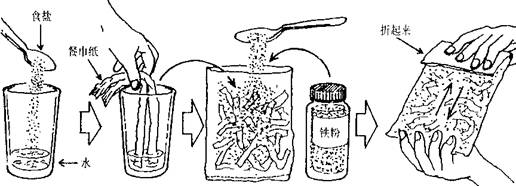
1. 向大玻璃杯中加入大约一小杯的水,再加入水量一半的食盐,然后,取2~3张餐巾纸拧紧成卷,把它们轻轻放入水中,浸湿。
2. 打开并摊开餐巾纸,把它们放入保鲜袋中,再把2~3匙的铁粉均匀地撒在餐巾纸上。
3. 折起保鲜袋的袋口,抓住保鲜袋的两端,摇晃,使铁粉粘在浸湿了的餐巾纸上。
4. 当温度还没有上升到很高时,打开保鲜袋,让空气进入袋中,封好袋口,外面再加一层布袋,就制成了快速发热的“保温袋”。
实验原理
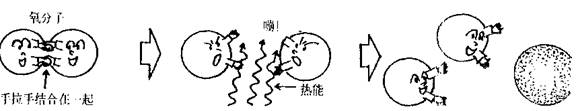
1. 空气中的氧分子是有两个氧原子结合在一起的。
2. 如果氧原子从外部吸收能量后,氧原子之间的结合就会破坏,氧分子变为更活泼的氧原子。
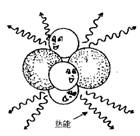
3. 如果附近有铁原子,氧原子就会马上与铁原子化合,3个氧原子与2个铁原子结合,变成了三氧化二铁,铁与氧的结合力很强,生成的三氧化二铁也处于很稳定的状态,这样,结合时多余的能量就变成了热能,向外放出。
![]()
注意事项
要注意安全,防止灼伤。
问题与讨论
1. 怎样才能延长发热时间?
2. 制作的保温袋有哪些用途?
3. 为了制得有较高温度的“保温袋”,如何调节水、食盐、铁粉的比例?
参考资料
1. 如果加入一些活性炭、细木屑,铁将会发生原电池反应,铁为负极,炭为正极。
2. 铁与氧气再高温下燃烧,生成四氧化三铁,但在常温下,也发生氧化反应,最终变为红色的三氧化铁,可能含有部分水。
(责任编辑:)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
