磷的同素异形体
时间:2021-11-09 17:16 来源:未知 作者:黄勇 点击: 次 所属专题: 磷单质
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
磷的同素异形体主要有三种:白磷、红磷、黑磷。
纯的白磷是无色透明的晶体,遇光即逐渐变为黄色,所以又叫黄磷。黄磷在隔绝光和空气的情况下蒸馏,又可变白色。经测定,无论在溶液中或在蒸气状态下,白磷都以P4的分子形式存在。
4个磷原子构成四面体,每一个磷原子用它的3个p轨道与另外3个磷原子的P轨道形成3个б键,P4分子中磷原子之间的键角是60°。P4分子是有张力的分子,这个张力使每一个P—P键的键能降低,这说明了为什么白磷在常温下有很高的化学活动性。
将白磷蒸气加热到800℃,P4开始分解为P2,这时的双原子分子结构跟氮分子相似(∶P≡P∶)。
白磷在密闭容器里加热到260℃,就会逐渐转化为暗红色粉末。常温时,在光的作用下,白磷也会发生上述的转化,生成的暗红色的变体,其中主要成分是紫磷。紫磷的化学活动性比白磷小,但仍能被硝酸氧化成磷酸。紫磷跟氯酸钾一起摩擦可以猛烈燃烧。
白磷或紫磷跟三溴化磷煮沸,都会生成红磷。红磷是紫磷的无定形体。
红磷的结构至今仍未弄清楚。有人认为红磷是四面体结构的P4分子断裂开1个键之后,连接起来形成的长链状巨大分子。
将白磷在1.21×109Pa下加热,就得到黑磷。黑磷呈铁灰色,具有金属光泽,能导电,密度为2.7g/cm3,着火点是490℃,外形像石墨。黑磷的化学活动性比紫磷差,通常难于发生化学反应。
黑磷具有双层结构,每个磷原子有3个相邻的原子。
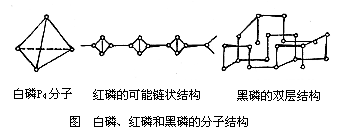
白磷、红磷和黑磷的分子结构如图。
许多元素的单质像磷那样会形成同素异形体。形成同素异形体有下列三种方式:(1)组成分子的原子数目不同,如氧气(O2)和臭氧(O3);(2)晶体里原子的排列方式不同,如金刚石和石墨;(3)晶体里分子的排列方式不同。如斜方硫和单斜硫。
(责任编辑:)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
