硫酸和硝酸的工业制取中的放热与对流
时间:2026-03-19 22:27 来源:未知 作者:郝凯军 点击: 次 所属专题: 硫酸工业 硝酸工业
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一.硫酸的工业制法
工业上制硫酸涉及三个主要反应。如果矿产是硫磺,先将硫灼烧成SO2。我国的含硫矿主要是硫铁矿(黄铁矿,主要成分是FeS2),首先将矿石粉碎后煅烧:
4FeS2+11O2 2Fe2O3+8SO2↑
2Fe2O3+8SO2↑
SO2在催化剂V2O5帮助下进一步被氧化为SO3:
2SO2+O2 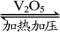 2SO3
2SO3
最后用相当浓度的硫酸吸收SO3生成更浓硫酸或发烟硫酸:
SO3+H2O→H2SO4
注意两个要点。
1.以上三步反应不是氧化就是化合,均为放热反应,故硫酸制造业中除矿物预备和空气预热外,不需要消耗更多的能源。
2.三个相应设备均采用了“对流”原理。
煅烧硫铁矿的设备叫沸腾炉。粉碎的矿石从上方投入,一定压力的空气从炉底鼓进。反应中矿石在炉中翻腾。
为什么要沸腾?即使厨房炒瓜子也需要翻炒,否则焦的焦生的还是生。凭什么沸腾?1,粉碎,矿石一块块脸盆大沸什么腾;2,反应放热,没有高温沸什么腾;3,对流,没有空气往上鼓(风压)沸什么腾?
SO2催化氧化用的第二个设备是带热交换器的接触室。SO2和O2先进入热交换器的外管接受预热,再进入内管接触催化剂并反应。
为什么要热交换?放热反应也需要引发,且充分利用热能。同时,该反应可逆,从平衡移动角度观察,过高温度不利于SO2的转化。凭什么热交换?1,反应本身放热,有热可换;2,对流,外管与内管的气流是反向的。
SO3被吸收为H2SO4的第三个设备叫吸收塔,也采取了对流措施,吸收剂自上往下喷淋,被吸收的SO3自塔底进入。用水吸收SO3会起“雾”,为什么起雾?至少与该化合反应放热有直接关系。所以改水为高沸点的浓硫酸。
三个设备都对流,纯属巧合?其实有其必然。高炉炼铁与沸腾炉一样,也是矿物向下空气向上的。实验室用的冷凝管与热交换器类似,也是内外管冷热对流的。对流效果就是比顺流好。
二.硝酸的工业制法
工业上制硝酸也是三个主要步骤,三个反应也都是放热反应(前两步都是被氧气氧化)。第一步是原料NH3在催化剂存在条件下由空气中的氧氧化成NO:
4NH3+5O2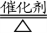 4NO+6H2O
4NO+6H2O
相应设备叫氧化炉,也接触催化剂,也可以采用热交换的方式对原料进行预热。
为什么第一步不直接将NH3氧化成NO2呢?常温下NO极易被氧化成NO2(以至于NO只能用排水法而不能用排空气法收集):
2NO+O2→2NO2
而该氧化反应放热,高温下不利于化合却有利于分解,所以等NO冷却后再用空气将其氧化。
最后在吸收塔内将NO2用水吸收,2/3溶解成为HNO3,1/3又变成NO:
3NO2+H2O→2HNO3+NO
在吸收的同时不断补充空气,NO又被氧化,再吸收,最后全部变成HNO3。
三.两酸对照
可以将两种重要强酸的工业制法作一个联系比较。除“都三步”、“都放热”、“都可对流”外,还有什么共同点?
都有一步氧化需要使用催化剂,一是SO2的催化氧化,一是NH3的催化氧化。需要催化剂帮忙的步骤往往是比较困难的一步,否则,硫就可以被直接氧化成SO3了。
如果尾气处理不当,两家工厂对环境造成的污染都是酸污染,硫氧化物和氮氧化物正是当今大气污染的罪魁祸首,都需要碱性物质将其吸收。如:
SO2+2NH3H2O→(NH4)2SO3+H2O
NO+NO2+2NaOH→2NaNO2+H2O
最后一步都在吸收塔内进行。重要的区别是:SO3是H2SO4的酸酐,NO2却不是HNO3的酸酐,所以两种吸收塔内发生的吸收反应前者是非氧化还原反应,后者则是氧化还原反应,需要补充空气。

- 全部评论(0)
