金刚石的晶胞分析
时间:2015-05-29 21:27 来源:未知 作者:何清松 点击: 次 所属专题: 金刚石晶胞
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
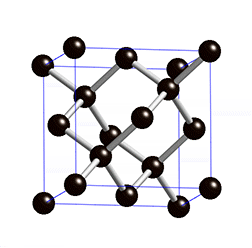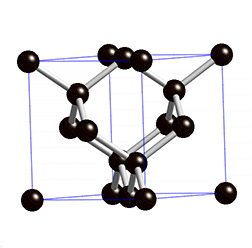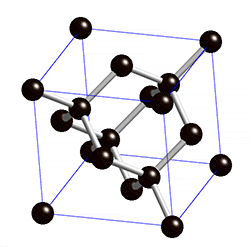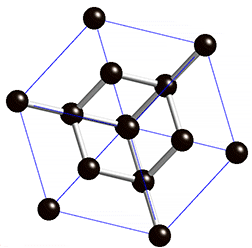
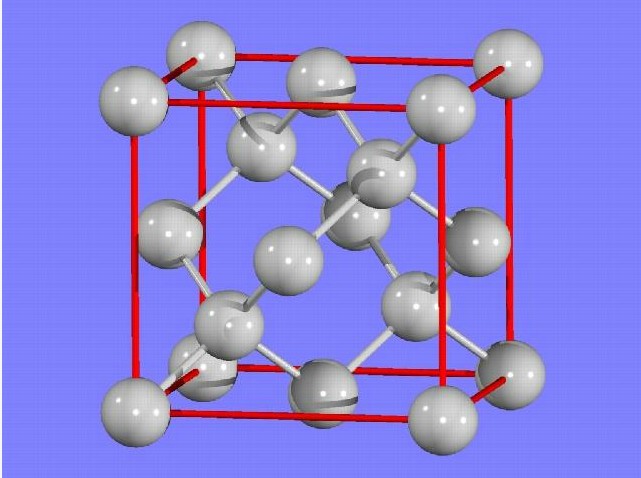
金刚石晶胞:面心立方结构,共有8粒碳原子,分别位于八个角,每角位占1/8粒,六个面心,每面占1/2粒,其余四整粒处于角原子及近邻面心原子间(底部对角两粒,顶部对角两粒),与旁边的四粒碳原子以共价键结合,组成了四个四面体。
金刚石属于面心立方晶胞,即C原子处在立方体的8个定点、6个面心,此外在晶胞中间会出现8个小立方体,其中交错的4个的体心也有C原子,所以一共是8+6+4=18个,但是,定点和面心的C原子实际上是与其它晶胞共用的,所以在实际计算时需要进行折算,定点是1/8,面心是1/2
所以,晶胞中实际含有的C原子数是=8*1/8+6*1/2+4=8个
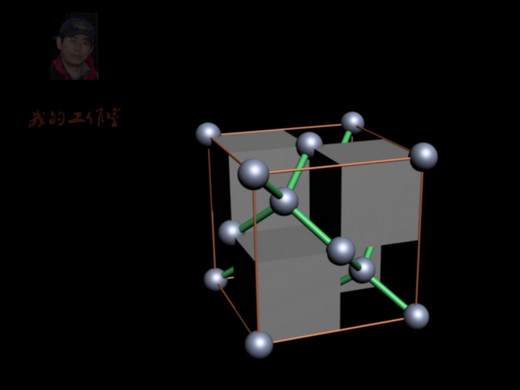
在学习中同学很难把晶胞和金刚石的网状结构联系起来,在晶胞去掉顶角上四个碳原子后,经旋转能清晰看出金刚石中碳原子的相互结合的空间位置关系,如仔细观看最后一帧定格画面,把顶角上的四个碳原子去掉,即可清晰看出金刚烷的结构特征。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
(1343435) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:支持作者啊,rz
(95762645) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:打赏一元就能看吗?
(1347655093) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:有人注意到图三左上角的人头吗
(1347655093) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:有人注意到图三左上角的人头吗
(1810091697) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:小学生不要看高中知识,看不懂的
(3682399) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:不会i家北滨河公园
(6652687) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:感谢个屁让你掏钱
(12345678) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:感谢个屁让你掏钱
(394257539) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:666赞同,本来就不应该付钱
(394257539) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:666赞同,本来就不应该付钱
(354063289) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:为什么要付钱给我一个理由
(354063289) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:为什么要付钱
(2759434575) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:66666,感谢
(1325863256) 评论 href="/plus/view.php?aid=13969">金刚石的晶胞分析:眉毛噢噢噢
还没有评论,快来抢沙发吧!
