化学式改写应用于明矾的计算
时间:2016-03-22 10:16 来源:未知 作者:吴琼 点击: 次 所属专题: 化学式组成计算 明矾
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、向含1mol KAl(SO4)2的溶液中逐滴滴加Ba(OH)2溶液,产生沉淀的物质的量变化的图象分析
KAl(SO4)2中逐滴滴加Ba(OH)2溶液,沉淀的物质的量是先增加后减少至恒定不变。
变形法:KAl(SO4)2变形为K2SO4·Al2(SO4)3
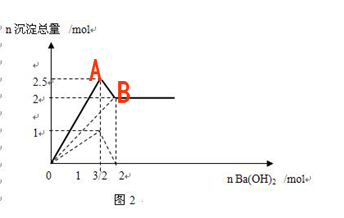
OA段:本质上是Al2(SO4)3+3Ba(OH)2=3BaSO4↓
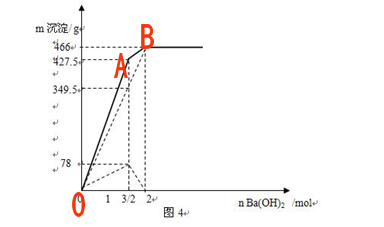
二、向含1mol KAl(SO4)2的溶液中逐滴滴加Ba(OH)2溶液,产生沉淀的质量变化的图象分析
由图可以看出向KAl(SO4)2中逐滴滴加Ba(OH)2溶液,沉淀的质量变化是持续增加至最大量后恒定不变。
三、
向100mL
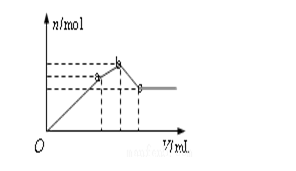
A.A点的沉淀总物质的量为0.03mol
B.OA段发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-=
C.AB段发生反应的离子方程式是:2NH4++SO42-+Ba2++2OH-=2NH3·H2O+
D.反应到C点时,加入Ba(OH)2溶液的总体积为250mL
【解析】变形法NH4Al(SO4)2变形为(NH4)2SO4·Al2(SO4)3
OA段发生反应:Al2(SO4)3+3Ba(OH)2=3BaSO4↓+2Al(OH)3↓;
AB段发生反应:(NH4)2SO4+Ba(OH)2=BaSO4↓+NH3·H2O,
BC段发生反应:Ba(OH)2+2Al(OH)3
反应到C点时,加入的Ba(OH)2反应变为BaSO4、
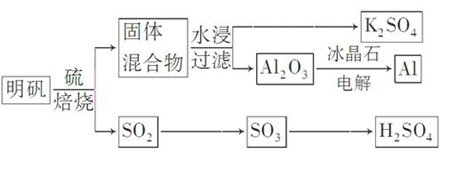
焙烧明矾的化学方程式为:
先将KAl(SO4)2·12H2O变形K2SO4·Al2(SO4)3·24H2O
观察焙烧产物为K2SO4、Al2O3、SO2
可认为是2Al2(SO4)3+3S=2Al2O3+9SO2↑
也就是2[K2SO4·Al2(SO4)3·24H2O]+3S=焙烧=2K2SO4+2Al2O3+9SO2↑+48H2O
即:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
四、若加入NaOH溶液,代替氢氧化钡。
OH-能与NH4+和Al3+作用,但由于
即碱性NaOH>NH3•H2O>Al(OH)3,
则先发生反应的是Al3+与OH-,最后Al(OH)3
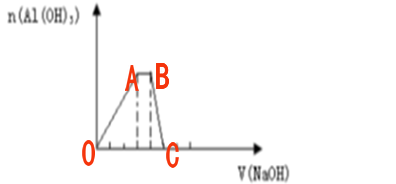
离子方程式为:
OA段:Al3++3OH-=Al(OH)3↓;
AB段:NH4++OH-=NH3↑+H2O;
BC段:Al(OH)3+OH-=AlO2-+2H2O(或Al(OH)3+OH-=[Al(OH)4]-).
【高频出现的方程式】
硫酸铝钾过量:2KAl(SO4)2
硫酸铝钾少量:KAl(SO4)2
反应物1:1
也就是产物有Al(OH)3、

- 全部评论(0)
