如何定量判断盐能否发生彻底水解?
时间:2016-04-22 22:57 来源:未知 作者:熊振典 点击: 次 所属专题: 双水解反应
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
对于CH3COONH4、NH4F等弱酸弱碱盐,它们的阴、阳离子都会发生水解导致水解相互促进。一般情况下,如CH3COONa、NH4F的水解程度虽然较大,但其溶液中主要还是以盐的形式存在,水解未进行彻底。
对于Al2S3、(NH4)2S等弱酸弱碱盐,它们的阴、阳离子都会发生水解,而且水解 的产物是易挥发的气体或沉淀,导致产物脱离平衡体系,平衡向水解的方向移动,从 而使水解进行得很完全,如Al2S3在水中可完全水解,(NH4)2CO3水解度高达 90%。这些物质不能存在于水溶液中。
高中化学中常见的水解能进行完全的离子对有:Al3+与HCO3-、CO32-、HS-、S2-、AlO2-,Fe3+与 HCO3-、CO32-、ClO-、AlO2-,NH4+ 与ClO-、AlO2-等。以上离子对水解相互促进,且进行较为彻底,因而不能大量共存。
(1) 对于弱酸强碱盐NaA来说,只有A-离子水解,其水解常数Kh为:
A-+H2O HA+OH-
HA+OH-
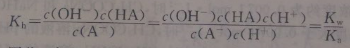
因此,对于一元弱酸强碱盐来说,水解常数的大小取决于Ka,Ka越小则Kh越大,这也就是常说的“越弱越水解”。
(2) 对于一元弱酸弱碱盐来说,阴阳离子都发生水解,其水解常数Kh为:
A-+B++H2O HA+BOH
HA+BOH
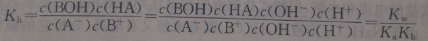
在一定条件下,某可逆反应的K值越大,说明平衡体系中生成物所占的比例越大,它的正反应进行的程度越大,即该反应进行得越完全,反应物转化率越大;反之, 反应就越不完全,转化率就越小。
当K>105时,该反应就能基本进行完全,一般看作非可逆反应;而K在0. 1〜10之间的反应则是典型的可逆反应。
(注:K值大小只能用来判断某可逆反应向某方向进行的最大限度,但不能用来 判断反应达到平衡所需要的时间)
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
