氨基酸的结构与酸碱性质
时间:2019-11-13 10:16 来源:未知 作者:化学自习室 点击: 次 所属专题: 氨基酸
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
氨基酸通常依据氨基离羟基的远近的碳位分类,如α—氨基酸、β—氨基酸等。氨基酸是构成蛋白质的基石,天然蛋白质水解 都得α—氨基酸。了解氨基酸结构与性质有重要意义。
(1)结构:偶极离子(Dipolarion)形式
过去曾长期认为,氨基酸在晶体甚至水溶液中都是以不离解 的中性分子形式![]() 存在的。后来,发现氨基酸晶体的熔点很高,一般都在200℃以上。此外,还发现氨 基酸使水的介电常数(dielectric constant)增高,而一般的有机物如乙醇、丙酮等却使水的介电常数降低。在20℃时,水的介电常数为80,而1 mol/L α—氨基酸水溶液介电常数为102〜108。如果氨基酸在晶体或水溶液中以偶极离子(又称兼性离子 (Zwitterion))形式存在,就能解释上述性质。
存在的。后来,发现氨基酸晶体的熔点很高,一般都在200℃以上。此外,还发现氨 基酸使水的介电常数(dielectric constant)增高,而一般的有机物如乙醇、丙酮等却使水的介电常数降低。在20℃时,水的介电常数为80,而1 mol/L α—氨基酸水溶液介电常数为102〜108。如果氨基酸在晶体或水溶液中以偶极离子(又称兼性离子 (Zwitterion))形式存在,就能解释上述性质。
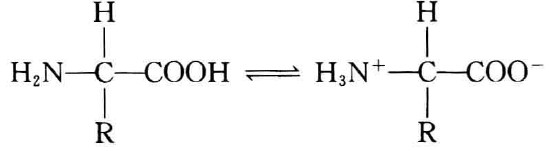
也就是说,氨基酸晶体是以离子晶格形式存在的,质点的作用力是强大的异性电荷之间的静电作用力,像氯化钠一样,所以熔点高。而一般的有机物晶体由分子晶格组成,分子质点间系范德华力(Vander Waals Force)作用,这种力较静电作用要弱得多, 所以它们的熔点低。介电常数与分子极性有关,极性分子的介电常数高。显然,偶极离子形式的氨基酸是强极性分子,自然增大了水的介电常数。氨基酸的偶极离子形式为人们所接受。
(2)氨基酸的两性电离


所以完全质子化的氨基酸可视为多元酸,如果侧链R不离解,可视为二元酸。因此,氨基酸是一类两性电解质。氨基酸主要以偶极离子形式存在时溶液的pH值称为等电点(Isoelectric Point缩写为PI)。
(2) 化学性质(典型的两性物质)
①碱性(氨基)——与酸反应成盐(盐有酸性)
H2NCH2COOH+HCl ClH3NCH2COOH
ClH3NCH2COOH
②酸性(羧基)——与碱反应成盐(盐有碱性)
C6H5CH2CH(NH2)COOH+NaOH C6H5CH2CH (NH2) COONa+H2O
C6H5CH2CH (NH2) COONa+H2O
③缩合或缩聚:分子间缩合成肽键
酶作催化剂
H2N—CH (R)—COOH+H2N—CH (R')—COOH  H2N—CH(R)—CONH—CH(R')一COOH+H2O
H2N—CH(R)—CONH—CH(R')一COOH+H2O
④酯化反应
盐酸作催化剂
H2NCH2COOH+CH3CH2OH  H2NCH2COOCH2CH3+H2O (甘氨酸乙酯)
H2NCH2COOCH2CH3+H2O (甘氨酸乙酯)
(3) 中学要求掌握的α—氨基酸
①甘氨酸
又叫做氨基乙酸,是最简单的氨基酸。结构简式: H2NCH2COOH。常温下是无色有甜味的晶体,易溶于水,水溶液 显酸性。熔点233℃(分解)。甘氨酸乙酯用作食品或饲料添加剂。
②丙氨酸
又叫做α—氨基丙酸。结构简式:CH3CH(NH2)CO〇H。有甜味,溶于水,微溶于醇。熔点297℃。
③苯丙氨酸
又叫做α—氨基一β—苯基丙酸。结构简式:C6H5CH2CH (NH2)COOH。溶于水,不溶于乙醇。熔点284℃。
④谷氨酸
又叫做α—氨基戊二酸。结构简式:HOOCCH2CH2CH(NH2) COOH。溶于热水,微溶于冷水,不溶于醇醚酮。200℃升华。
味精——含结晶水的谷氨酸的一钠盐
HOOCCH2CH2CH (NH2 )COOH+NaOH HOOCCH2CH2CH (NH2 )COONa • H2O
HOOCCH2CH2CH (NH2 )COONa • H2O

- 全部评论(0)
