有机化学计算题类型与思路
时间:2020-02-16 15:07 来源:未知 作者:化学自习室 点击: 次 所属专题: 有机化学计算
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1、有机物化学式的确定
(1)确定有机物的式量的方法
①根据标准状况下气体的密度ρ,求算该气体的式量:M= 22.4ρ(标准状况)
②根据气体A对气体B的相对密度D,求算气体A的式量:MA=DMB
③求混合物的平均式量:M=m(混总)/n(混总)
④根据化学反应方程式计算烃的式量。
⑤应用原子个数较少的元素的质量分数,在假设它们的个数为1、2、3时,求出式量。
(2)确定化学式的方法
①根据式量和最简式确定有机物的分子式。
②根据式量,计算一个分子中各元素的原子个数,确定有机物的分子式。
③当能够确定有机物的类别时。可以根据有机物的通式,求算n值,确定分子式。
④根据混合物的平均式量,推算混合物中有机物的分子式。
(3)确定有机物化学式的一般途径

(4)有关烃的混合物计算的几条规律
①若平均式量小于26,则一定有CH4
②平均分子组成中,l< n(C)< 2,则一定有CH4。
③平均分子组成中,2< n(H)< 4,则一定有C2H2。
2、有机物燃烧规律及其运用


(1)物质的量一定的有机物燃烧
规律一:等物质的量的烃CnHm和Cn-mH5m,完全燃烧耗氧量相同。
[  ]
]
规律二:等物质的量的不同有机物CnHm、CnHm(H2O)x、CnHm(CO2)y、CnHm(H2O)x(CO2)y(其中变量x、y为正整数),完全燃烧耗氧量相同。或者说,一定物质的量的由不同有机物CnHm、CnHm(H2O)x、CnHm(CO2)y、CnHm(H2O)x(CO2)y(其中变量x、y为正整数)组成的混合物,无论以何种比例混合,完全燃烧耗氧量相同,且等于同物质的量的任一组分的耗氧量。
符合上述组成的物质常见的有:
①相同碳原子数的单烯烃与饱和一元醇、炔烃与饱和一元醛。其组成分别为
![]() 。
。
②相同碳原子数的饱和一元羧酸或酯与饱和三元醇。
![]()
③相同氢原子数的烷烃与饱和一元羧酸或酯

规律三:若等物质的量的不同有机物完全燃烧时生成的H2O的量相同,则氢原子数相同,符合通式CnHm(CO2)x(其中变量x为正整数);若等物质的量的不同有机物完全燃烧时生成的CO2的量相同,则碳原子数相同,符合通式CnHm(H2O)x(其中变量x为正整数)。
(2)质量一定的有机物燃烧
规律一:从C+O2=CO2、6H2+3O2=6H2O可知等质量的碳、氢燃烧,氢耗氧量是碳的3倍。可将CnHm→CH(m/n),从而判断%m(H)或%m(C)。推知:质量相同的烃(CnHm),m/n越大,则生成的CO2越少,生成的H2O越多,耗氧量越多。
规律二:质量相同的下列两种有机物 与
与 完全燃烧生成CO2物质的量相同;质量相同的下列两种有机物
完全燃烧生成CO2物质的量相同;质量相同的下列两种有机物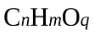 与
与 ,燃烧生成H2O物质的量相同。
,燃烧生成H2O物质的量相同。
规律三:等质量的具有相同最简式的有机物完全燃烧时,耗氧量相同,生成的CO2和H2O的量也相同。或者说,最简式相同的有机物无论以何种比例混合,只要总质量相同,耗氧量及生成的CO2和H2O的量均相同。
(3)由烃燃烧前后气体的体积差推断烃的组成
当温度在100℃以上时,气态烃完全燃烧的化学方程式为:

①△V> 0,m/4> 1,m> 4。分子式中H原子数大于4的气态烃都符合。
②△V= 0,m/4= 1,m= 4。、CH4,C2H4,C3H4,C4H4。
③△V< 0,m/4< 1,m< 4。只有C2H2符合。
(4)根据含氧烃的衍生物完全燃烧消耗O2的物质的量与生成CO2的物质的量之比,可推导有机物的可能结构
①若耗氧量与生成的CO2的物质的量相等时,有机物可表示为
②若耗氧量大于生成的CO2的物质的量时,有机物可表示为
③若耗氧量小于生成的CO2的物质的量时,有机物可表示为
(以上x、y、m、n均为正整数)
最简式相同的有机物
(1)CH:C2H2、C4H4(乙烯基乙炔)、C6H6(苯、棱晶烷、盆烯)、C8H8(立方烷、苯乙烯)
(2)CH2:烯烃和环烯烃
(3)CH2O:甲醛、乙酸、甲酸甲酯、葡萄糖
(4)CnH2nO:饱和一元醛(或饱和一元酮)与二倍于其碳原子数的饱和一元羧酸或酯。如:乙醛(C2H4O)与丁酸及异构体(C4H8O2)
(5)炔烃(或二烯烃)与三倍于其碳原子数的苯及苯的同系物。如丙炔(C3H4)与丙苯(C9H12)

- 全部评论(0)
