������ˮ���йصļ���
ʱ��:2020-03-30 21:19 ��Դ:δ֪ ����:Τΰ ���:�� ����ר�⣺ �л���ѧ���� ��ˮ��
��Ȩ��������������Ϊ����ѧ��ϰ�ҡ�����ζ��δ����ϵ��ԭ���ߣ���ԭ���߿�����������ϵ�����䣺79248376@qq.com����
�ݹ۽�����ĸ߿����л���ѧһֱ����Ҫ��������֮һ. ������֪���߿���ѧ����ṹ����˵����7 �� 4����7��ѡ�� ��4�����⣬�����л���ѧһ�㶼ռ2��ѡ��(12��)�������� ��һ������ѡ��(��ѡһ)�У��л���ѧ��ռ��һ(15��)���� 2012��߿��¿α����۾���ѧ�У�����һ��ʵ����(14��)�����屽���Ʊ���ʹ����100�־����У��л���ѧ��ռ�� 41��֮ �࣬�ɴ˿ɼ����߿���ѧ�У��л���ѧ�Dz��ܺ��ӵ�һ����.�� �У��й�����ˮ��ļ��㼰��ص��ƶ����Ǿ�����������ݡ�
�����л���ѧ�ڸ��л�ѧ��ռ������˵���Ҫ��λ������ ������⼸������ܸ�ϰ�ľ��飬��������ˮ��ļ�������� ���ܽ�һ�³������ͺͽ��������ķ���.
�����й�����ˮ��ļ����ļ���
���������������֣���ʹ����ɵ��������ͷ����ɵ������� ��֬����������ɵ���(��֬).�������Ͳ�ͬ��ˮ�����ͬ���ᵼ����ˮ���������IJ�ͬ.
���о�����������ڼ��Ի����µ�ˮ�⣬���ںļ����Ŀ�������ص�.
��1����ˮ����(�׳ư�˾ƥ��)��һ�ֳ����Ľ��ȡ��� �ס���ʹҩ�����һ���л����ᣬ��ṹ��ʽΪ
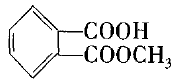
��������ˮ���ܺͼӦ.��1 mol ��˾ƥ�ֺ���������������Һ��Ӧʱ�������������( )
(A) 2 mol (B) 3 mol (C) 4 mol (D) 5 mol
���������и�������ˮ����Ľṹ��ʽ�������ֹ����ţ� һCOOH��һCOO�������ݹ����ŵ����ʣ�1 mol ��COOH�ܺ� 1 mol NaOH�кͣ�������ˮ�Ⲣ������NaOH��NaOHֻ���� �����Ի�������ˮ������ɵ�������ܺͼ���кͷ�Ӧ.�� ���е�����ˮ�����������ʹ����ǻ����л����ʱ���ڷ� ������кͣ�1 mol ���л��ﹲ����������3 mol������ѡ(B).
��2 ��֪��ij�л�����ṹΪ
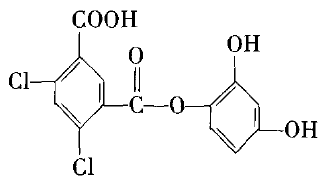
(A) 1 mol��4 mol (B) 3 mol��7 mol
(C) 2 mol��4 mol (D) 3 mol��9 mol
���������ݷӺ�����Ļ�ѧ���ʣ�1 mol ���ǻ�������Ʒ� Ӧ��1 mol �����ƣ�1 mol һCOOH������Ʒ�Ӧ��1 mol ���� �ƣ���֪���л���Ľṹ����2�����ǻ���1��һCOOH����� 1 mol ���л���������Ʒ�Ӧ������3 mol �����ơ����⣬���л����л������ֹ����ţ���������ԭ�ӣ������� �������Ʒ�Ӧ�����У����˷��ǻ����Ȼ�������������⣬�� ��ˮ�⣬±������ˮ��Ҳ�����������ƣ��ر���Ҫע����ǣ�ˮ ������У��������ƽ�������Ϊ�������ṩ���Ի������ѣ��� �������������{����ˮ���IJ��������������Ʒ�Ӧ��ˮ����������Ȼ������ǻ��Լ�HCl���ټ���ԭ���ķ��ǻ����Ȼ����� ��1 mol ���л������������������Ʒ�Ӧ��9 mol ��������.
����ͨ������ˮ��ļ����ж��������
������Ӧ�Ĺ���һ���ǡ������ǻ��������⡱������������ ��CһO���Ǻ��γɵģ���֮������ˮ��ʱ��Ҳ��CһO�������� �ѣ�������Ӧ����ʹ�.
��3�л���A��һ��������ˮ�����ɼס��������л�� ������С�մ���Һ��Ӧ������ͬ�����£�������ͬ�ļס������� ������ռ�������ͬ���������л����У������������( )
(A)��������
(B)�������
(C)�������
(D)1��������
����������֪��ˮ���IJ�������С�մ���Һ��Ӧ�ı��� �ᣬ��������ǿ��̼�ᡣ
��±����ˮ�����ڼ��������½��У���������±������ ��Ӧ�����Σ���˲��������ᣬ���������ų�(D)ѡ��.���⣬ ������˵����ͬ�����£�������ͬ�ļס�������������ռ����� ��ͬ������˵����ˮ���Ժ����ɵ���ʹ�����Է����������� �ȣ����ѡ��(C)Ϊ��ȷ��.��n��̼ԭ�����ı���һԪ���� (n �� 1)��̼ԭ�����ı���һԪ������Է���������ȡ�
��4 ij���ķ���ʽ��Cn��3H2n��4 O2�����Ƿ���ʽΪ CnH2n-2O2��A���л���B��Ӧ�������B�ķ���ʽ��( )
(A) C3H6O (B) C3H6O2 (C) C3H8O (D) C2H6O
����������֪���ķ���ʽ��֪��������һԪ���������ᣫ�� =����ˮ�����ķ���ʽ����һ���ӵ�ˮ�ķ���ʽ��Ȼ���ټ�ȥA�ķ���ʽ�����ɵ�b�ķ���ʽ������B�ķ���ʽΪC3H8O������ ѡ(C)��

- ȫ�����ۣ�0��
