建构“三步”解题模型,突破高考电化学题
时间:2023-08-23 10:35 来源:未知 作者:刘洁 点击: 次 所属专题: 电化学选择题
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
各种层出不穷的电化学装置给人类工作和生活带来了便利,相关的电化学知识也成为了高考命题的热点.高考试题常常关注新型化学电源,具有基于真实问题情境考查学科知识与能力、学科核心素养的趋势,同时试题对学生接受、吸收、整合化学信息的能力以及分析解决问题的能力提出了全方位、更高层次和水平的认知要求.由于该题型存在情境新颖、陌生度大、问题真实等特点,学生普遍感觉较难突破,但这些高考题的考点实际上是课堂教学所研究的基础问题:电极判断、电极反应式和微粒移动,故本文通过建构解题模型“三步曲”,帮助学生快速准确地突破电化学选择题.
一、分清两池———原电池、电解池
高考试题会对陌生情境的装置进行相关的文字介绍或必要的标注,首先应该确定题中所涉及的是哪种装置 , 是只含原电池还是只含电解池,或是可充放电的二次电池,因为原电池装置和电解池装置所对应的工作原理是不同的.
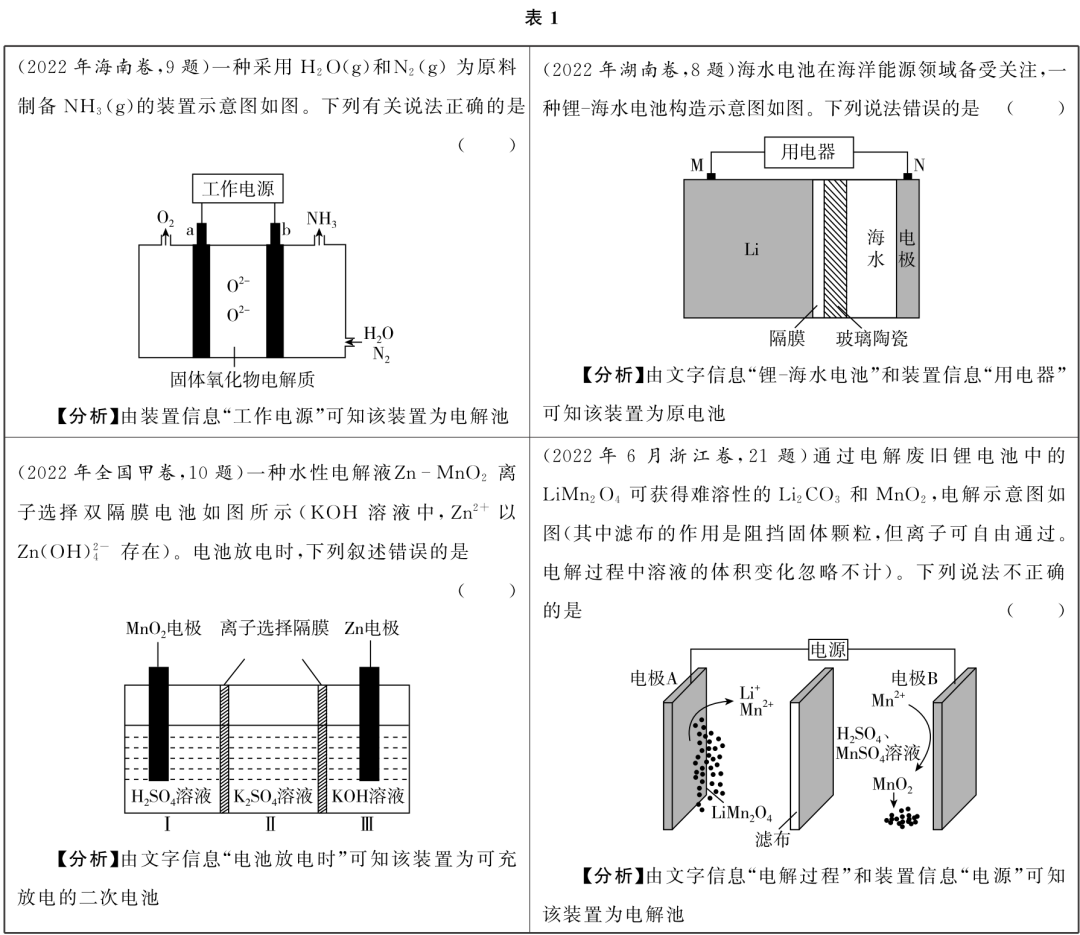
如果是二次电池,要明确放电方向和充电方向.放电时,装置遵循原电池工作原理 ——“ 负失正得、负负正正 ”( 负极失去电子,正极得到电子 , 带负电荷的阴离子向负极移动 , 带正电荷的阳离子向正极移动 );充电时,装置遵循电解池工作原理 ——“ 阳失阴得、阴阳相吸 ”(阳极失去电子 , 阴极得到电子 , 阴离子向阳极移动 , 阳离子向阴极移动).
二、判断两极———负或正、阴或阳
如何判断两极有很多种方法,不管何种方法,本质是相同的.原电池中失去电子的电极为负极、得到电子的电极为正极(负失正得),而电解池中失去电子的电极为阳极、得到电子的电极为阴极(阳失阴得),二次电池中充放电对应的电极反应正好相反.

结合上述内容,分清两池后,根据题中的信息正确判断两极,但是要注意一定不能混淆两极,原电池中的两极名称是正极、负极,而电解池中的两极名称是阳极、阴极.
在明确两极的过程中,可以完成电极反应式的书写和判断:
第一步:找信息,定物质;认真审题,获取题中的信息(文字信息、装置信息),确定该电极上的反应物和生成物.
第二步:标价态,写得失;标出价态变化元素的化合价,化合价升高即失去电子,降低即得到电子,并确定得失电子的数目即电子的系数.
第三步:看环境,配守恒;结合电极反应所处的环境,根据得失电子守恒、电荷守恒和原子守恒将电极反应式配平.


三、确定两路———内电路、外电路
在电化学装置中,微粒移动的考查有两大方面,内电路离子的移动方向和外电路电子的移动方向.在前两步的基础上,确定选项所涉及的是外电路中的电子还是内电路中的离子,然后熟记下表中口诀进行判断.若遇到相关计算,要谨遵“守恒思想”,外电路两极上得失电子总数相等,内电路移动离子的电荷总数与外电路电子的电荷总数相等.






- 全部评论(0)
