元素拓展:锌及其化合物总结
时间:2023-10-07 11:19 来源:未知 作者:化学自习室 点击: 次 所属专题: 锌及其化合物
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.锌及其化合物“心连心”
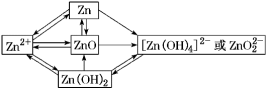
2.金属锌的化学性质
(1)与空气中的水、CO2、O2反应:
CO2+2O2+3H2O+4Zn===ZnCO3·3Zn(OH)2
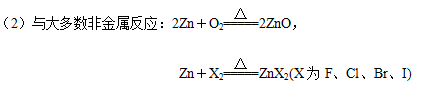
(3)与酸、碱的反应:Zn+2HCl===ZnCl2+H2↑,
Zn+2H2O+2NaOH===Na2[Zn(OH)4]+H2↑
或Zn+2NaOH===Na2ZnO2+H2↑
(4)与盐溶液的置换反应:Zn+Cu2+===Cu+Zn2+
3.氧化锌——两性氧化物
ZnO+2HCl===ZnCl2+H2O
ZnO+2NaOH+H2O===Na2[Zn(OH)4]
或ZnO+2NaOH===Na2ZnO2+H2O
4.氢氧化锌——两性氢氧化物
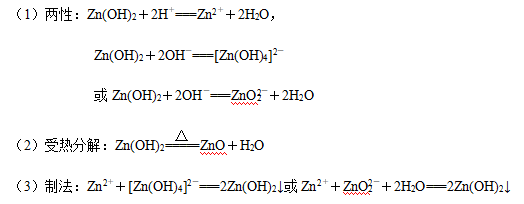
5.锌盐
(1)ZnSO4
①与可溶性钡盐反应:
ZnSO4+BaCl2===ZnCl2+BaSO4↓
②与强碱溶液反应
ZnSO4溶液中加入少量NaOH溶液:
Zn2++2OH-===Zn(OH)2↓
ZnSO4溶液中加足量NaOH溶液:
Zn2++4OH-===[Zn(OH)4]2-
或Zn2++4OH-===ZnO22-+2H2O
③与Na2[Zn(OH)4]或Na2ZnO2反应生成Zn(OH)2沉淀。
(2)Na2[Zn(OH)4]或Na2ZnO2
①与少量盐酸反应:
Na2[Zn(OH)4]+2HCl===Zn(OH)2↓+2NaCl+2H2O
或Na2ZnO2+2HCl===Zn(OH)2↓+2NaCl
②与足量盐酸反应:
Na2[Zn(OH)4]+4HCl===ZnCl2+2NaCl+4H2O
或Na2ZnO2+4HCl===ZnCl2+2NaCl+2H2O
③与少量CO2反应:
Na2[Zn(OH)4]+CO2===Zn(OH)2↓+Na2CO3+H2O
或Na2ZnO2+CO2+H2O===Zn(OH)2↓+Na2CO3
④与足量CO2反应:
Na2[Zn(OH)4]+2CO2===Zn(OH)2↓+2NaHCO3
或Na2ZnO2+2H2O+2CO2===Zn(OH)2↓+2NaHCO3
⑤与可溶性锌盐发生相互促进的水解反应,生成Zn(OH)2沉淀。

- 全部评论(0)
