羧酸的酸性大小的比较
时间:2024-03-13 07:05 来源:未知 作者:化学自习室 点击: 次 所属专题: 羧酸酸性
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
影响脂肪族羧酸酸性的因素:
(1)连有吸电子诱导效应的原子或基团,使酸性增强;连有给电子诱导效应效应的原子或基团,使酸性减弱。

图1 吸电子诱导效应↓,酸性↓

图2 诱导效应具有加和性

图3 诱导效应与距离成反比
(2)与羧基存在共轭效应的基团,能使羧基上电子云密度分散,使得酸性增强。

图4
影响芳香族羧酸酸性的因素:
在芳环上引入一般来说,在芳环上引入吸电子基团,使酸性增强;引入供电子基团使酸性减弱,而且还与基团所连接的位置有关。
(1)对位取代芳香酸的酸性同时受诱导效应和共轭效应的影响(如图5)。

图5
(2)间位取代芳香酸的酸性,因共轭效应受阻,主要受诱导效应的影响(如图6)。

图6
(3)邻位取代芳香酸的酸性都较苯甲酸的酸性强(如图7)。

图7
注:
a. 这主要是电子效应和空间效应综合影响的结果。由于邻位取代基的空间效应使苯环与羧基难以形成共平面,难以产生共轭效应 (苯环与羧基共轭时,苯环具有+C效应);另一方面邻位取代基与羧基的距离较近,-I效应的影响较大,故酸性增强。
b. 有的有的邻位基团能与羧基形成氢键,使其羧基的氢更易解离,因此表现出更强的酸性。
题目:
1. 将下列二元酸化合物按酸性强弱顺序排列。
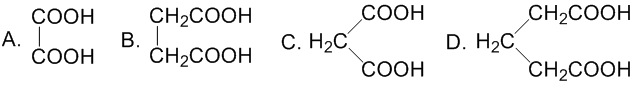
2. 将下列化合物按酸性由大到小排列。
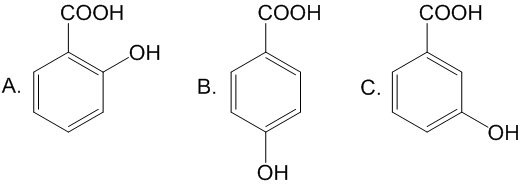
答案:
1. A>C>B>D
2. A>C>B
解析:
第一题,二元酸中两个羧基随着距离增加,而使其中一个羧基对另个羧基的吸电子诱导效应降低,进而酸性降低。故酸性大小为A>C>B>D。
第二题,羟基为在邻位时与羧基可形成氢键(如图8),稳定羧基负离子,因此酸性最强。又由于羟基在对位时为给电子基,因此酸性减弱,在间位时是吸电子基,酸性增强。因此,酸性大小为A>C>B。

图8
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
