电极反应式书写错误例析
时间:2017-08-21 22:24 来源:河北省赵县实验中学 作者:丁萍 点击: 次 所属专题: 电极反应式
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、 不能正确判断原电池正负极
例1、 将Al片和Cu片用导线相连,插入浓HNO3中,形成原电池。
错误:负极:2Al-6e-=2Al3+
正极:6H++6e-=3H2↑
解析:将Al片和Cu片用导线相连,插入浓HNO3,由于Al在浓硝酸中钝化,不能持续反应,而Cu却能与浓HNO3持续反应,所以Cu为负极,Al为正极,因此正负极的判断应根据氧化还原反应的实质来确定,谁失去电子,谁做为负极。
正确:负极:2Cu-4e-=2Cu2+
正极:2NO3-+2e-+4H+=2NO2↑+2H2O
二、 不能正确判断电极产物
例2、将Al片和Cu片用导线相连,插入稀NaOH溶液中形成原电池。
错误:负极:2Al-6e-=2Al3+
正极:6H++6e-=3H2↑
解析:Cu片和Al片用导线相连插入NaOH溶液中,其实质是Al和NaOH溶液反应,2Al+2NaOH+2H2O=2NaAlO2+3H2↑, Al失去电子生成AlO2-,而正极由于H+在碱性条件下不能大量存在,所以得到电子的物质是H2O
正确:负极:2Al+8OH--6e-=2AlO2-+4H2O
正极:6H2O+6e-=3H2↑+6OH-
三、 忽视电极产物与电解质溶液反应
例3、氢氧燃料电池是一种高效低污染的新型电池,主要用于航天领域,它的电极材料一般为活化电极,具有很强的催化活性。如铂电极、活性炭电极等,电解质溶液一般为40%的KOH溶液,写出电极反应式:
错误:负极:2H2-4e-=4H+
正极:O2+2H2O+4e-=4OH-
解析:在负极H2失去电子生成H+,而H+在碱性溶液中与OH-反应,生成H2O,因此应把两个式子合并为:2H2+4OH--4e-=4H2O
正确:负极:2H2+4OH--4e-=4H2O
正极:O2+2H2O+4e-=4OH-
四、 忽视了电解质的状态
例4、固体氧化物燃料电池是由美国西屋公司研制开发的,它从固体氧化锆——氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极A、b均不参与电极反应
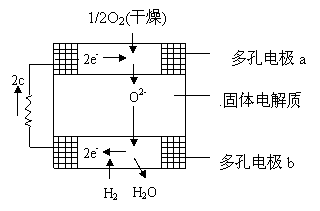
其电极反应式为_________。
错误:负极:2H2-4e-=4H+
正极:O2+2H2O+4e-=4OH-
解析:此类燃料电池的电解质是固体,并不是水溶液,因此正极电极反应为:
O2+4e-=O2-
正确:负极:2H2+O2--4e-=2H2O
正极:O2+4e-=O2-
五、 忽视了金属单质与阴、阳离子的放电顺序
例5、电解醋酸的浓溶液,以Pb做电极,在电解过程中,无沉淀产生,但电解效率逐渐下降,同时[H+]也随之降低,随后溶液不再导电,电解自然停止。
(1)电极反应是_________;
(2)电解总反应的方程式为_________;
错误:阳极:4OH—4e-=O2↑+2H2O
阴极:2H++2e-=H2↑
分析:放电顺序:
阳极:非惰性电极>I->Br->Cl->OH->SO42-(NO3-)
阴极:Ag+>Cu2+>Fe2+>Mg2+
(1)本题属于电解的应用。用铅做阳极材料,根据电解规律,非惰性电极做阳极时,阳极本身被氧化而溶解,即Pb-2e-=Pb2+,而Pb2+与CH3COO-结合生成难电离的(CH3COO)2Pb,所以阳极反应为:Pb+2CH3COOH-2e-=(CH3COO)2Pb+2H+,阴极反应为:2H++2E=H2↑
(2)电解总反应式为:Pb+2CH3COOH ![]() (CH3COO)2Pb+H2↑
(CH3COO)2Pb+H2↑
练习1: 按图所示进行铁钉被腐蚀的实验,
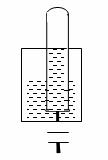
一周后观察:
(1) 若试管中液面上升,发生的是_________腐蚀,
电极反应:正极_________,负极_______。
(2) ![]() 若试管中液面下降,发生的是_________腐蚀,
若试管中液面下降,发生的是_________腐蚀,
电极反应:正极_________,负极_________。
练习2: 将铂电极插入氢氧化钾溶液,然后向两个电极分别通入甲烷等燃料和氧气等氧化剂组成的一种电池。由于所发生的反应类似于甲烷的燃烧,所以称为燃料电池。根据两极上反应实质判断通入甲烷的一极为电池的____极,这一电极的反应式为_________,该电池放电反应的总反应方程式为_________。
练习3 :设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一,最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的 ZrO2晶体,它在高温下能传导O2-,回答如下问题:
(1) 以丁烷代表汽油,这个电池放电时发生的化学反应的化学方程式是:_______。
(2) 这个电池的正极发生的反应是:_________,负极发生的反应是:_________,固体电解质里的O2-的移动方向是:_________,向外电路释放电子的电极是:_________。
(3) 人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是什么?_________。
(4)汽油燃料电池最大的障碍是氧化不完全产生_________堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,这正是新一代化学家的历史使命。
答案:练习1:(1)吸氧腐蚀 O2+2H2O+4e-=4OH- 2Fe-4e-=2Fe2+
(2)吸氢腐蚀 H2+2e-=2H+ Fe-2e-=Fe2+
练习2:负 CH4+10OH--8e-=CO32-+7H2O CH4+2O2+2OH-=CO32-+3H2O
练习3:(1)
(2)13O2+52E=2O2-
(3)燃料电池具有较高的能量利用率。
(4)炭粒

- 全部评论(0)
