镁及其化合物知识点总结
时间:2026-01-13 11:18 来源:未知 作者:化学自习室 点击: 次 所属专题: 镁及其化合物
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、镁
(一)镁的结构
1、构成微粒:Na+和自由电子,作用力金属键
2、电子排布式:1s22s22p63s2
3、第一电离能:I1(Mg)>I1(Al)
4、晶胞结构
(1)堆积名称:六方最密堆积,堆积类型:A3型或镁型
(2)堆积方式:…ABAB…
(3)配位数12

(4)结构和性质的关系

(二)物理性质
具有银白色金属光泽的固体,密度、硬度均较小,熔点较低,有良好的导电、传热和延展性
(三)化学性质

1、与非金属反应(O2、Cl2、N2等)
(1)与O2反应:
![]()
(发出耀眼的白光)
(2)与Cl2反应:
![]()
(3)与N2反应:
![]()
(4)与S反应:

2、与H2O反应:
![]()
(冷水慢,沸水快)
3、与非氧化性酸(如:稀盐酸、稀硫酸)的反应:

4、与CO2反应:
![]()
(剧烈燃烧,生成白色粉末和黑色固体)
5、与盐溶液反应:
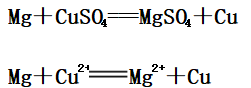
6、镁与NH4Cl溶液反应
(1)反应:

(2)原理:Mg与H+反应,促进NH4Cl的水解平衡正向移动
(四)镁的用途
1、国防金属:镁合金的强度高、机械性能好,制造汽车、飞机、火箭
2、冶金工业:用做还原剂和脱氧剂
3、军事上:用做照明弹、燃烧弹
(五)海水提镁
1、流程图

2、基本反应
(1)制取石灰乳:

(2)沉淀Mg2+:
![]()
(3)提取MgCl2:
![]()
(4)制氯化镁晶体:
![]()
①基本操作:加热浓缩、冷却结晶、过滤洗涤、干燥称量
②基本仪器:酒精灯、烧杯、玻璃棒、漏斗、干燥器、天平

(5)氯化镁晶体脱水:

①HCl的作用:带走部分水蒸气,减少MgCl2的水解
②HCl的作用:抑制MgCl2的水解,得到无水MgCl2
(6)制金属镁
①反应:

②加入少量CaCl2的作用:降低MgCl2的熔点,节能
3、原料
(1)直接原料:海水、贝壳和盐酸
(2)间接原料:氢气
(3)循环利用:氯气
二、氧化镁
1、晶胞结构(晶胞参数a cm)

(1)晶胞中含MgO个数:4
(2)配位数:6,O2-的堆积方式:面心立方最密堆积
(3)晶格能:MgO>CaO
(4)晶胞密度:

2、物理性质:
白色固体,难溶于水,熔点较高,是优良的耐火材料
3、化学性质:
属于碱性氧化物,具有碱性氧化物的通性
(1)与水能缓慢反应:

(2)能与酸反应:

4、工业制备(煅烧碳酸镁):

5、主要用途:氧化镁熔沸点高,可制造耐火、耐高温器材
三、氢氧化镁
1、物理性质:
白色固体,难溶于水的中强碱,能使酚酞试液变为浅红色
2、化学性质
(1)能与酸反应:
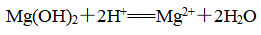
(2)热稳定性差:

(3)溶解度小于碳酸镁:

3、实验室制法
(1)将NaOH溶液滴入MgCl2溶液中:

(2)将氨水滴入MgSO4溶液中:

四、氮化镁
1、电子式:

2、化学性质
(1)水解反应:

(2)与酸反应:

五、碳酸镁
1、溶解性:难溶于水,溶解度比Mg(OH)2的大
2、热不稳定性:
 (工业制备MgO)
(工业制备MgO)
3、分解温度:CaCO3>MgCO3
六、镁的化合物间的重要转化关系
1、一些镁盐加热蒸干、灼烧的产物

2、惰性电极电解某些镁的化合物
(1)MgCl2溶液:

(2)熔融MgCl2:

(工业上炼镁原理)
(3)熔融MgO:

(耗能多,不适于炼镁)
七、碳酸镁转化成氢氧化镁
1、转化的实质:沉淀的转化

2、转化的原因:
MgCO3的溶解度比Mg(OH)2的大
3、转化的应用:
Mg(HCO3)2溶液与NaOH溶液的反应
(1)少量NaOH:

(2)少量NaOH:


- 全部评论(0)
