化学工艺流程题常考元素之硼及其化合物
时间:2026-05-06 07:39 来源:未知 作者:化学自习室 点击: 次 所属专题: 硼及其化合物 工艺流程题常考元素
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、硼及其常考化合物的性质简介
1.硼单质
硼(B)的化学性质与 Si有某些相似之处(对角线相似原则),通常呈现+3氧化数,负氧化数的情况很少见。B₂O₃是酸性氧化物,硼烷、硅烷可形成多种可燃性气态物质,而AlH3是固态的。在自然界中,硼以硼砂(Na2B4O7·10H2O)、四水硼砂(Na2B4O7·4H2O)、天然硼酸(H3BO3)的形式存在。
硼在自然界中丰度之所以低,是因为

所以硼材料可作为核反应堆的减速剂和生物防护。单质硼有多种复杂的晶体结构,其中,最普通的一种是α-菱形硼,其结构如图所示,基本结构单元为正二十面体的对称几何构型,然后由 B12的这种二十面体排布起来组成六方晶系的α-菱形硼。

2.硼烷
硼烷是缺电子化合物,例如,B2H6中价电子总共只有12个,不足以形成7 个二中心二电子单键(2C-2e-),B原子采取sp³杂化,位于一个平面的 BH2原子团以二中心二电子键连接,位于该平面上、下且对称的H原子与硼原子分别形成三中心二电子键,称为氢桥键。其分子结构如图3.4所示。

硼烷可作为火箭燃料:
 -1
-1
乙硼烷(B₂H₆)理应是理想的火箭燃料,但由于硼烷有很高的毒性,且贮存条件苛刻(易燃且易水解),只好暂时放弃。
硼烷作为一种万能还原剂在有机化学上被广泛使用。可以用于制备聚合物,其在高温下稳定,低温下保持黏度不变。硼烷化合物与蛋白质结合,可用于肿瘤治疗。
乙硼烷的制备方法主要包括以下 3种:
(1)质子置换法:

(2)氢化法:

(3)氢负离子置换法:


3.硼的含氧化合物
(1)B2O3
B2O3易溶于水,可用作吸水剂:

熔融的B2O3可与金属氧化物反应得到特征颜色:
 (蓝色)
(蓝色)
 (绿色)
(绿色)
B2O3与NH3反应,在500℃时生成(BN)n,其结构与石墨相似。

(2)H3BO3
H3BO3为一元弱酸,呈片状晶体结构,OH ⁻间以氢键连接。在冷水中溶解度小,在热水中因部分氢键断裂而使溶解度增大。

H3BO3与碱反应时,有

过量 NaOH 使 Na2B4O7变成NaBO2

H3BO3的酸性可通过加入甘油或甘露醇等多元醇而大大增强:

二、以典例逐层破解陌生元素的工艺流程题的思维
25-26高三上·北京东城·期末试题如下:
某盐湖卤水中含Na+、Mg2+、Li+、Cl-、[B(OH)4]-等。一种综合利用流程示意图如下。

(1)脱硼时[B(OH)4]-转化为H3BO3的离子方程式是___________。
(2)H3BO3在水中的溶解度随温度升高而显著增大。补全重结晶的步骤:加热溶解、___________(补全操作)、过滤、洗涤、干燥。
(3)由浓缩液制备高纯Li2CO3流程示意图如下。

已知:
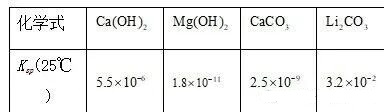
①沉镁反应的离子方程式是___________。
②沉钙时,当c(Ca2+)<1×10-5mol/L,可认为其沉淀完全。溶液2中,若c(Li+)=2 mol/L,则c(CO32-)的范围是___________~___________mol/L。
(4)电解LiHCO3溶液原理示意图如下。

结合电极反应式解释,电解过程中LiOH溶液浓度增大的原因:___________。
(5)电解后,向浓LiOH溶液中加入过量NH4HCO3溶液并加热,过滤后直接烘干即可制得高纯Li2CO3.为确保Li2CO3纯度,NH4HCO3必须过量,原因是___________。
1、问题剖析
本题为工艺流程题,向某含Na+、Mg2+、Li+、Cl-、[B(OH)4]-等的盐湖卤水中加入盐酸进行脱硼处理,过滤得到粗硼酸晶体和脱硼液,对粗硼酸进行重结晶处理可获得高纯H3BO3,将脱硼液进行脱水浓缩得到浓缩液,向浓缩液中加入石灰乳进行沉镁,过滤得到溶液1和沉淀1Mg(OH)2、Ca(OH)2,向溶液1中加入Na2CO3进行沉钙出来,过滤得到溶液2和沉淀2CaCO3,向溶液2中加入饱和Na2CO3溶液进行沉锂,过滤得到粗Li2CO3沉淀,将Li2CO3沉淀转化为LiHCO3溶液,电解LiHCO3溶液得到LiOH,LiOH溶液和CO2反应获得高纯Li2CO3,据此分析解题。
(1)脱硼时[B(OH)4]-和盐酸发生反应,生成H3BO3和H2O,[B(OH)4]-+H+=H3BO3↓+H2O;
(2)因为杂质是难溶性物质,而H3BO3在水中的溶解度随温度升高而显著增大,故趁热过滤,除去不溶性杂质后,冷却结晶,使H3BO3析出,故答案为:趁热过滤,冷却结晶;
(3)①Ca(OH)2浊液和Mg2+反应生成Mg(OH)2,离子方程式:Ca(OH)2(s)+Mg2+(aq)==Mg(OH)2(s)+Ca2+(aq);
②当钙离子恰好沉淀完全时,c(Ca2+)=1×10-5mol/L,由Ksp(CaCO3)=c(Ca2+)c(CO32-)得c(CO32-)==mol/L=2.5×10-4mol/L,根据题意,Li2CO3不能沉淀,由Ksp(Li2CO3)=c2(Li+)c(CO32-)得c(CO32-)==mol/L=8×10-3mol/L,所以c(CO32-)的范围:2.5×10-4mol/L~8×10-3mol/L,故答案为:2.5×10-4;8×10-3;
(4)电解LiHCO3溶液是水的电解,阴极反应式为2H2O+2e-=H2↑+2OH-,电解过程中Li+从阳极通过Li+离子交换膜进入阴极溶液,与阴极生成的OH-形成LiOH,因此LiOH浓度增大;
(5)加入过量的NH4HCO3,为了确保LiOH完全转化为Li2CO3,无剩余;加热条件下,NH4HCO3会分解氨气、二氧化碳和水,烘干时易除去,不会引入新杂质,故答案为:确保LiOH完全转化为Li2CO3,无剩余;加热条件下,NH4HCO3会分解氨气、二氧化碳和水,烘干时易除去,不会引入新杂质.
2、好题思路反思,到底考了哪些知识点?
Ø脱硼离子方程式:卤水中的 [B(OH)₄]⁻ 与加入的盐酸反应生成硼酸沉淀,属于复分解反应,注意硼酸是弱酸但难溶于水,离子方程式为 [B(OH)₄]⁻ + H⁺ = H₃BO₃↓ + H₂O。
重结晶操作:由于硼酸溶解度随温度升高显著增大,重结晶时应先加热溶解,再趁热过滤除去不溶性杂质,然后冷却结晶使硼酸析出,最后过滤、洗涤、干燥。因此补全的操作为“趁热过滤,冷却结晶”。
沉镁反应:加入石灰乳(Ca(OH)₂ 悬浊液)与 Mg²⁺ 反应生成 Mg(OH)₂ 沉淀,由于石灰乳以固体形式存在,离子方程式应写为 Ca(OH)₂(s) + Mg²⁺(aq) ⇌ Mg(OH)₂(s) + Ca²⁺(aq),体现固体参与反应。
沉钙时 CO₃²⁻ 浓度范围:要求 Ca²⁺ 沉淀完全(c(Ca²⁺) < 1×10⁻⁵ mol/L)且 Li⁺ 不沉淀。根据 Ksp(CaCO₃) = c(Ca²⁺)·c(CO₃²⁻),可得使 Ca²⁺ 沉淀完全所需的最小 c(CO₃²⁻) = Ksp(CaCO₃) / 1×10⁻⁵ = 2.5×10⁻⁹ / 10⁻⁵ = 2.5×10⁻⁴ mol/L。同时,为防止 Li₂CO₃ 沉淀,c(CO₃²⁻) 必须小于使 Li₂CO₃ 开始沉淀的浓度,由 Ksp(Li₂CO₃)=c²(Li⁺)·c(CO₃²⁻)得 c(CO₃²⁻) = Ksp(Li₂CO₃) / (2²) = 3.2×10⁻2/ 4 = 8×10⁻³ mol/L,思路是利用溶度积计算两个临界值,得出范围。
电解 L iHCO₃ 溶液:电解池中阴极发生还原反应:2H₂O + 2e⁻ = H₂↑ + 2OH⁻,阳极发生氧化反应:2H₂O - 4e⁻ = O₂↑ + 4H⁺。Li⁺ 通过阳离子交换膜从阳极区移向阴极区,与阴极生成的 OH⁻ 结合成 L iOH,因此阴极区 LiOH 浓度增大。
NH₄HCO₃ 过量的原因:为确保 LiOH 完全转化为 Li₂CO₃,需要加入过量 NH₄HCO₃;同时过量的 NH₄HCO₃ 在加热条件下分解为 NH₃、CO₂ 和水,烘干时易除去,不会引入新杂质,从而保证产品纯度。

- 全部评论(0)
