条件不同 产物各异
时间:2016-03-09 18:37 来源:未知 作者:田兴虎 点击: 次 所属专题: 条件与产物
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在化学反应过程中,由于反应条件、反应物的物质的量不同等原因,往往使反应进程发生改变,导致反应生成物的不同。中学化学中涉及到的这类反应很多,学习、掌握和运用这些反应,不仅可以深刻理解化学反应实质,且有利于培养严谨的科学态度,使知识得以升华。
一、反应物浓度的影响
随着反应进行,反应物的浓度逐渐减少,有的反应就会停止或者进行另一反应。如实验室用![]() 与浓盐酸反应制取
与浓盐酸反应制取![]() ,盐酸的浓度不断降低,最终反应停止;铜与浓
,盐酸的浓度不断降低,最终反应停止;铜与浓![]() 在加热条件下反应,随着反应进行,浓
在加热条件下反应,随着反应进行,浓![]() 也转变为稀
也转变为稀![]() ,因铜与稀
,因铜与稀![]() 不反应导致反应停滞;铜与浓
不反应导致反应停滞;铜与浓![]() 反应时,生成的气体也由
反应时,生成的气体也由![]() 变为NO,所以得到气体一般是两者的混合物。
变为NO,所以得到气体一般是两者的混合物。
二、反应温度的影响
温度不仅是影响化学反应速率快慢的一个重要因素,温度的不同也能影响反应“进程”,从而得到不同产物,如:
1. ![]() 与浓
与浓![]() 反应
反应
![]() (浓)
(浓)![]()
![]()
![]() (浓)
(浓)![]()
![]()
2. ![]() 与强碱反应
与强碱反应
![]()
3. 钠与氧气反应
![]()
4. Al与浓硝酸反应
![]() (冷、浓)
(冷、浓)![]() 钝化
钝化
![]() (热、浓)
(热、浓)![]()
5. 乙醇与浓![]() 加热
加热
![]()
![]()
![]()
![]()
![]()
![]()
三、反应物的量的影响
由于反应物的量不同,改变了反应的进程会得到不同产物。如:
1. 磷在氯气中燃烧
![]()
![]()
![]()
![]() (过量)
(过量)![]()
![]()
2. 硫化氢的燃烧
![]()
![]()
![]()
![]()
![]()
![]()
3. ![]() 通入澄清的石灰水中
通入澄清的石灰水中
![]()
![]() (过量)
(过量)![]()
4. ![]() 溶液与NaOH溶液混合
溶液与NaOH溶液混合
![]()
![]() (过量)
(过量)![]()
5. ![]() 溶液与NaOH溶液混合
溶液与NaOH溶液混合
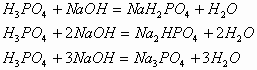
6. 铁与浓![]() 加热
加热
![]() (浓)
(浓)![]()
![]()
![]() (过量)
(过量)![]() (浓)
(浓)![]()
![]()
四、试剂滴加顺序的影响
两溶液反应时,将甲滴入乙或乙滴入甲,出现不同现象,结果产物也不同。如:
1. 向可溶性铝盐溶液中滴加强碱溶液,先出现白色絮状沉淀,继而溶解;向强碱溶液中滴加可溶性铝盐溶液,先无沉淀后出现大量沉淀。
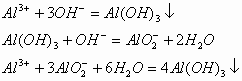
2. 向偏铝酸钠溶液中滴加强酸(如盐酸),先出现白色沉淀,酸过量沉淀溶解;强酸中滴加偏铝酸钠溶液先无沉淀,后出现大量沉淀。
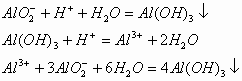
3. 向石灰水[或![]() 溶液]中滴入磷酸,先出现白色沉淀后溶解;反之,先无沉淀后才有沉淀。
溶液]中滴入磷酸,先出现白色沉淀后溶解;反之,先无沉淀后才有沉淀。
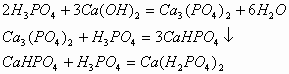
4. 向饱和![]() 溶液中滴加盐酸或硫酸,振荡先无气体逸出,后冒大量气泡;反之则立即产生气泡。
溶液中滴加盐酸或硫酸,振荡先无气体逸出,后冒大量气泡;反之则立即产生气泡。
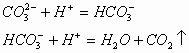
5. 向硝酸银溶液中滴加氨水,先产生沉淀(AgOH或![]() ),后生成
),后生成![]() 络离子而溶解;反之则先无沉淀后才出现沉淀。
络离子而溶解;反之则先无沉淀后才出现沉淀。
6. 向![]() 溶液中滴加少量
溶液中滴加少量![]() 时,因生成硫出现浅黄色沉淀;反之则因
时,因生成硫出现浅黄色沉淀;反之则因![]() 氧化
氧化![]() 而出现黑色沉淀(FeS)。
而出现黑色沉淀(FeS)。
7. 向![]() 胶体中滴加强酸,开始有红褐色沉淀,后红褐色沉淀消失;反之,开始无红褐色沉淀,后产生红褐色沉淀。
胶体中滴加强酸,开始有红褐色沉淀,后红褐色沉淀消失;反之,开始无红褐色沉淀,后产生红褐色沉淀。
8. 向水玻璃溶液中滴加盐酸立即出现白色胶冻(![]() 或
或![]() );反之则无显著现象。
);反之则无显著现象。
9. 氢硫酸中滴加浓溴水,出现浅黄色沉淀;反之则溴水褪色而无沉淀。
10. 向蛋白质中滴加无机盐溶液,开始无白色沉淀后有白色沉淀;反之则开始有白色沉淀后白色沉淀不消失。

- 全部评论(0)
