为什么浓硫酸的氧化性很强?
时间:2016-01-21 16:16 来源:未知 作者:石峰 点击: 次 所属专题: 浓硫酸
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
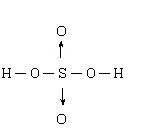
硫原子的价电子构型为3S23P4,在形成硫酸分子的过程中,硫原子发生SP3杂化,其中硫原子的两个SP3杂化轨道与两个氧原子形成两个σ键,另外两个SP3杂化轨道中的孤对电子分别给予两个氧原子,生成配σ键,同时还生成部分反配位π键。因为硫原子的3d轨道是空的,氧原子的孤对P电子可和它生成π键,其方向恰好与σ配键相反,正因为如此,实验测得S→O键长比正常单键略短,但硫原子的3d轨道能量较高,σ-π配键中主要是σ配键,π配键比较弱,因此硫酸的性质非常特别。其分子结构为:
浓硫酸具有强烈的氧化性,在于硫酸是不对称分子,其H+的体积很小,具有强烈的极化作用而使O-2的电子云变形并钻入其中,中和-2价O的部分负电荷,使-2价O与中心原子+6价S的结合力减弱,从而破坏了硫酸分子的稳定性,使得+6价S易接受外来的电子而被还原。因此浓硫酸是一种氧化能力相当强的氧化剂,特别是在加热时,其氧化能力格外显著,能与部分非金属和绝大多数金属反应,其产物依还原剂还原性强弱的不同而异。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!