高中化学中的共轭大π键
时间:2018-05-31 10:33 来源:未知 作者:化学自习室 点击: 次 所属专题: 大π键
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1、苯分子中的p-p大π键
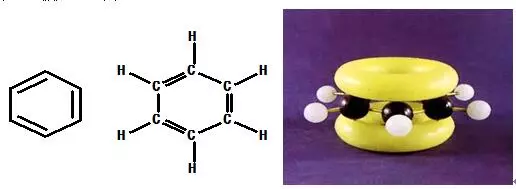
苯的结构式里的碳-碳键有单键和双键之分,这种结构满足了碳的四价,可是事实上苯分子的单键和双键的键长和键能并没有区别,苯的结构式并不能反映这个事实。用形成p-p大P键的概念可以解决这个矛盾。
苯中的碳原子取sp2杂化,每个碳原子尚余一个未参与杂化的p轨道,垂直于分子平面而相互平行。所以我们认为所有6个平行p轨道总共6个电子在一起形成了弥散在整个苯环的6个碳原子上下形成了一个p-p离域大P键,符号P66。用p-p大P键(有机化学中的共轭体系)的概念苯的结构式写成如下右图更好。后者已经被广泛应用。
2、CO2分子里的大π键
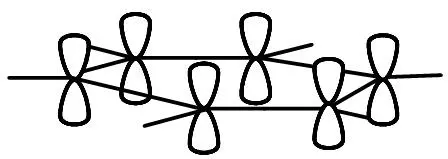
CO2的碳原子取sp杂化轨道,它的两个未参加杂化的p轨道在空间的取向是跟sp杂化轨道的轴相互垂直。CO2分子里有两套3原子4电子符号为P34的p-p大P键。

3、CO32-离子中的大π键
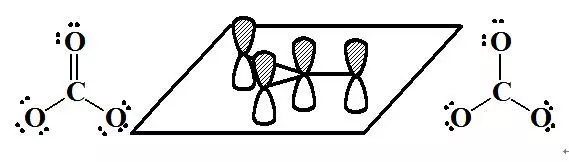
碳酸根离子属于AY3型分子,中心碳原子取sp2杂化形式,碳原子上有一个垂直于分子平面的p轨道;端位的3个氧原子也各有1个垂直于分子平面的p轨道;分子的总价电子数等于24,3个C-O键有6个电子,每个氧原子上有2个不与分子平面垂直的孤对电子对,因此4个平行p轨道中共有24-6-3×4=6个电子,所以CO32-离子中有1个4轨道6电子p-p大Π键,符号为Π46。
4、O3分子里的大π键
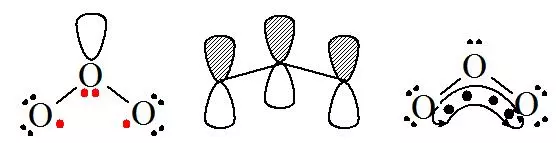
O3分子的中心O原子采取sp2杂化,和两个端位O原子形成两个s键,另外中心O原子和配位O原子都有p轨道,共有4个电子,小于轨道数的两倍6,满足上述条件即可形成离域Π34键。
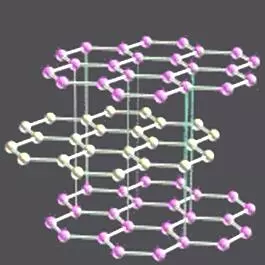
5、石墨里的大π键
石墨结构是层形结构,每层是由无限个碳六元环所形成的平面,其中的碳原子取sp2杂化,与苯的结构类似,每个碳原子尚余一个未参与杂化的p轨道,垂直于分子平面而相互平行。平行的n个p轨道形成了一个p-p大P键。n个电子弥散在整个层的n个碳原子形成的大Π键里,电子在这个大Π nn键中可以自由移动,所以石墨能导电。
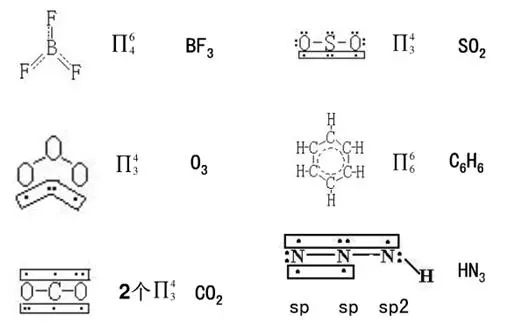
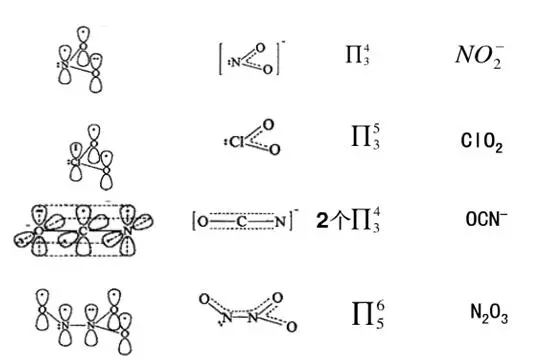
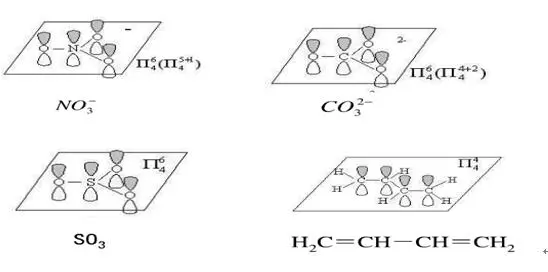
6、其它

- 全部评论(0)
(923623976) 评论 href="/plus/view.php?aid=16773">高中化学中的共轭大:BF3和ClO2能详细解释下吗?
