高中教材必会的有机实验梳理
时间:2020-12-24 15:54 来源:未知 作者:化学自习室 点击: 次 所属专题: 有机实验
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、物理性质实验
1.石油的分馏
实验:装配一套蒸馏装置,将100mL 石油注入蒸馏烧瓶中,再加几片碎瓷片以防石油暴沸。然后加热,分别收集60℃~150℃和150℃~300℃时的馏分。
装置:
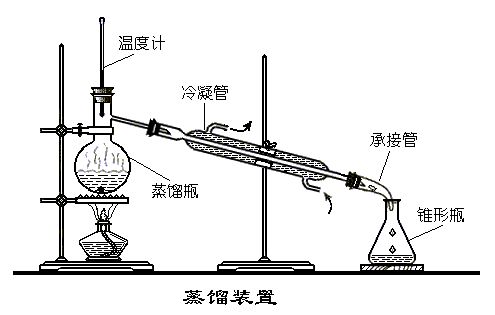
现象与解释:石油是烃的混合物,没有固定的沸点。在给石油加热时,低沸点的烃先气化,经过蒸馏分离出来;随着温度的升高,高沸点的烃再气化,经过蒸馏后又分离出来。收集到的60℃~150℃时的馏分是汽油,150℃~300℃时的馏分是煤油。
2.蛋白质的盐析
实验:在盛有鸡蛋白溶液的试管里,缓慢地加入饱和(NH4)2SO4或Na2SO4溶液,观察现象。然后把少量带有沉淀的液体加入盛有蒸馏水的试管里,观察沉淀是否溶解。
装置:

现象与解释:有沉淀的析出,析出的沉淀可以溶解在水中。向蛋白质溶液中加入某些浓的无机盐溶液后,蛋白质的溶解度减小,使蛋白质凝聚析出,这种作用叫盐析。盐析是一个可逆的过程。
3.有机物物理性质也表现出一定的规律,归纳如下:
⑴颜色:有机物大多无色,只有少数物质有颜色。如苯酚氧化后的产物呈粉红色。
⑵状态:分子中碳原子数不大于4的烃(烷、烯、炔)、烃的衍生物中的一氯甲烷、甲醛呈气态,汽油、煤油、苯、甲苯、乙醇、乙酸、乙酸乙酯等呈液态,绝大多数高分子化合物常温下呈固态。
⑶气味:中学化学中涉及到的很多有机物具有一定的气味,如:苯有特殊气味,硝基苯有苦杏仁味,甲醛、乙醛、乙酸有刺激性气味,乙酸乙酯有芳香气味。
⑷密度:气态有机物的相对分子质量大于29时,密度比空气大;液态有机物密度比水小的有烃(烷、烯、炔、芳香烃)、低级酯、一氯代烃、乙醇、乙醛等;密度比水大的有硝基苯、溴苯、四氯化碳、氯仿、溴代烃、乙二醇、丙三醇等。烷、烯、炔等烃类同系物相对密度随着分子内碳原子数的增加的而增大;一氯代烷的相对密度随着碳原子数的增加而减小。
⑸水溶性:与水任意比混溶和易溶于水的有乙醇、乙酸、乙醛、乙二醇、丙三醇、苯酚(65℃以上)、甲醛、葡萄糖等;难溶于水的有烃(烷、烯、炔、芳香烃)、卤代烃、高级脂肪酸、硝基苯、溴苯。醇、醛、羧酸等有机物的水溶性随着分子内碳原子数的增加而逐渐减小。
二、化学性质实验
(一)甲烷
1.甲烷通入KMnO4酸性溶液中
实验:把甲烷通入盛有KMnO4酸性溶液的试管里,观察紫色溶液是否有变化?
现象与解释:溶液颜色没有变化。说明甲烷与KMnO4酸性溶液不反应,进一步说明甲烷的性质比较稳定。
2.甲烷的取代反应
实验:取一个100mL 的大量筒,用排饱和食盐水的方法先后收集20mL CH4和80mL Cl2,放在光亮的地方(注意:不要放在阳光直射的地方,以免引起爆炸),等待片刻,观察发生的现象。
装置:
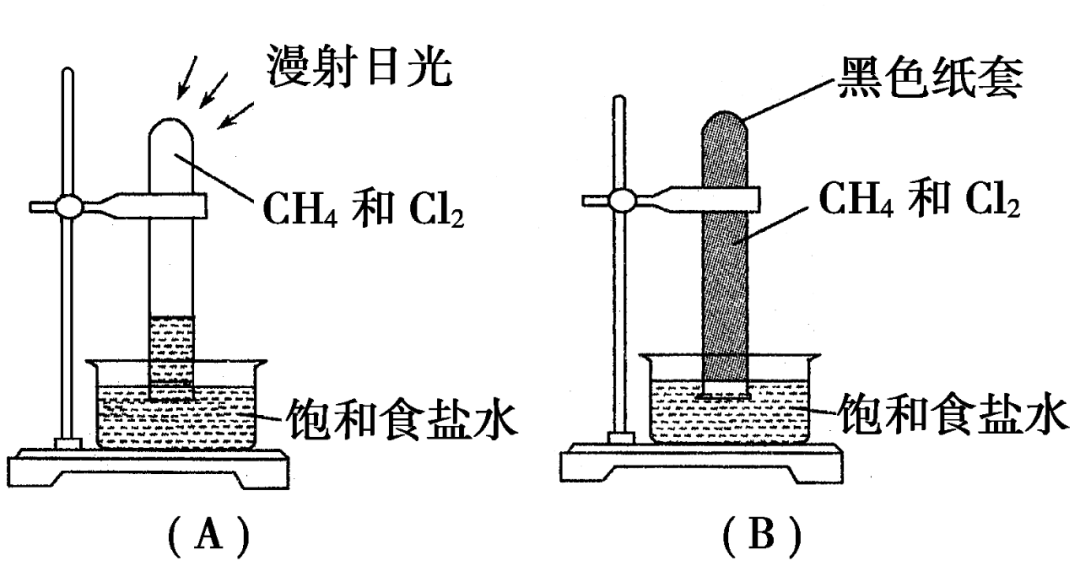
现象与解释:大约3min后,可观察到量筒壁上出现油状液滴,量筒内饱和食盐水液面上升。说明量筒内的混合气体在光照下发生了化学反应;量筒上出现油状液滴,说明生成了新的油状物质;量筒内液面上升,说明随着反应的进行,量筒内的气压在减小,即气体总体积在减小。
反应原理:
CH4+Cl2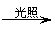 CH3Cl+HCl,
CH3Cl+HCl,
CH3Cl+Cl2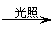 CH2Cl2+HCl,
CH2Cl2+HCl,
CH2Cl2+Cl2 CHCl3+HCl,
CHCl3+HCl,
CHCl3+Cl2 CCl4+HCl
CCl4+HCl
(二)石蜡油的分解
实验:将浸透了石蜡油(17个碳以上的液态烷烃混合物)的石棉放置在硬质试管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸气通过炽热的碎瓷片表面,发生反应,可得到一定量的气体生成物。
装置:
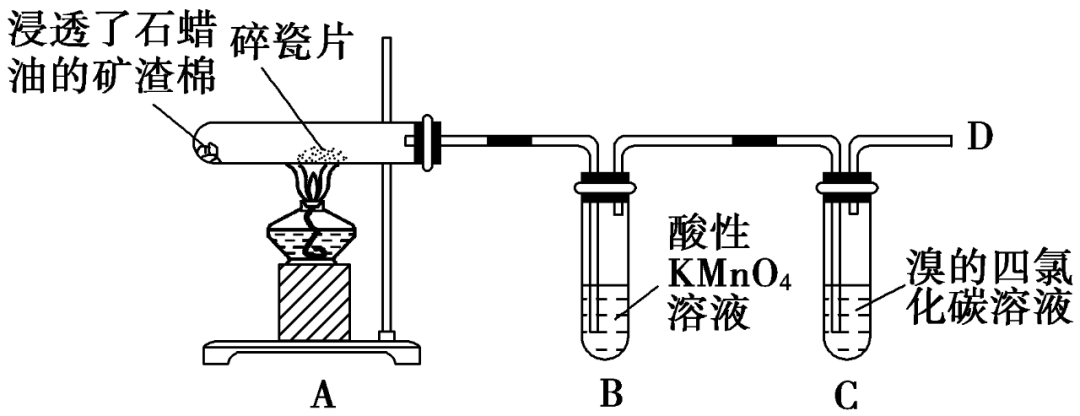
现象与解释:B中溶液紫红色褪去,C中溶液红棕色褪去,D处点燃火焰明亮并伴有黑烟。石蜡油在炽热碎瓷片的作用下,产生可以使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的气态产物,主要是乙烯和烷烃的混合物。
(三)乙烯
1.乙烯的制取
实验:在圆底烧瓶中加入乙醇和浓硫酸(体积比约为1∶3)的混合液20mL,放入几片碎瓷片,以避免混合液在受热时暴沸。加热混合液,使液体温度迅速升到170 ℃,将生成的气体通入KMnO4酸性溶液和溴的四氯化碳溶液中,观察并记录实验现象。
装置:
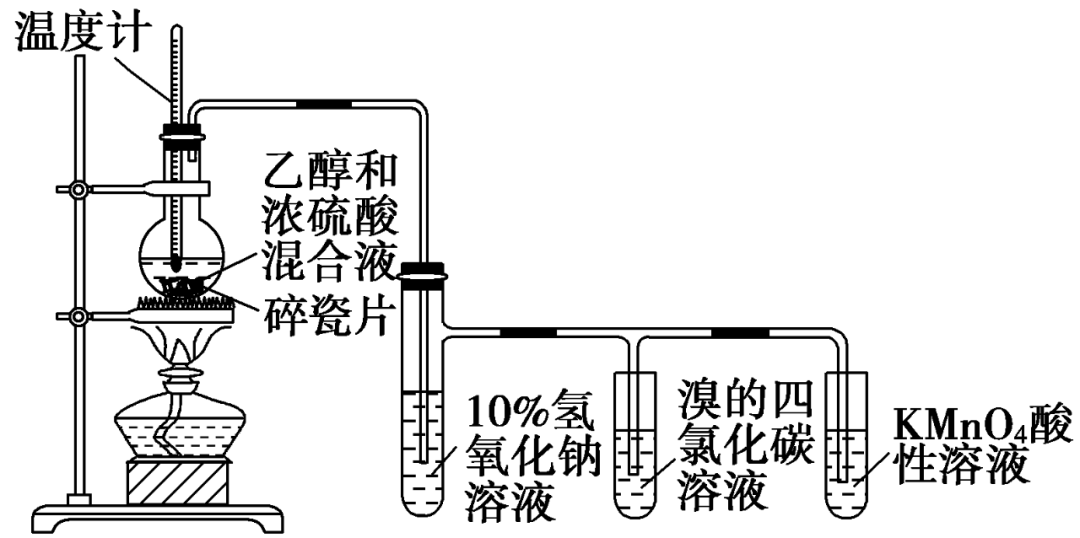
现象与解释:加热混合液时,温度要迅速上升到并稳定于170 ℃左右,生成乙烯;浓硫酸起催化剂和脱水剂的作用。由于反应物都是液体而无固体,所以要向烧瓶中加入碎瓷片,以防液体受热时发生暴沸;温度计要选择量程在200~300 ℃的为宜。温度计的水银球要置于反应液的中央位置,因为需要测量的是反应液的温度;氢氧化钠溶液的作用是除去混在乙烯中的CO2、SO2等杂质,防止干扰乙烯与溴的四氯化碳溶液和KMnO4酸性溶液的反应。
反应原理:CH3CH2OH CH2===CH2↑+H2O
CH2===CH2↑+H2O
2.乙烯的燃烧
实验:点燃纯净的乙烯。观察乙烯燃烧时的现象。
现象与解释:乙烯在空气中燃烧,火焰明亮,并伴有黑烟。乙烯中碳的质量分数较高,燃烧时有黑烟产生。
3.乙烯使KMnO4酸性溶液褪色
实验:把乙烯通入盛有KMnO4酸性溶液的试管里,观察试管里溶液颜色的变化。
现象与解释:KMnO4酸性溶液的紫色褪去,说明乙烯能被氧化剂KMnO4氧化,它的化学性质比烷烃活泼。
4.乙烯使溴的四氯化碳溶液褪色
实验:把乙烯通入盛有溴的四氯化碳溶液的试管里,观察试管里溶液颜色的变化。
现象与解释:溴的红棕色褪去,说明乙烯与溴发生了反应。
(四)乙炔
1.乙炔的制取
实验:在平底烧瓶(或大试管、广口瓶、锥形瓶等)中加入几块电石(CaC2),塞好双孔橡胶塞,打开分液漏斗活塞使水滴下,用排水法收集气体。
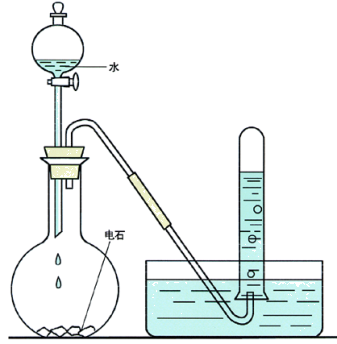
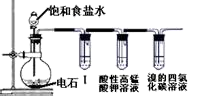
现象与解释:电石(CaC2)与水反应剧烈生成乙炔。此反应剧烈,为了得到平稳的乙炔气流,常用饱和食盐水代替水。反应装置不能用启普发生器。这是因为碳化钙与水反应剧烈,块状电石遇水后,立即变成粉末状,且反应放出大量热,会使启普发生器受热不均匀而炸裂。乙炔中H2S、PH3诸气体,可用CuSO4溶液洗气除去。
原理:CaC2+2H2O → Ca(OH)2↓ + CH≡CH↑
2.点燃纯净的乙炔
实验:点燃纯净的乙炔。观察乙炔燃烧时的现象。
现象与解释:乙炔燃烧时,火焰明亮,并伴有浓烈的黑烟。这是乙炔中碳的质量分数比乙烯还高,碳没有完全燃烧的缘故。
3.乙炔使KMnO4酸性溶液褪色
实验:把纯净的乙炔通入盛有KMnO4酸性溶液的试管里,观察试管里溶液颜色的变化。
现象与解释:KMnO4酸性溶液的紫色褪去,说明乙炔能与KMnO4酸性溶液反应。
4.乙炔使溴的四氯化碳溶液褪色
实验:把纯净的乙炔通入盛有盛有溴的四氯化碳溶液的试管里,观察试管里溶液颜色的变化。
现象与解释:溴的红棕色褪去,说明乙炔也能与溴发生加成反应。
(五)苯和苯的同系物
实验:苯、甲苯、二甲苯各2mL 分别注入3支试管,各加入3滴KMnO4酸性溶液,用力振荡,观察溶液的颜色变化。
现象与解释:苯不能使KMnO4酸性溶液褪去,说明苯分子中不存在碳碳双键或碳碳三键。甲苯、二甲苯能使KMnO4酸性溶液褪去,苯说明甲苯、二甲苯能被KMnO4氧化。
(六)苯的溴代反应和硝化反应
实验:在三颈烧瓶中加入少量铁粉,向三颈烧瓶上的一个滴液漏斗中加入5 mL 苯和1 mL 液溴的混合物,另一个滴液漏斗中加入30 mL 10%的氢氧化钠溶液,锥形瓶内注入蒸馏水,干燥管中加入碱石灰,连接好仪器,检查装置的气密性。先向三颈烧瓶中加入苯和液溴的混合物,观察三颈烧瓶和锥形瓶中出现的现象。反应完毕后,向三颈烧瓶中加入氢氧化钠溶液,观察三颈烧瓶中生成物的状态。
装置:
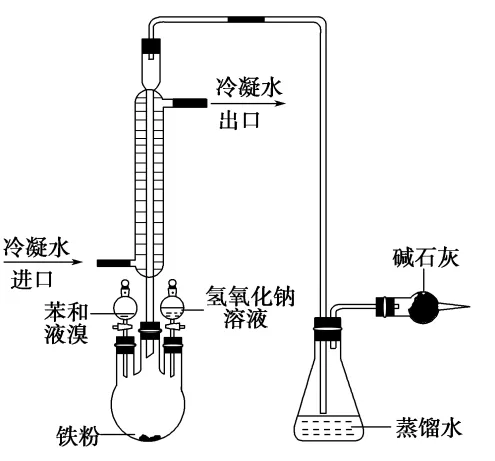
现象与解释:①将苯、液溴和铁粉混合后,很快会看到烧瓶中的混合液呈微沸状态,这说明此反应为放热反应;②导管末端有大量的白雾产生;③反应后的混合溶液分为两层,下层为溴苯(不溶于水且密度比水大的无色液体)。在有催化剂存在的条件下,苯与溴发生反应,苯环上的氢原子被溴原子取代生成溴苯。
反应原理:略
(七)卤代烃
1.溴乙烷的水解反应
实验:取一支试管,滴入10滴~15滴溴乙烷,再加入1mL5%的NaOH溶液,充分振荡、静置,待液体分层后,用滴管小心吸入10滴上层水溶液,移入另一盛有10mL 稀硝酸溶液的试管中,然后加入2滴~3滴2%的AgNO3溶液,观察反应现象。
装置:
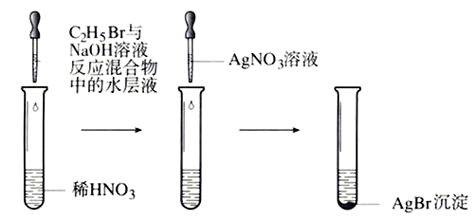
现象与解释:看到反应中有浅黄色沉淀生成,这种沉淀是AgBr,说明溴乙烷水解生成了Br-。
2.1,2-二氯乙烷的消去反应
实验:在试管里加入2mL1,2-二氯乙烷和5 mL10%NaOH的乙醇溶液。再向试管中加入几块碎瓷片。在另一支试管中加入少量溴水。用水浴加热试管里的混合物(注意不要使水沸腾),持续加热一段时间后,把生成的气体通入溴水中,观察有什么现象发生。
装置:
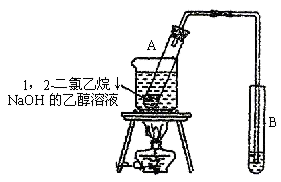
现象与解释:生成的气体能使溴水褪色,说明反应生成了不饱和的有机物。
(八)乙醇
1.乙醇与金属钠的反应
实验:在大试管里注入2mL 左右无水乙醇,再放入2小块新切开的滤纸擦干的金属钠,迅速用一配有导管的单孔塞塞住试管口,用一小试管倒扣在导管上,收集反应中放出的气体并验纯。
装置:

现象与解释:乙醇与金属钠反应的速率比水与金属钠反应的速率慢,说明乙醇比水更难电离出H+。
2.乙醇的消去反应
实验:在烧瓶中注入20mL 酒精与浓硫酸(体积比约为1:3)的混合液,放入几片碎瓷片。加热混合液,使液体的温度迅速升高到170℃。
现象与解释:生成的气体能使溴的四氯化碳溶液褪色,也能使高锰酸钾酸性溶液褪色。
3.乙醇的催化氧化
实验:将光亮的铜丝放在酒精灯火焰上灼烧,然后再趁热插入乙醇中。为了增强实验效果,可加以改进。
装置:

现象与解释:将发现铜丝先由紫红色变为黑色,插入乙醇中后,又变为紫红色,同时在乙醇中生成乙醛,可闻到乙醛的刺激性气味。反应中Cu作催化剂。
反应原理:2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
(九)苯酚
1.苯酚与NaOH反应
实验:向一个盛有少量苯酚晶体的试管中加入2mL 蒸馏水,振荡试管,有什么现象发生?再逐滴滴入5%的NaOH溶液并振荡试管,观察试管中溶液的变化。
现象与解释:苯酚与水混合,液体呈混浊,说明常温下苯酚的溶解度不大。当加入NaOH溶液后,试管中的液体由混浊变为澄清,这是由于苯酚与NaOH发生了反应生成了易溶于水的苯酚钠。
2.苯酚钠溶液与CO2的作用
实验:向苯酚与NaOH反应所得的澄清中通入CO2气体,观察溶液的变化。
装置:
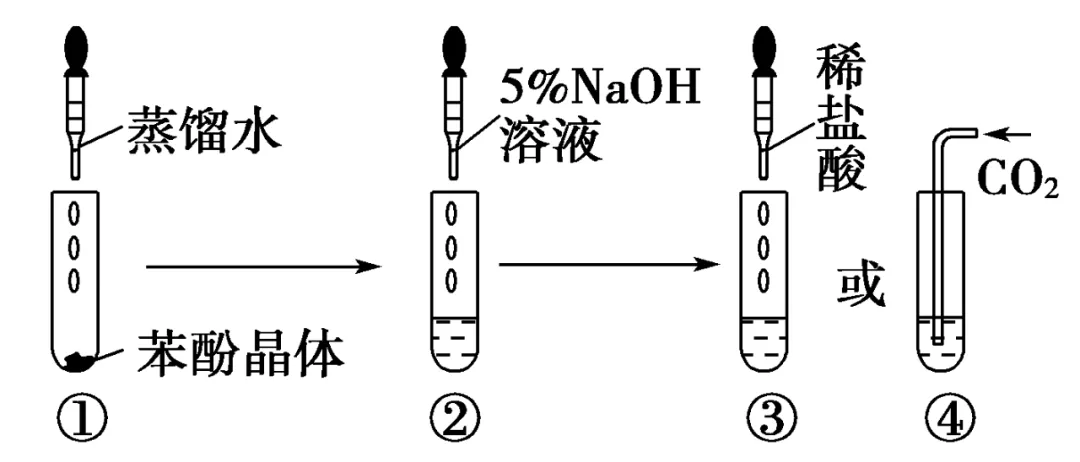
现象与解释:可以看到,二氧化碳使澄清溶液又变混浊。这是由于苯酚的酸性比碳酸弱,易溶于水的苯酚钠在碳酸的作用下,重新又生成了苯酚。
3.苯酚与Br2的反应
实验:向盛有少量苯酚稀溶液的试管里滴入过量的浓溴水,观察现象。
现象与解释:可以看到,立即有白色沉淀产生。苯酚与溴在苯环上的取代反应,既不需加热,也不需用催化剂,比溴与苯及其同系物苯环上的取代反应容易得多。这说明受羟基的影响,苯酚中苯环上的H变得更活泼了。
4.苯酚的显色反应
实验:向盛有苯酚溶液的试管中滴入几滴FeCl3溶液,振荡,观察现象。
装置:
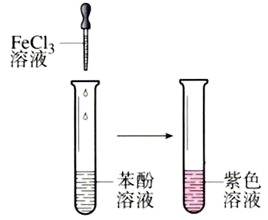
现象与解释:苯酚能与FeCl3反应,使溶液呈紫色。
(十)乙醛
1.乙醛的银镜反应
实验:在洁净的试管里加入1mL 2%的AgNO3溶液,然后一边摇动试管,一边逐滴加入2%的稀氨水,至最初产生的沉淀恰好溶解。再滴入3滴乙醛,振荡后把试管放在热水浴中温热。观察现象。
装置:
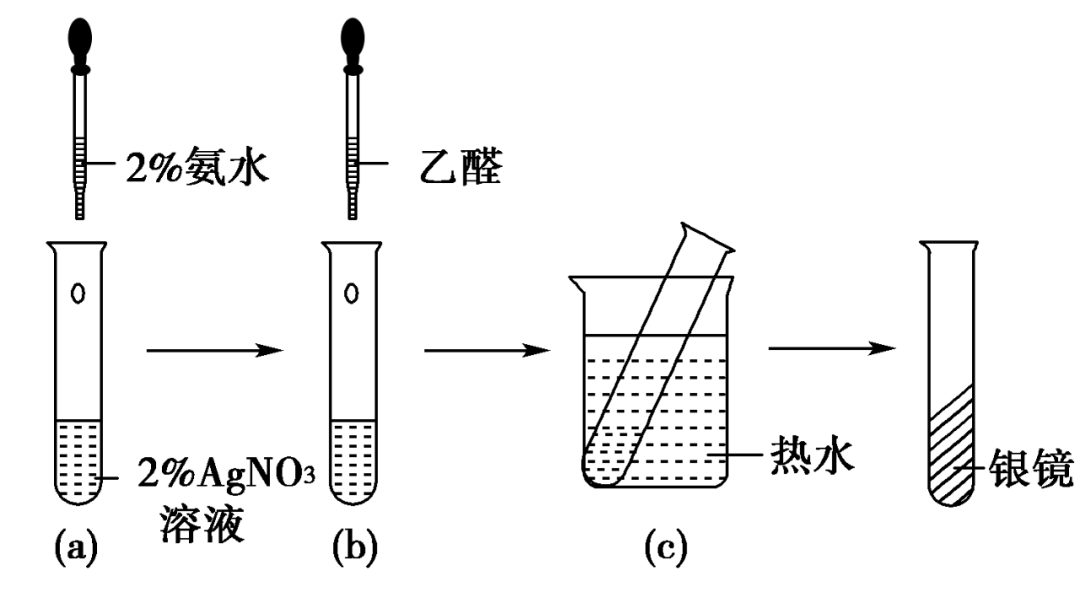
现象与解释:AgNO3与氨水生成的银氨溶液中含有的Ag(NH3)2OH是一种弱氧化剂,它能把乙醛氧化成乙酸,而Ag+被还原成金属银。
反应原理:CH3CHO+2Ag(NH3)2OH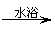 2Ag↓+CH3COONH4+3NH3+H2O
2Ag↓+CH3COONH4+3NH3+H2O
2.乙醛与Cu(OH)2的反应
实验:在试管中加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液4滴~6滴,振荡后乙醛溶液0.5 mL,加热至沸腾,观察现象。
装置:
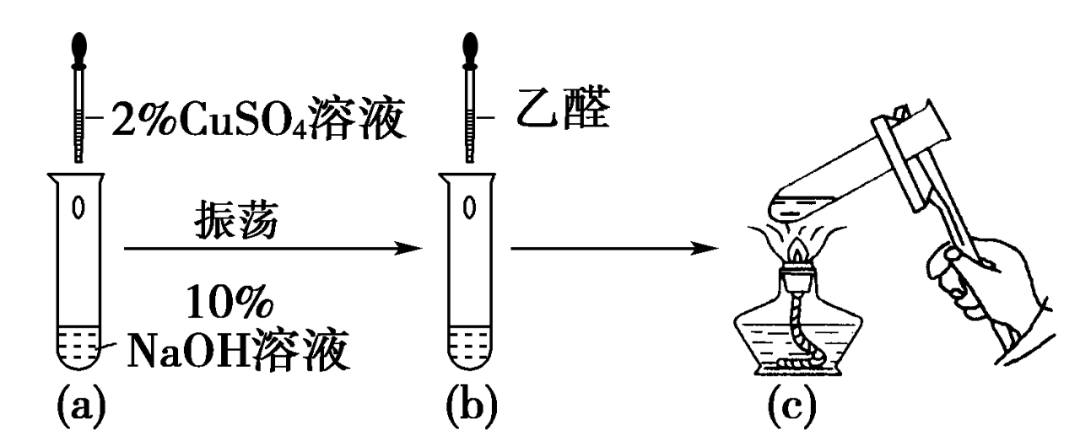
现象与解释:可以看到,溶液中有红色沉淀产生。反应中产生的Cu(OH)2被乙醛还原成Cu2O。醛基能将新制的Cu(OH)2还原为红色的Cu2O沉淀,这是检验醛基的另一种方法。该实验注意以下几点:①所用Cu(OH)2必须是新制的,在制备Cu(OH)2时,应向NaOH溶液中滴加少量硫酸铜,NaOH溶液必须明显过量。②加热时须将混合溶液加热至沸腾,才有明显的红色沉淀产生。③加热煮沸时间不能过久,过久将出现黑色沉淀,原因是Cu(OH)2受热分解为CuO。
反应原理:CH3CHO+2Cu(OH)2+NaOH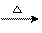 CH3COONa+Cu2O↓+3H2O
CH3COONa+Cu2O↓+3H2O
(十一)乙酸
1.乙酸与Na2CO3的反应
实验:向1支盛有少量Na2CO3粉末的试管里,加入约3mL 乙酸溶液,观察有什么现象发生。
现象与解释:可以看到试管里有气泡产生,说明乙酸的酸性强于碳酸。
2.乙酸的酯化反应
实验:在1支试管中加入3mL 乙醇,然后边摇动试管边加入2 mL 浓硫酸和2 mL 冰醋酸。用酒精灯小心均匀地加热试管3min~5min,产生的气体经导管通到Na2CO3饱和溶液的液面上。
现象与解释:在液面上看到有透明的油状液体产生,并可闻到香味。这种有香味的透明油状液体是乙酸乙酯。
(十二)乙酸乙酯
实验:在3支试管中各滴入6滴乙酸乙酯。向第一支试管里加蒸馏水5mL;向第二支试管里加稀硫酸(1:5)0·5mL、蒸馏水5mL;向第三支试管里加30%的NaOH溶液0.5mL、蒸馏水5mL。振荡均匀后,把3支试管都放入70℃~80℃的水浴里加热。
装置:
现象与解释:几分钟后,第三支试管里乙酸乙酯的气味消失了;第二支试管里还有一点乙酸乙酯的气味;第一支试管里乙酸乙酯的气味没有多大变化。实验说明,在酸(或碱)存在的条件下,乙酸乙酯水解生成了乙酸和乙醇,碱性条件下的水解更完全。
反应原理:CH3COOH+C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
(十三)葡萄糖
1.葡萄糖的银镜反应
实验:在1支洁净的试管里配制2mL 银氨溶液,加入1mL10%的葡萄糖溶液,振荡,然后在水浴里加热3min~5min,观察现象。
现象与解释:可以看到有银镜生成。葡萄糖分子中含醛基,跟醛类一样具有还原性。
2.与Cu(OH)2的反应
实验:在试管里加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液5滴,再加入2mL10%的葡萄糖溶液,加热,观察现象。
现象与解释:可以看到有红色沉淀生成。葡萄糖分子中含醛基,跟醛类一样具有还原性。葡萄糖与银氨溶液或新制Cu(OH)2悬浊液的反应,均需在加热和碱性条件下进行,否则不能产生银镜或砖红色沉淀。
(十四)蔗糖
实验:这两支洁净的试管里各加入20%的蔗糖溶液1mL,并在其中一支试管里加入3滴稀硫酸(1:5)。把两支试管都放在水浴中加热5min。然后向已加入稀硫酸的试管中加入NaOH溶液,至溶液呈碱性。最后向两支试管里各加入2mL 新制的银氨溶液,在水浴中加热3min~5min,观察现象。
现象与解释:蔗糖不发生银镜反应,说明蔗糖分子中不含醛基,不显还原性。蔗糖在硫酸的催化作用下,发生水解反应的产物具有还原性。
(十五)淀粉
实验:在试管1和试管2里各放入0.5g 淀粉,在试管1里加入4mL 20%的H2SO4溶液,在试管2里加入4mL 水,都加热3min~4min。用碱液中和试管1里的H2SO4溶液,把一部分液体倒入试管3。在试管2和试管3里都加入碘溶液,观察有没有蓝色出现。在试管1里加入银氨溶液,稍加热后,观察试管内壁有无银镜出现。
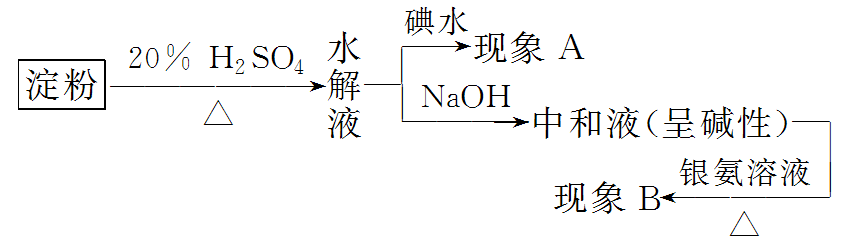
现象与解释:从上述实验可以看到,淀粉用酸催化可以发生水解,生成能发生水解反应的葡萄糖。而没有加酸的试管中加碘溶液呈现蓝色,说明淀粉没有水解。
情况 | 现象A | 现象B | 结论 |
① | 溶液呈蓝色 | 未产生银镜 | 未水解 |
② | 溶液呈蓝色 | 出现银镜 | 部分水解 |
③ | 溶液不呈蓝色 | 出现银镜 | 完全水解 |
(十六)纤维素
实验:把一小团棉花或几小片滤纸放入试管中,加入几滴90%的浓硫酸,用玻璃棒把棉花或滤纸捣成糊状。小火微热,使成亮棕色溶液。稍冷,滴入3滴CuSO4溶液,并加入过量NaOH溶液使溶液中和至出现Cu(OH)2沉淀。加热煮沸,观察现象。
现象与解释:可以看到,有红色的氧化亚铜生成,这说明纤维素水解生成了具有还原性的物质。
(十七)蛋白质
1.蛋白质的变性
实验:在两支试管里各加入3mL 鸡蛋白溶液,给一支试管加热,同时向另一支试管加入少量乙酸铅溶液,观察发生的现象。把凝结的蛋白和生成的沉淀分别放入两只盛有清水的试管里,观察是否溶解。
现象与解释:蛋白质受热到一定温度就会凝结,加入乙酸铅会生成沉淀。除加热外,紫外线、x射线、强酸、强碱、重金属盐以及一些有机物均能使蛋白质变性,蛋白质变性后,不仅失去了原有的可溶性,同时也失去了生理活性,是不可逆的。
2.蛋白质的颜色反应
实验:在盛有2mL 鸡蛋白溶液的试管里,滴入几滴浓硝酸,微热,观察现象。
现象与解释:鸡蛋白溶液遇浓硝酸变成黄色。蛋白质可以跟许多试剂发生特殊的颜色反应。某些蛋白质跟浓硝酸作用会产生黄色。
三、有机化学实验比较
(一)各类烃与液溴、溴水、溴的四氯化碳溶液、酸性KMnO4溶液反应的比较
液溴 | 溴水 | 溴的四氯化碳溶液 | 酸性KMnO4溶液 | |
烷烃 | 与溴蒸气在光照条件下取代 | 不反应,液态烷烃可发生萃取而使溴水层褪色 | 不反应,互溶,不褪色 | 不反应 |
烯烃 | 加成 | 加成褪色 | 加成褪色 | 氧化褪色 |
苯 | 一般不反应,催化可取代 | 不反应,发生萃取而使溴水层褪色 | 不反应,互溶,不褪色 | 不反应 |
(二)利用官能团的性质检验或鉴别有机物
物质 | 试剂与方法 | 现象与结论 |
饱和烃与不饱和烃 | 加入溴水或酸性KMnO4溶液 | 褪色的是不饱和烃 |
羧酸 | 加入新制Cu(OH)2悬浊液 | 蓝色絮状沉淀溶解 |
NaHCO3溶液 | 产生无色气泡 | |
葡萄糖 | 加入银氨溶液水浴加热 | 产生光亮银镜 |
加入新制Cu(OH)2悬浊液加热至沸腾 | 产生砖红色沉淀 | |
淀粉 | 加碘水 | 显蓝色 |
蛋白质 | 加浓硝酸微热(或灼烧) | 显黄色(或烧焦羽毛气味) |
(三)羧酸羟基、水羟基、醇羟基的性质比较
羟基类型 | CH3CO—OH | H—OH | CH3CH2—OH |
跟钾、钙、钠反应状况 | 特快速反应 | 快速反应 | 缓慢反应 |
跟锌、铁反应状况 | 较快反应 | 常温下不反应 | 不反应 |
跟氢氧化钠反应状况 | 快速反应 | 不反应 | 不反应 |
跟碳酸氢钠反应状况 | 快速反应 | 不反应 | 不反应 |
跟酸碱指示剂反应状况 | 快速反应 | 不反应 | 不反应 |
(四)渗析、盐析、变性的比较
渗析 | 盐析 | 变性 | |
内涵 | 利用半透膜分离胶体粒子与小分子和离子 | 加入无机轻金属盐使胶体中的物质析出 | 一定条件下,使蛋白质凝聚失去原有生理活性 |
条件 | 胶体、半透膜、水 | 浓的盐溶液如(NH4)2SO4、Na2SO4、NaCl溶液等 | 加热、紫外线、x射线、重金属盐、强酸、强碱、乙醇、丙酮等 |
变化实质 | 物理变化 | 物理变化 | 化学变化 |
特点 | 可逆,需多次换水 | 可逆,蛋白质仍保持原有活性 | 不可逆,蛋白质已失去原有活性 |
用途 | 除杂,如:除去淀粉溶胶中的NaNO3杂质 | 分离提纯蛋白质 | 消毒、灭菌,如:给果树使用波尔多液,保存动物标本等 |

- 全部评论(0)
