四个量子数含义与计算
时间:2023-12-11 09:41 来源:未知 作者:化学自习室 点击: 次 所属专题: 量子数
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在多电子原子中,由于各电子所具有的能量不同,因而分布在离核远近不同的区域内做高速运动。能量低的电子在离核近的区域内运动,能量高的电子在离核较远的区域内运动。
四个量子数:
(1)主量子数n: 描述原子中电子出现几率最大区域离核的远近(电子层数); 决定电子能量高低。
取值: n=1 2 3 4 5 6……
电子层符号 K L M N O P……
对于氢原子其能量高低取决于n
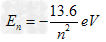
但对于多电子原子,电子的能量除受电子层影响,还因原子轨道形状不同而异,(即受角量子数影响)
(2)角量子数l:它决定了原子轨道或电子云的形状或表示电子亚层(同一n层中不同分层)意义:在多电子原子中,角量子数与主量子数一起决定电子的能量。之所以称l为角量子数,是因为它与电子运动的角动量M有关。
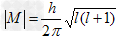
如M=0时,说明原子中电子运动情况同角度无关,即原子轨道或电子云形状是球形对称的。角量子数,l只能取一定数值。
(3)磁量子数m:决定波函数(原子轨道)或电子云在空间的伸展方向,决定角动量在空间的给定方向上的分量大小。
(4)自旋量子数ms:ms=±1/2,表示同一轨道中电子的二种自旋状态
ms称自旋量子数取值:ms=±1/2,即仅有两种运动状态。(↑↓)
用分辨力较强的光谱仪观察氢原子光谱,发现,大多数谱线是由靠得很近的两条谱线组成的。这是因为同一空间运动状态,即同一轨道中,可能有两种电子运动状态,即电子还有自身旋转运动,(类似于地球绕太阳转,自转)其自旋角动量沿外磁场方向的分量为
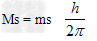
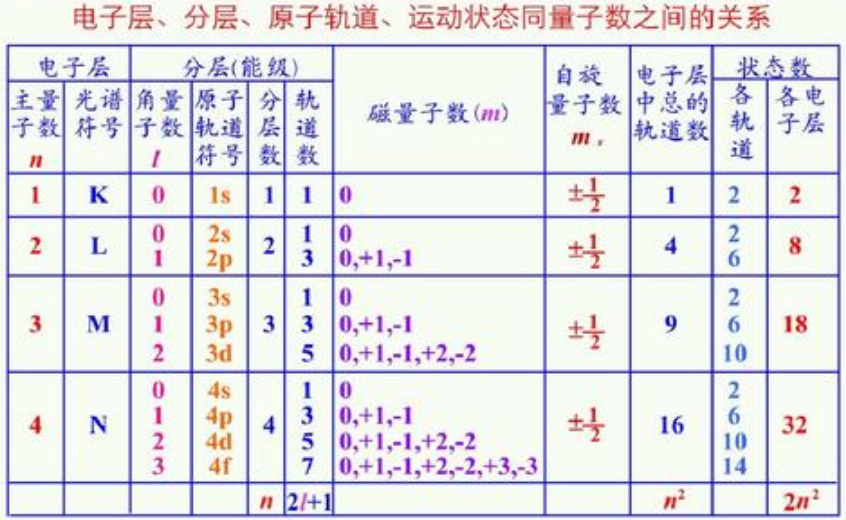
综合所述,若描述核电子的运动状态,需要四个量子数,即n、l、m、ms。
注意:n、l、m可描述核外电子的一种空间运动状态,即一个原子轨道。每个原子轨道中能容纳两个自旋相反的电子。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
