硫酸根离子检验总汇
时间:2016-01-21 18:16 来源:未知 作者:汪军 点击: 次 所属专题: 离子检验 硫酸根离子
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【关于硫酸根离子检验的各种表述】
(1)人教版第一册(必修)第82页,1995年10月第2版:“由此可见,用可溶性钡盐溶液和盐酸(或稀硝酸)可以检验硫酸根离子(SO42-)的存在。”
(2)人教版第一册(必修加选修),2003年6月第1版:“在实验室里,检验溶液中是否含有SO42-时,常常先用盐酸(或稀硝酸)把溶液酸化,以排除CO32-等离子可能造成的干扰。再加入BaCl2[或Ba(NO3)2]溶液,如果有白色沉淀出现,则说明原溶液中有SO42-存在”。
(3)人教版“化学1”第6页,2007年3月第3版:“在溶液中解离能产生SO42-的化合物与BaCl2溶液反应,生成不溶于稀盐酸的白色BaSO4沉淀。利用这一反应可以检验硫酸和可溶性硫酸盐。例如,Na2SO4溶液与BaCl2溶液反应的化学方程式:Na2SO4+BaCl2=BaSO4↓+2NaCl。”
(4)沪教版高中一年级第二学期(试用本)第17页,2007年1月第1版:“在实验室里,检验溶液中是否含有SO42-时,常常先用盐酸把溶液酸化,排除CO32-等离子可能造成的干扰,再加入BaCl2溶液,如果有白色沉淀出现,则说明原溶液中肯定有SO42-存在。”
(5)苏教版“化学1”第22页,2009年6月第5版:“人们常用向溶液中加入酸性氯化钡溶液的方法来检验溶液中是否含有硫酸根离子。”
(6)鲁教版“化学1”第46页,2007年7月第3版:“离子方程式和化学方程式都能描述化学反应,但离子方程式的描述更加本质,所表示的不仅仅是一个化学反应,而是一类化学反应,并揭示了这类化学反应的实质。例如,可溶性钡盐与可溶性硫酸盐(或硫酸)在溶液中反应的实质是Ba2+与SO42-结合生成难溶性的硫酸钡(BaSO4),其离子方程式为:Ba2++ SO42-= BaSO4↓。利用离子反应可以检验某种(或某些)离子是否存在。”
不难看出,上述表述中,(2)、(4)、(5)的表述基本相同,都是给出了检验SO42-的具体方案,这也是现在课堂教学中被广泛接受的一种,(1)、(3)、(6)只是给出了检验SO42-的反应原理。
【一般方法】
先加HCl溶液,若有沉淀或气体,则不断加HCl溶液,直到沉淀或气体不再产生为止,再加BaCl2溶液,若有沉淀,则说明原溶液中存在SO42-离子。
前提,该溶液中不存在在酸性条件下具有强氧化性的离子,如:NO3-和NO2-离子
典型例题:证明K2SO4、NaCl、Na2CO3、Na2SO3溶液中含有SO42-就是采用这样的方法。
【溶液中存在NO3-、NO2--以及SO32-离子时】
先加BaCl2溶液,沉淀完全,过滤,洗涤、然后在沉淀物中加过量HCl溶液,若沉淀不完全消失,则说明原溶液中存在SO42-
典型例题:原溶液中可能存在NO3-、NO2-、SO32-、SO42-,如何证明该溶液中可能存在SO42-。
【若溶液中可能存在NO3-、NO2-、SO32-、SO42-、SiO32-、AlO2-如何证明存在SO42-离子】
先加钡盐,沉淀完全,过滤,洗涤、在沉淀物中加过量HCl溶液,后加过量NaOH溶液,若有沉淀,则含有SO42-离子,否则无。
对于偏铝酸钡是否存在,是否沉淀也无关紧要了。
硫酸钡既难溶于水、难溶于酸和碱的基本知识的充分利用。
【其他的典型个案】
判断下列说法是否正确:
A.向某溶液中加入BaCl2溶液,产生白色沉淀,证明溶液中一定含有SO42-;
B.向某溶液中加入Ba(OH)2溶液,产生白色沉淀,证明溶液中一定含有SO42-;
C.向某溶液中加入Ba(NO3)2溶液,产生白色沉淀,证明溶液中一定含有SO42-。
显然,这三种说法都是错误的。这种采取极端思维方式命题,让学生知道Ag+、SO32-、CO32-、Mg2+会对SO42-的检验产生干扰就达到目的了。
三位同学设计了如下三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可证明试液中含有SO42-。
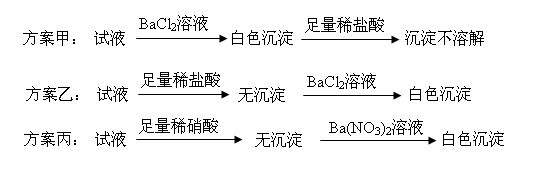
试评价上述各种方案是否严密,并分别说明理由。
参考答案是方案乙严密,理由是方案甲中Ag+会干扰,方案丙中SO32-被稀硝酸氧化会干扰,方案乙因排除了Ag+、SO32-的干扰而被认为严密。
值得注意的是,若某溶液完全是未知溶液,则高中阶段事实上无法很好地检验是否有SO42-离子的存在的。
在教材表述以及离子检验的命题中,都没有界定离子存在的环境到底是已知的,还是未知的,这就造成混乱。多数教材关于SO42-的检验方法,都是针对或暗指Ag+、SO32-、CO32-等几种离子造成的干扰,但都没有明确说明溶液的成分是指定的或已知的,读者都是按“未知溶液”去理解的,既然溶液成分是未知的、开放的,设计方案时就应考虑到更多离子可能造成的干扰。
如F-、PO43-、HPO42-、C2O42-、AlO2-、SiO32-、C17H35COO-等更多我们不知道性质的离子,它们的钡盐是否溶于水?是否白色沉淀?是否溶于稀盐酸?在“未知溶液”中检验SO42-时为什么不考虑它们的干扰?既然离子存在的环境是未知的,试图定制一个绝对化、万能的检验方案,当然是经不起推敲的。回顾前述题目中的检验方案(甲、乙、丙),题目对“试液”未作限制,应是“未知溶液”,既然是“未知溶液”,那么方案乙的严密性就值得商榷,因为乙方案可能再加盐酸以后,生成了SO42-离子。

- 全部评论(0)
