有机物的制备实验考点总结
时间:2020-03-30 21:17 来源:未知 作者:谢振超 点击:次 所属专题: 有机物制备
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
有机物的制备在近几年的新课标I卷的化学高 考题中连续出现,成为化学高考备考中不可忽视的 重要专题。在有机物的制备实验中,通常涉及的环节有:有机物的制备、有机物的分离提纯、有机物的产率计算。
―、有机物的制备
1.仪器。
①三颈圆底烧瓶。
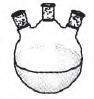
又称三口烧瓶,在有机化学实验中被广泛使用。它有三个口,可以同时加入多种反应物,或是加冷凝管。三口烧瓶 因瓶口很窄,不适用玻璃棒搅拌,若需要搅拌时,可以手握瓶口微转手腕即可顺利搅拌均匀,或是使用专用搅拌器。
常见的搅拌器:

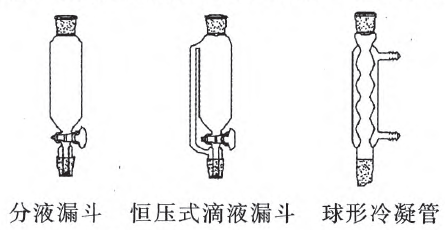
②分液漏斗或恒压滴液漏斗。作用:滴加液体。 通常可以控制滴加液体的速度,从而控制反应速度。
③温度计。控制反应的温度。
④球形冷凝管。作用:冷凝回流。使挥发的反 应物在冷凝管中液化,重新回流到反应装置,继续发 生反应。使用注意点:冷凝水要从下口进,上口出。
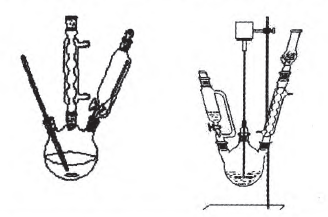
2.制备装置。
常见的反应装置如下所示(加热装置省略):
二、液态有机物的分离提纯
在新制的有机产物中,通常会混有有机物杂质 和无机物杂质。无机物杂质通常用相应的无机试剂 洗去;有机物杂质通常通过蒸馏法与有机产物分离开。
1. 除无机物杂质。
(1) 方法:用一些无机试剂洗涤。
(2) 仪器:分液漏斗。
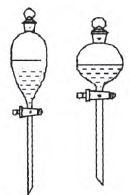
使用方法:
①查漏。
②萃取或洗涤有机物时,需要充分 振荡并放气。
③静置。将分液漏斗置于铁架台上静置。
④放出液体。打开上口玻璃塞(或使塞上的凹 槽对准漏斗口上的小孔),然后打开旋塞,放出下层 液体,上层液体从上口倒出。
(3) 步骤:
①水洗(借助溶解性原理,除去大量的易溶于水 的无机物),静置,分液。
②相应的溶液洗涤(进一步通过化学反应,除去 相应的无机物杂质),静置,分液。
③水洗或盐溶液洗(加盐的作用是降低有机物 在水溶液中的溶解度,目的是除去上一步加人的无 机试剂),静置,分液。
④干燥:有机物常用的干燥剂有:无水CaCl2、无 水 MgSO4、无水 Na2SO4 等。
⑤蒸馏:收集液态有机物。
2. 除去有机物杂质。
(1) 方法:蒸馏。
(2) 仪器:蒸馏烧瓶、温度计、直形冷凝管、牛角 管(或尾接管)、锥形瓶、铁架台等。
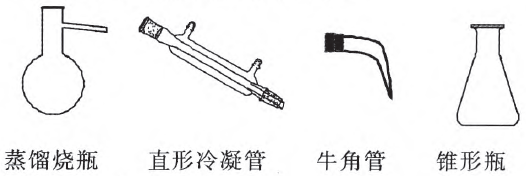
(3)蒸馏装置:
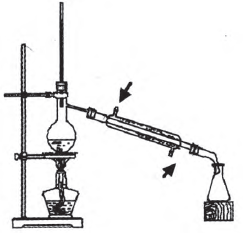
①实验注意事项:
A.温度计的水银球要置于蒸 馏烧瓶的支管口处(测馏分的沸点)。
B.冷凝水要从下口进,上口出。
C.蒸馏时,要事先在蒸馏烧瓶中加沸石,以防止 爆沸。
②特别说明:
A.产物必须蒸馏出来,在锥形瓶中收集。
B.收集产物时,温度计 的温度应该与产物的沸点一 致。
若是得到的有机物是固 态的,通常还要通过重结晶 提纯产品,如苯甲酸。
三、产率的分析
1. 增大产率的方法。
根据化学平衡移动原理,常用的方法有:增大某 种反应物的用量(往往是廉价的),及时分离出产物 (如酯的制备,用分水器及时分离出水分)。
2. 产率计算。

注意事项:在计算理论产量的时候,要注意反应 物的过量问题。
四、真题再现
1.苯乙酸铜是合成优良催化剂、传感材料―― 纳米氧化铜的重要前驱体之一。下面是它的一种实 验室合成路线:
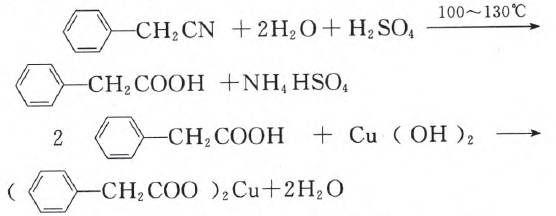
制备苯乙酸的装置示意图如右(加 热和夹持装置等略):
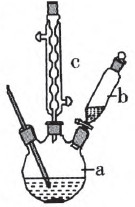
已知:苯乙酸的熔点为76.5 °C,微 溶于冷水,溶于乙醇。
回答下列问题:
(1) 在250 mL 三口瓶a中加人 70 mL 70%硫酸。配制此硫酸时,加入蒸馏水与浓 硫酸的先后顺序是 。
(2)将a中的溶液加热至100 °C,缓缓滴加40 g 苯乙腈到硫酸中,然后升温至130 °C继续反应。在 装置中,仪器b的作用是 ;仪器c的名称是 , 其作用是 。
反应结束后加适量冷水,再分离出苯乙酸粗品。
加人冷水的目的是____ 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A.分液漏斗B.漏斗C.烧杯D.直形冷凝 管E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g 纯品,则苯乙酸的产率是____ 。
(4)将苯乙酸加人到乙醇与水的混合溶剂中,充 分溶解后,加人Cu(OH)2搅拌30 min,过滤,滤液静 置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的 作用是__。
2. 正丁醛是一种化工原料。某实验小组利用如 下装置合成正丁醛。发生的反应如下:

实验步骤如下:
将6. 0 g Na2Cr2O7放人100 mL 烧杯中,加 30 mL 水溶解,再缓慢加入5 mL 浓硫酸,将所得溶 液小心转移至b中。在a中加入4. 0 g 正丁醇和几 粒沸石,加热。当有蒸汽出现时,开始滴加b中溶 液。滴加过程中保持反应温度为90〜95°C,在E中 收集90°C以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干 燥后蒸馏,收集75〜77°C馏分,产量2.0 g。
回答下列问题:
(1) 实验中,能否将Na2Cr2O7溶液加到浓硫酸 中,说明理由: 。
(2) 加人沸石的作用是 。若加热后发现未 加沸石,应采取的正确方法是 。
(3) 上述装置图中,B仪器的名称是,D仪器的名称是____ 。
(4) 分液漏斗使用前必须进行的操作是__ (填 正确答案标号)。
A.润湿B.干燥C.检漏D.标定
(5) 将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)。
(6) 反应温度应保持在90〜95°C,其原因是
(7)本实验中,正丁醛的产率为 _
参考答案
1.
(1)先加水,再加入浓硫酸
(2)滴加苯乙腈 球形冷凝管 回流(或使气化的反应液冷凝)便于苯乙酸析出 BCe
(3) 重结晶 95%
(4) 增大苯乙酸的溶解度,便于充分反应
2.
(1)不能,浓硫酸溶于水会放出大量热,容易溅出伤人
(2) 防止液体暴沸冷却后补加
(3)分液漏斗 冷凝管
(4)C
(5)下
(6)为了将正丁醛及时分离出来,促使反应正向进行,并减少正丁醛进一步氧化
(7)51

- 全部评论(0)
