变途径解化学平衡题
时间:2020-02-16 10:42 来源: 作者:张澳 点击: 次 所属专题: 等效法
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
化学平衡这一部分内容理论性强,对逻辑思维能力有较高要求,这就要求学生在应试时必须快而准,而要达到这一目的,寻找一条快速解题的途径显得尤为重要。现举例就巧变平衡途径速解化学平衡试题谈点看法。
例1.(1998年高考试题)体积相同的甲乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )。
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )。
A.等于p%
B.大于p%
C.小于p%
D.无法确定
解析:设甲、乙两容器中变化途径如下:
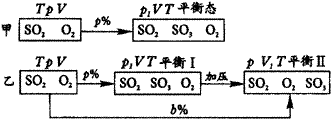
从平衡Ⅰ→Ⅱ,需要加压:2SO2+O2![]() 2SO3,平衡右移,使SO2转化率增大,故b%>p%,即选B。
2SO3,平衡右移,使SO2转化率增大,故b%>p%,即选B。
例2.(1996年测试题)一真空密闭容器中盛有1molPCl5,加热到200℃时发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)反应达到平衡时,PCl5所占体积百分数为m%,若在同一温度和同一容器中最初投入的量2molPCl5,反应达到平衡时,PCl5所占体积百分数为n%,则m和n的正确关系是()。
PCl3(g)+Cl2(g)反应达到平衡时,PCl5所占体积百分数为m%,若在同一温度和同一容器中最初投入的量2molPCl5,反应达到平衡时,PCl5所占体积百分数为n%,则m和n的正确关系是()。
A.m>n B.m<n C.m=n D.无法比较
解析:图示两容器中气体变化途径:
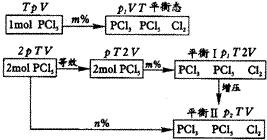
从平衡Ⅰ→Ⅱ需要增压,PCl5(g)![]() PCl3(g)+Cl2(g), 平衡左移,PCl5分解率减小,故m<n,应选B。
PCl3(g)+Cl2(g), 平衡左移,PCl5分解率减小,故m<n,应选B。
例3.可逆反应A(g)+B(g)![]() 2C(g)在固定容积的容器中进行,如果向容器中充入1molA和1molB,在某温度下达平衡时,C的体积分数为m%,若向容器中充入1molC,在同样温度下,达到平衡时,C的体积分数为n%,则m和n的正确关系是( )。
2C(g)在固定容积的容器中进行,如果向容器中充入1molA和1molB,在某温度下达平衡时,C的体积分数为m%,若向容器中充入1molC,在同样温度下,达到平衡时,C的体积分数为n%,则m和n的正确关系是( )。
A.m>n B.m<nC.m=nD.无法确定
解析:向容器中充入1molC就相当于向容器中充入0.5molA和0.5molB时的状态,则两容器中气体变化途径如下:
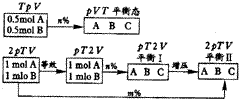
从平衡Ⅰ→Ⅱ,需要增压:A(g)+B(g)![]() 2C(g)平衡不移动,即C的百分含量不变,应选C。
2C(g)平衡不移动,即C的百分含量不变,应选C。
通过对以上3例的分析,我们可以看到巧变平衡途径在解析化学平衡类试题时,不失为一种有效方法。

- 全部评论(0)
