气压变化在解答实验题中的十大应用
时间:2020-03-07 13:17 来源:未知 作者:潘祥泰 点击: 次 所属专题: 压强 高考实验
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一.“H2还原CuO”实验中生成物Cu的冷却
操作要求是:待反应完全后撤走酒精灯且继续通H2至Cu冷却为止。防止撤灯后的温度骤降,造成装置内气压减小致使空气倒吸入热的试管中,这样保证生成的铜不被氧化为CuO。即H2应该“早出晚归”。
二.检验装置的气密性
装置气密性的检验是中学化学实验的基本操作之一。解答这类题目要答准、答全,既要答出操作方法,又要答出观察到的现象,还要答出判断气密性是否良好的结论,三者缺一不可。检验气密性的常用方法有两种:
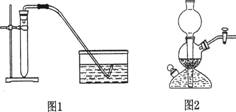
①微热法(如图1):用手捂热试管(或用酒精灯微热),导气管末端产生气泡,松手后导管末端有一段水柱上升,证明装置气密性良好(即“手捂加热有气泡,松手冷却有液柱”);
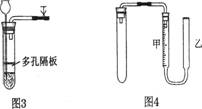
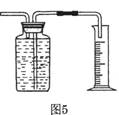
②液差法:图2是启普发生器,关闭导气管,向球形漏斗中加水,使漏斗中的液面高于容器中的液面,一段时间后,液面差不变,说明装置气密性良好;图3装置与启普发生器类似,检验方法相同:图4中乙管内注入水后,上移乙管,使其液面比甲管高,固定后液面差不发生变化,证明装置气密性良好。
|
|
|
三.测量气体体积及读取数据的策略
在化学实验中,常用一个洗气瓶(广口瓶)和一个量筒组装成量气装置(如图5),利用气体的压强将洗气瓶中的液体压入量筒,测量气体的体积。
例1某化学课外活动小组利用如图所示的装置将NO2和O2的混合气通入水中反应,并测定反应后混合气的体积。将标况下50mL NO2和10mL O2的混合气通入反应装置后,
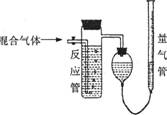
(1)试计算反应后剩余的气体在标况下的体积,为___________;
(2)在读取量气管体积时应注意的问题是_______________________________________。
解析:(1)由反应4NO2+O2+2H2O=4HNO3可知NO2剩余10mL,因3NO2+H2O=2HNO3+NO,故剩余的气体为NO,共 10/3 mL。
(2)在读取量气管体积时应注意液面和视线的问题。
答案:(1) 10/3 mL (2)①上下移动量气管,使前后两次读数时均保持量气管内液面和球形容器内液面相平:②读数时视线应与量气管内凹液面相切。
四.确定洗气装置中净化剂的状态及进气的方向

分析图示的净化装置必有如下规律:
(1)若A管长B管短,则净化剂(吸收剂)必为液体,且一定是A管进气B管出气(长进短出);(2)若气流方向是短进长出,必会使液体受压而流出,你能分析出其中 的“倒吸”道理吗?A、B管如果均短(稍露出橡皮塞),则净化剂必为固体,由A或B管进气均可。
五.液体的倒吸及防止
将气体通入某一液体或溶液中,如果该气体极易溶解或反应,就会使反应容器内压强迅速减小,导致液体倒吸进入反应容器,发生危险。所以要用防倒吸装置进行实验。我们平常所接触到的,如用钢笔吸取墨水,胶头滴管吸取液体、移液管移取定量液体等都是倒吸原理的最直接应用。实验中吸收多余的易溶性气体(如HCl、NH3、SO2、HBr等)时,常法是在导管末端连接一个倒扣的小漏斗,且使其边缘恰好与水面接触。也可将导管末端直接脱离液面,但距水面以1-2mm为宜。其目的都是为了防止倒吸。
例2双球洗气管是一种多用途仪器,常用于杂质去除、气体干燥、气体吸收(能防止倒吸)等实验操作。右图是用水吸收下列某气体时的情形,根据下面附表判断由左方进入的被吸收气体是( )
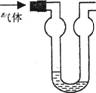
A.Cl2 B.HCl C.H2S D.CO2
解析:由这些常见气体的溶解性关系可以知道HCl的溶解度最大,溶解的速率大于气体进入洗气管的速率,导致洗气管左侧气压降低:出现如图所示的情形。
答案:B。
六.制备白色的Fe(OH)2
在化学实验中可利用气压将液体压入另一反应器以达到实验目的。
例3 在右图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备白色的Fe(OH)2沉淀。
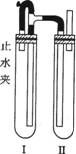
(1)在试管I里加入的试剂是________________。
(2)在试管Ⅱ里加入的试剂是___________。
(3)为了制得白色Fe(OH)2沉淀,在试管I和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是______________
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是________________________________________。
解析:两支试管,试管Ⅱ是开口式,无法用产生的气体将液体压入试管I中,所以铁屑和稀H2SO4应放在试管I中,试管Ⅱ中加入的是NaOH溶液。当铁与稀H2SO4反应时,产生的H2可从试管I的短管中导出,可将试管I和试管Ⅱ中的空气排尽。然后关闭止水夹,试管I内产生的H2将试管I的FeSO4等溶液压入试管II中,与NaOH溶液反应生成白色的Fe(OH)2沉淀,整个过程都处于H2的环境中,Fe(OH)2沉淀不会被氧化,可较长时间保持白色。
答案:(1)稀H2SO4铁屑 (2)NaOH溶液
(3)检验试管Ⅱ出口处排出氢气的纯度,当排出的H2纯净时,再夹紧止水夹。
(4)试管I中反应生成的H2充满了试管I和试管Ⅱ,且外界空气不容易进入。
七.启普发生器原理及装置的变通设计
例4 从下面三个反应中可以用图示这种随制随停的制气装置制取的气体的是_______
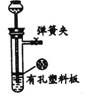
①大理石与盐酸反应制取二氧化碳
②黄铁矿与盐酸反应制取硫化氢
③用二氧化锰催化分解过氧化氢制氧气
解析:启普发生器制备气体的条件:(1)块状固体与液体反应;(2)反应不需要加热;(3)生成的气体不溶于水。凡符合以上三条的气体制备,均可用该题装置。显然①可行,③不可行(二氧化锰是粉末而不是块状固体)。对于②中 FeS2跟盐酸怎样反应,却是很陌生的。如果能积极联想,疑虑自然排除。FeS2与Na2O2在形式上相似,S和O又位于同一主族,联想到O22-与S22-在结构和性质上相似。
经过以上的联想,可以明确:FeS2不仅与盐酸能反应,而且产生是H2S。因此②也可行
这种以新情景联系旧背景,将熟悉的知识、方法正向迁移到未知的领域,使其在新情景中开花结果。这一过程就是创新,就是发展。如果在学习过程中,能经常的运用联想,学生的创新能力一定会提高。
答案:①②
例5 现有用品:仪器:单孔橡皮塞、双孔橡皮塞、球形干燥管、破底试管、 U形管、塑料垫圈、塑料盖、烧杯、铜丝、带活塞的导管等。药品:FeS固体、浓H2SO4、蒸馏水、浓盐酸、Na2S固体。试运用创造性思维,设计出尽可能多的简易的能随开随用、随关随停的H2S气体发生器(画出装置图)。
答案:
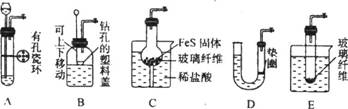
八.“喷泉”实验的变压原理
例6 “喷泉”是一种常见的自然现象,其产生原因是存在压强差。
(1)做氨的喷泉实验时,若要在图(A)装置中收集一瓶氨气,氨气应由____口进入,原因是_________________。
(2)某学生做喷泉实验时,用向下排空气法在体积为V mL 的烧瓶中收集氨气,最后所得气体对氢气的相对密度为10.5,将此充满气体的烧瓶倒置于水中,瓶内水面上升到一定高度停止。则在同温同压下瓶内剩余气体的体积为_______mL。
(3)如图(B)为化学教材中所用的喷泉实验装置。在烧瓶中充满干燥的气体,胶头滴管及烧杯中分别盛有液体,下列组合中不可能形成喷泉是②(填序号);
①HCl和H2O ②O2和H2O ③NH3和H2O④CO2和NaOH溶液
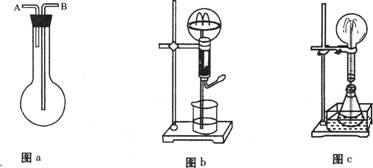
(4)某学生积极思考产生喷泉的其他方法,并设计了图(C)所示的装置。在图(C)所示的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是④(填序号)
①Cu和稀H2SO4 ②NaHCO3和NaOH溶液 ③CaCO3和稀H2SO4 ④NH4HCO3和稀盐酸
(5)在图(C)锥形瓶外放一水槽,瓶内加入酒精,水槽中加入冷水后,再加人足量的下列物质,结果也产生了喷泉。水槽中可以加入的物质可以是①(填序号)
①浓H2SO4 ②食盐 ③硝酸钾 ④硫酸铜
(6)比较图(B)和图(C)两套装置,以产生喷泉的原理来分析,图(B)是_______上部烧瓶内压强;图(C)________下部锥形瓶内气体压强(填“增大”或“减小”)。城市中常见的人造喷泉及火山喷发的原理与上述图 _______(填“图(B)”或“图(C)”)装置的原理相似。
解析:(1)气体的收集方法取决于气体的物理性质,NH3极易溶于水,且密度比空气小(17<29),因此,只能用向下排空气法收集。采用图(A)的装置收集时,要分清空气是从哪个导管中排出的。
(2)根据所得气体对氢气的相对密度为10.5可知,烧瓶内气体的相对分子质量为21,说明氨气没有收集满,我们把烧瓶内气体看作是空气和氨气两部分,根据空气的平均相对分子质量29和氨气的相对分子质量17,采用“十字交叉”法可求出烧瓶中NH3与空气的体积比。瓶内剩余气体的体积V/3 mL 。
(3)图(B)装置形成“喷泉”是因为烧瓶内气体极易溶解于烧杯和滴管中的液体,使烧瓶内的压强突然减少而产生压强差形成 “喷泉”。显然只有②中没有压强的变化。
(4)图(C)装置恰恰相反,下部烧瓶中的物质相互反应产生气体,使锥形瓶内气体压强增大而产生压强差,将液体从下瓶中压入到上瓶形成喷泉.所给选项涉及到化学反应为NaHCO3+NaOH=Na2CO3+H2O CaCO3+H2SO4=CaSO4+CO2↑ NH4HCO3+HCl=NH4Cl+CO2↑,注意CaSO4微溶于水,会使反应生成的CO2气体的量迅速减少而很快停止。只有④符合题意。
(5)酒精是易挥发物质,当温度升高时酒精的挥发将加快,显然浓硫酸遇水放出的大量热提供了热源。
答案:(1)A NH3密度比空气小 (2)V/3 mL (3)② (4)④ (5)① (6)减小 增大 图(C)
例7 如图(1)
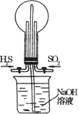
常温下将H2S、SO2以1:1充满烧瓶,不久烧瓶中能观察到的现象是________________________________。
(2)若用Cl2代替SO2,其余同图,观察到现象与(1)相同和不同之处分别为_______________________________________。
解析:(1)由于有反应2H2S+SO2==3S↓+2H2O.SO2+2NaOH==Na2SO3+H2O导致烧瓶内压强减小,造威压强差形成喷泉。
(2)由于发生Cl2+H2S=S↓+2HCl,反应前后气体体积未变,未能形成压强差,所以看不到喷泉现象。好多学生误认为HCl与NaOH反应或溶解而形成喷泉,其实长直玻璃导管导致HCl与NaOH溶液没有接触的机会(被空气隔绝了)。
答案:(1)烧瓶内壁有水珠且有黄色固体析出。NaOH溶液喷入烧瓶内。
(2)有黄色晶体析出,无喷泉现象。
九.“喷烟”及“双喷泉”现象的产生
例8如图所示,实验前A、B、C活赛均关闭。
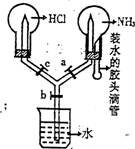
(1)若要在装置中产生“喷烟”现象,其操作方法是 ___________________________________________________
(2)若要产生双喷泉现象,最佳的操作方法是______________。
解析:(1)先打开A、C、活塞(保证气路的畅通),再挤压胶头滴管(原理是:NH3溶解的瞬间必导致左烧瓶中的HCl迅速倒吸进入右烧瓶并敷.剧烈反应NH3+HCl=NH4Cl而产生“发烟”现象)。
(2)的最佳操作是先挤压胶头滴管,再打开A、C活塞,最后打开b活塞(为什么呢?)。
答案:略
十.易拉罐变形
例9 在铝制易拉罐内充满CO2气体,再加入20mL 6 mol·L-1NaOH溶液(足量)并立即封闭罐口,一段时间后可观察到的现象是______。
解析:因反应2NaOH+CO2=Na2CO3+H2O使罐内压强逐渐减小,但空气不能倒吸入罐内, 故易拉罐将逐渐变瘪. 而后随反应2Al +2NaOH+2H2O=2NaAlO2+3H2 ↑ 的发生,罐内气压又逐渐增大,致逐渐鼓起。因NaOH足量,最终会将罐底的铝耗完造成液体泄漏现象的发生。答案:略。
可见,准确分析气体压强的变化与倒吸之间的辩证关系,就会使好多实验操作及实验现象的推断或解释等问题迎刃而解。

- 全部评论(0)